Перейти к:
Клинико-экспериментальные параллели в обосновании способа герниопластики срединных послеоперационных вентральных грыж
https://doi.org/10.21886/2219-8075-2024-15-1-108-114
Аннотация
Цель: разработка, клиническое применение нового оригинального метода герниопластики срединных послеоперационных вентральных грыж и биомеханическое экспериментальное обоснование эффективности данного способа.
Материалы и методы: разработан и клинически апробирован на 63 пациентах метод герниопластики срединных послеоперационных вентральных грыж с укреплением рубцово-измененных структур грыжевых ворот. В рамках анатомического эксперимента исследованы биомеханические показатели укрепленных тканей срединных отделов передней брюшной стенки по оригинальной методике.
Результаты: установлено повышение биомеханических показателей срединных структур, укреплённых по оригинальной методике каркасной нитью в сравнении с рубцово-измененной фасцией у грыженосителей. Предел прочности фасции увеличился на 59,4%, а модуль упругости — на 40,2%. Данные результаты позволяют предположить уверенную профилактику рецидивов грыжеобразования при применении данной методики. Данное предположение подтверждено после внедрения методики в клиническую практику. У всех 63 наблюдаемых пациентов отсутствует рецидив грыженосительства в течение 1–5 лет. Отсутствовали значимые осложнения течения раннего послеоперационного периода, связанные с примененным способом пластики. Способ характеризуется материальной и финансовой доступностью, отсутствием сложных технических манипуляций, увеличивающих продолжительность герниопластики.
Выводы: эффективность в профилактике рецидивов грыжеобразования, доступность и простота исполнения предложенного способа хирургического лечения послеоперационных и рецидивных вентральных грыж позволяет рекомендовать его к широкому клиническому применению.
Для цитирования:
Коробка В.Л., Татьянченко В.К., Даблиз Р.О., Толстопятов С.В., Гончар М.В., Клец И.С. Клинико-экспериментальные параллели в обосновании способа герниопластики срединных послеоперационных вентральных грыж. Медицинский вестник Юга России. 2024;15(1):108-114. https://doi.org/10.21886/2219-8075-2024-15-1-108-114
For citation:
Korobka V.L., Tatyanchenko V.K., Dabliz R.O., Tolstopyatov S.V., Gonchar M.V., Kletz I.S. Clinical and experimental parallels in the substantiation of the method of hernioplasty of postoperative ventral hernias of median localization. Medical Herald of the South of Russia. 2024;15(1):108-114. (In Russ.) https://doi.org/10.21886/2219-8075-2024-15-1-108-114
Введение
Послеоперационная вентральная грыжа — заболевание передней брюшной стенки, возникающее после лапаротомных операций. Представляет собой выхождение органов брюшной полости через дефект мышечно-апоневротического слоя в области послеоперационного рубца, покрытый париетальной брюшиной1,2. Данное осложнение является одним из самых частых (от 2 до 28%) после операций на органах брюшной полости [1][2][3].
Причинами образования послеоперационных вентральных грыж являются ошибки ушивания лапаротомной раны и выбора оперативного доступа (выполнение необоснованно больших разрезов, не учитывающих особенности топографо-анатомическое строения передней брюшной стенки, пересечение мышц, магистральных сосудов и нервов) [4][5]. Следует отметить, что зачастую послеоперационные грыжи, причиняют больному больше страданий, чем первоначальное заболевание, которое послужило причиной лапаротомии, тем самым являясь причиной повторных хирургических вмешательств [6][7].
Лечение послеоперационных вентральных грыж в настоящее время невозможно представить без применения сетчатых эндопротезов и соблюдения принципов ненатяжной аллопластики, особенно при больших размерах грыжевых выпячиваний [2][7]. Одним из важных моментов ненатяжной герниопластики является расположение и фиксация аллотрансплантата, так как именно он определяет эффективность создаваемой конструкции и профилактирует риск рецидива грыженосительства [7][8].
Цель исследования — разработка, клиническое применение нового оригинального метода герниопластики срединных послеоперационных вентральных грыж и биомеханическое экспериментальное обоснование эффективности данного способа.
Материал и методы
Работа учитывает результаты собственного анатомо-морфологического экспериментального исследования [9] целевых фасциальных структур срединного отдела брюшной стенки, проведённых по методике Татьянченко В.К.3 [10]. Нами ранее проведены биомеханические исследования нативных препаратов фасциально-анатомических образований области прямых мышц живота, а также препаратов рубцово-измененных фасциально-анатомических структур грыжевых ворот на стенде ИСС-500 (государственный реестр №16540-97) с помощью датчика силы Scaima ZF-500 (Франция). Были определены предел прочности (Ϭ) и модуль упругости (Е). Расчёты этих параметров проводили по формулам
Ϭ=Р/F, Е=Ϭ/е, е=∆L/L,
где Р — нагрузка на образец исследования, F — площадь поперечного сечения образца, L — длина образца, ∆L — абсолютное удлинение, е — продольная деформация. Установлено, что у грыженосителей предел прочности рубцово-измененных участков передней брюшной стенки был снижен в 1,5–1,9 раза, а модуль упругости — в 1,9–2,5 раза по сравнению с аналогичными показателями нативных препаратов. Таким образом, в проведённом ранее исследовании определена необходимость повышения прочности рубцово-измененных тканей у грыженосителей при выполнении герниопластики для профилактики рецидива грыжеобразования.
Нами разработан и клинически апробирован метод герниопластики срединных послеоперационных вентральных грыж с укреплением фасциально-апоневротических структур передней брюшной стенки (патент РФ №2685682)4.
Основными этапами предложенного способа являются иссечение послеоперационного рубца, выделение и обработка грыжевого мешка, ушивание брюшины, пластика грыжевого дефекта сетчатым протезом, который фиксируют П-образными швами, дополнительно предбрюшинно на расстоянии 1,5–2 см от края грыжевых ворот в виде петли проводят толстую нить из синтетического нерассасывающегося материала (далее каркасная нить), концы нити выводят в углу раны, по обе стороны грыжевых ворот через мышцы в проекции петли каркасной нити накладывают П-образные швы таким образом, чтобы захватить расположенную под мышцами каркасную нить, при этом расстояние между швами должно быть не менее 1,5 см и не более 2,5 см, поверх мышц укладывают сетчатый эндопротез, продольный размер которого соответствует продольному размеру грыжевого дефекта, а поперечный — выступает на 0,5 см от линии П-образных швов, протез фиксируют ранее наложенными П-образными швами, по мере завязывания которых петлю каркасной нити подтягивают, а по завершении фиксации сетчатого протеза — завязывают. Указанные этапы иллюстрируются на рис. 1–4.
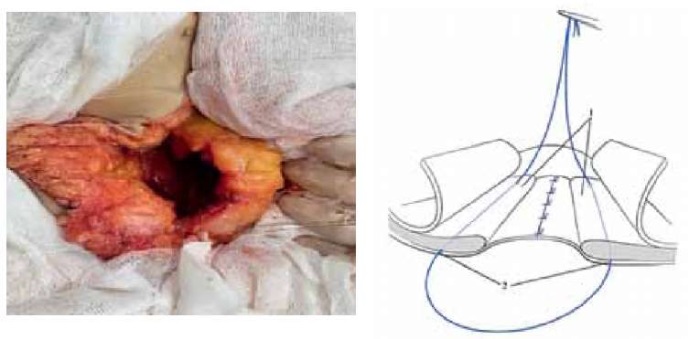
Рисунок 1. Анатомический эксперимент и схема.
Проведение нерассасывающейся каркасной нити
и создание петли по окружности грыжевых ворот.
Figure 1. Anatomical experiment and diagram.
Carrying out a non-absorbable frame thread
and creating a loop around the circumference of the hernial gate.
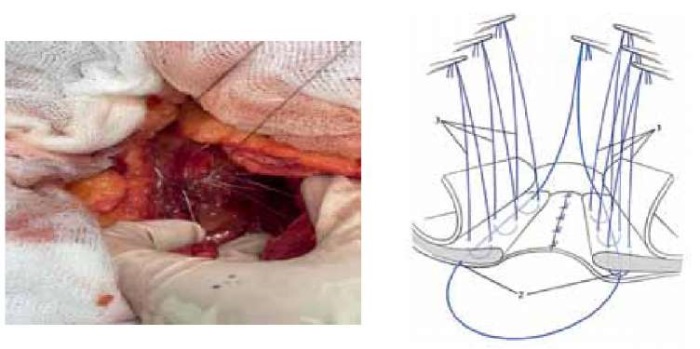
Рисунок 2. Анатомический эксперимент и схема.
Проведение нитей П-образных швов с захватом каркасной нити.
Figure 2. Anatomical experiment and diagram.
Carrying out threads of U-shaped seams with the capture of the frame thread.
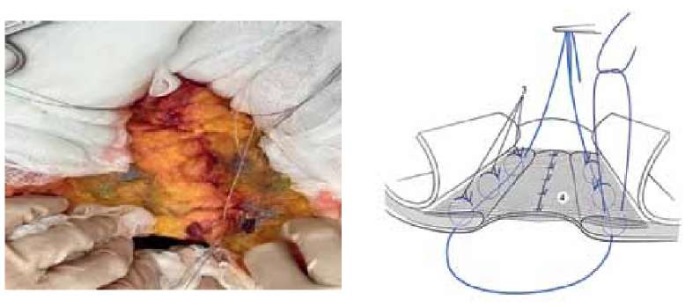
Рисунок 3. Анатомический эксперимент и схема.
Фиксация сетчатого эндопротеза П-образными швами.
Figure 3. Anatomical experiment and diagram.
Fixation of the mesh endoprosthesis with U-shaped sutures.
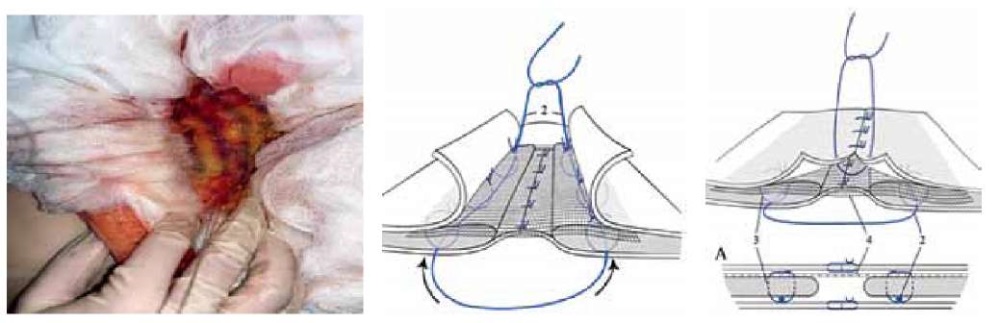
Рисунок 4. Анатомический эксперимент и схема.
Подтягивание каркасной нити и её фиксация. Окончательный вид операции.
А: поперечный срез передней брюшной стенки.
Figure 4. Anatomical experiment and diagram.
Tightening of the frame thread and its fixation. The final type of operation.
A: cross section of the anterior abdominal wall.
Итоговый вид создаваемой конструкции представлен на рисунке 4. Каркасная нить, проведённая через П-образные швы, фиксирующие сетчатый эндопротез, не даёт прорезываться им и распределяет внутрибрюшное давление на всю линию данных швов. Этим достигается повышенная упругость и прочность пластики по оригинальному способу.
На завершающем этапе анатомического эксперимента нами исследованы предел прочности и модуль упругости рубцово-измененных структур срединных отделов передней брюшной стенки, укреплённых по разработанной нами технологии на стенде ИСС-500 в сравнении с нативными и рубцово-измененными препаратами (табл. 1).
Таблица / Table 1
Сравнительная оценка биомеханических параметров
различных видов фасциальных структур передней брюшной стенки
Comparative evaluation of biomechanical parameters
of various types of fascial structures of the anterior abdominal wall
Вид ткани Type of tissue | Биомеханический параметр Biomechanical parameter | |
Предел прочности, кгс/см² Tensile strength, kgf/cm² | Модуль упругости, кгс/см² Modulus of elasticity, kgf/cm² | |
Нативная фасция Native fascia | 3,04±0,35 | 5,83±0,61 |
Рубцовая фасция* Scar fascia* | 1,31±0,12 | 2,01±0,32 |
Фасция с каркасной нитью Fascia with a skeleton thread | 6,86±0,40 | 8,21±0,54 |
Примечание: * — изменённая задняя стенка фасциального футляра
прямой мышцы живота грыженосителей (МI, RII, WIV),
р < 0,05 при сравнении исследуемых групп.
Note: * — modified posterior wall of the fascial sheath
of the rectus abdominis of herniators (МI, RII, WIV),
p < 0.05 when comparing the studied groups.
По итогам сравнительного анализа результатов эксперимента выявлено повышение биомеханических параметров препаратов, укреплённых каркасной нитью. Предел прочности превысил аналогичный показатель рубцово-измененной фасции на 59,4%, а нативной фасции — на 22,6%. Модуль упругости препаратов, укреплённых по оригинальной методике, был выше, чем у рубцово-измененной и нативной фасции соответственно на 40,2% и 14,1%.
По оригинальной методике в 2018–2022 гг. в центре хирургии Ростовской областной клинической больницы были прооперированы 63 пациента со срединными послеоперационными вентральными грыжами. Средний возраст больных составил 63 года (P25 51; P75 73), 18 (28,6%) мужчин и 45 (71,4%) женщин, 19 человек (30,2%) нормостенического и 44 (69,8%) — гиперстенического типа телосложения.
Средняя продолжительность заболевания составила в среднем 22,6 месяца (P25 1,8; P75 44,3), что представлено в таблице 2.
Таблица / Table 2
Распределение больных по длительности грыженосительства
Distribution of patients by duration of herniation
Грыженосительство (сроки) Herniation (terms) | Абс. Abs. | % |
До 6 месяцев Up to 6 months | 2 | 3,2 |
От 6 месяцев до 1 года From 6 months to 1 year | 17 | 27,0 |
От 1 года до 3 лет From 1 year to 3 years | 26 | 41,3 |
Свыше 3 лет Over 3 years | 18 | 28,6 |
Первый раз грыжа рецидивировала у 34 человек (54,0%), повторные рецидивы наблюдались у 29 пациентов (46,0%). В среднем число рецидивов грыж у всех пациентов составило 1,31 (95% ДИс 1,10–1,52). В 14 случаях (22,2%) больные прооперированы по экстренным показаниям в связи с явлениями острой кишечной непроходимости, в плановом порядке пролечены 49 человек (77,8%).
В соответствии с классификацией Европейского общества герниологов (EHS) у 34 пациентов (54,0%) грыжа определялась как WII с размером грыжевых ворот в среднем 8,75 см (P25 7,30; P75 10,13), у 29 человек (46,0%) встречались грыжи WIII со средним размером 10,30 см (P25 8,65; P75 11,40). Среди 63 прооперированных пациентов, у 45 (71,4%) имелась одиночная грыжа, у 18 из них (28,6%) определялись многочисленные грыжевые дефекты.
Средняя длительность оперативного лечения составила 119 минут (P25 114; P75 127), при этом основной этап операции длился 20 минут (P25 18; P75 22).
В послеоперационном периоде у 5 пациентов (7,9%) на протяжении первых суток имела место лихорадка, у такого же количества больных в течение 5–6 дней отмечался парез кишечника, в 2 случаях (3,2%) на протяжении 2–3 дней регистрировалась олигоурия. Большинство пациентов (30 больных (47,6%)) в послеоперационном периоде отмечали умеренную степень выраженности болевого синдрома. 23 пациента (36,5%) жаловались на выраженную боль, и 9 больных (14,3%) — на слабую. У одного пациента в течении 8 суток отмечалась нестерпимая боль в области послеоперационной раны, купированная введением наркотических анальгетиков. В зоне оперативного доступа у 9 пациентов (14,3%) отмечался инфильтрат мягких тканей в течение 4–12 суток. Послеоперационные раны у всех больных зажили первичным натяжением. Швы были сняты, как правило, спустя 14 суток после оперативного лечения (P25 13; P75 16).
В показателях лабораторных исследований в раннем послеоперационном периоде не выявлены статистически значимые отличия от нормальных значений по большинству показателей гемограммы, гемостазиограммы и биохимических показателях крови. Необходимо отметить, что наблюдалось снижение количества эритроцитов (4,23±0,59×10⁹/л (p<0,001)), уровня гемоглобина (125,84±11,86 г/л (p=0,040)), а также увеличение количества лейкоцитов (8,12±4,15×10¹²/л (p<0,001)) и СОЭ (25,67±14,18 мм/ч (p <0,001)).
Все пациенты выписаны в удовлетворительном состоянии, летальных исходов не отмечалось. Продолжительность стационарного лечения пациентов составила в среднем 15 суток (P25 12; P75 17). В отдалённом периоде рецидивов грыж у наблюдаемых пациентов не было. Вместе с тем, у 2 больных в течении 1–2 лет после оперативного лечения отмечались лигатурные свищи.
Обсуждение
Основываясь на низкой способности рубцово-измененных фасциально-мышечных структур у пациентов со срединными послеоперационными вентральными грыжами противостоять повышенному градиенту внутрибрюшного давления после герниопластики, мы разработали, запатентовали и апробировали технологию оперативного лечения данной категории больных. Основой её является профилактика прорезывания швов, фиксирующих эндопротез, и укрепление тканей передней брюшной стенки в зоне грыжевых ворот каркасной нитью.
В ходе сравнительного анализа результатов анатомического эксперимента установлено повышение биомеханических показателей срединных структур, укреплённых по оригинальной методике каркасной нитью: предела прочности фасции — на 59,4%, а модуля упругости — на 40,2% по сравнению с рубцово-измененной фасцией у грыженосителей. Полученные результаты позволяют предположить уверенную профилактику рецидивов грыжеобразования при применении данной методики.
Данное предположение подтверждено после внедрения методики в клиническую практику. При наблюдений в отдаленном периоде в течение 1–5 лет у всех 63 наблюдаемых пациентов отсутствует рецидив грыженосительства. Также отсутствовали значимые осложнения течения раннего послеоперационного периода, связанные с примененным способом пластики. Следует отметить материальную и финансовую доступность способа, отсутствие сложных технических манипуляций, увеличивающих продолжительность герниопластики.
Таким образом, оригинальная методика является эффективным, доступным и безопасным способом оперативного лечения пациентов со срединными послеоперационными вентральными грыжами.
Выводы
Выбор оптимальной методики герниопластики является главенствующим условием достижения удовлетворительных результатов при лечении любых вентральных грыж. Особенностью срединных послеоперационных вентральных грыж является сниженная способность рубцово-измененных тканей в зоне грыжевых ворот сопротивляться внутрибрюшному давлению, повышающемуся в послеоперационном периоде. При пластике с укреплением швов, фиксирующих эндопротез, каркасной нитью по оригинальной методике, повышаются биомеханические показатели рубцово-измененых фасциально-апоневротических структур.
Эффективность в профилактике рецидивов грыжеобразования, доступность и простота исполнения предложенного способа хирургического лечения послеоперационных и рецидивных вентральных грыж позволяет рекомендовать его к широкому клиническому применению.
1. Григорян Р.А. Абдоминальная хирургия: В 2 т. Том 1. М.: ООО «Медицинское информационное агентство», 2006.
2. Иванова Т. Е., Жидков С. А. Послеоперационные грыжи живота: метод. Рекомендации. Минск: БГМУ; 2007.
3. Патент №2271740 Российская Федерация, A61B 5/103 (2006.01), Способ исследования фасций и клетчаточных пространств: № 2004115696: заявл. 25.05.2004: опубл. 20.03.2006 / Татьянченко В.К., Саркисян В.А., Андреев Е.В., Чубарян К.А.; заявитель Татьянченко В.К., Саркисян В.А., Андреев Е.В., Чубарян К.А. – 4 с. – Текст: непосредственный.
4. Патент №2685682 Российская Федерация, A61B 17/00 (2019.02), Способ хирургического лечения послеоперационных и рецидивных вентральных грыж: № 2018116827: заявл. 04.05.2018: опубл. 22.04.2019 / Коробка В.Л., Коробка А.В., Даблиз Р.О., Данильчук О.Я., Шаповалов А.М.; заявитель Коробка В.Л. – 14 с.: ил. – Текст : непосредственный.
Список литературы
1. Попов А.Ю., Петровский А.Н., Губиш А.В., Вагин И.В., Шевченко М.С., и др. Результаты восстановления передней брюшной стенки при послеоперационных вентральных грыжах с использованием сетчатых имплантатов. Хирургия. Журнал им. Н.И. Пирогова. 2020;(3):35-42.
2. Parker SG, Wood CPJ, Butterworth JW, Boulton RW, Plumb AAO, et al. A systematic methodological review of reported perioperative variables, postoperative outcomes and hernia recurrence from randomised controlled trials of elective ventral hernia repair: clear definitions and standardised datasets are needed. Hernia. 2018;22(2):215-226. https://doi.org/10.1007/s10029-017-1718-4
3. Ермолов А.С., Благовестнов Д.А., Алексеев А.К., Упырев А.В., Ярцев П.А., и др. Хирургическое лечение пациентов с большими и гигантскими послеоперационными вентральными грыжами. Хирургия. Журнал им. Н.И. Пирогова. 2019;(9):38-43.
4. Федосеев А.В., Рыбачков В.В., Трушин С.Н., Лебедев С.Н., Инютин А.С. Превентивное эндопротезирование брюшной стенки в группах риска развития послеоперационных вентральных грыж. Хирургия. Журнал им. Н.И. Пирогова. 2019;(1):32-36.
5. Bueno-Lledó J, Torregrosa-Gallud A, Sala-Hernandez A, Carbonell-Tatay F, Pastor PG, et al. Predictors of mesh infection and explantation after abdominal wall hernia repair. Am J Surg. 2017;213(1):50-57. https://doi.org/10.1016/j.amjsurg.2016.03.007
6. Chandra R, Jacobson RA, Poirier J, Millikan K, Robinson E, Siparsky N. Successful non-operative management of intraabdominal hypertension and abdominal compartment syndrome after complex ventral hernia repair: a case series. Am J Surg. 2018;216(4):819-823. https://doi.org/10.1016/j.amjsurg.2018.07.063
7. Pawlak M, Tulloh B, de Beaux A. Current trends in hernia surgery in NHS England. Ann R Coll Surg Engl. 2020;102(1):25-27. https://doi.org/10.1308/rcsann.2019.0118
8. Dietz UA, Menzel S, Lock J, Wiegering A. The Treatment of Incisional Hernia. Dtsch Arztebl Int. 2018;115(3):31-37. Erratum in: Dtsch Arztebl Int. 2018;115(6):98. https://doi.org/10.3238/arztebl.2018.0031
9. Коробка В.Л., Даблиз Р.О., Шаповалов А.М., Татьянченко В.К., Толстопятов С.В. Экспериментальное обоснование оригинальной методики герниопластики при рецидивном течении вентральных грыж срединной локализации. Московский хирургический журнал. 2022;(4):49-60.
Об авторах
В. Л. КоробкаРоссия
Коробка Вячеслав Леонидович, д.м.н. доцент, заведующий кафедрой реконструктивной, сердечно-сосудистой, торакальной, челюстно-лицевой хирургии и трансплантологии
Ростов-на-Дону
В. К. Татьянченко
Россия
Татьянченко Владимир Константинович, д.м.н., профессор, заведующий кафедрой оперативной хирургии и клинической анатомии и патологической анатомии ФПК и ППС
Ростов-на-Дону
Р. О. Даблиз
Россия
Даблиз Рашад Омарович, хирург
Ростов-на-Дону
С. В. Толстопятов
Толстопятов Сергей Владимирович, к.м.н., хирург, ассистент кафедры реконструктивной, сердечно-сосудистой, торакальной, челюстно-лицевой хирургии и трансплантологии; хирург
Ростов-на-Дону
М. В. Гончар
Россия
Гончар Михаил Викторович, ассистент кафедры реконструктивной, сердечно-сосудистой, торакальной, челюстно-лицевой хирургии и трансплантологии; хирург
Ростов-на-Дону
И. С. Клец
Клец Иван Сергеевич, ассистент кафедры реконструктивной, сердечно-сосудистой, торакальной, челюстно-лицевой хирургии и трансплантологии; хирург
Ростов-на-Дону
Рецензия
Для цитирования:
Коробка В.Л., Татьянченко В.К., Даблиз Р.О., Толстопятов С.В., Гончар М.В., Клец И.С. Клинико-экспериментальные параллели в обосновании способа герниопластики срединных послеоперационных вентральных грыж. Медицинский вестник Юга России. 2024;15(1):108-114. https://doi.org/10.21886/2219-8075-2024-15-1-108-114
For citation:
Korobka V.L., Tatyanchenko V.K., Dabliz R.O., Tolstopyatov S.V., Gonchar M.V., Kletz I.S. Clinical and experimental parallels in the substantiation of the method of hernioplasty of postoperative ventral hernias of median localization. Medical Herald of the South of Russia. 2024;15(1):108-114. (In Russ.) https://doi.org/10.21886/2219-8075-2024-15-1-108-114
JATS XML







































