Перейти к:
Оценка четырехлетнего ведения листа ожидания трансплантации печени Ростовской области: перспективы снижения смертности в листе
https://doi.org/10.21886/2219-8075-2019-10-3-32-39
Аннотация
Цель: анализ различных вариантов клинического исхода в листе ожидания трансплантации печени.
Материалы и методы: работа проведена на базе Центра хирургии и координации донорства Ростовской областной клинической больницы с использованием клинико-лабораторных и инструментальных данных 198 пациентов из ЛО ТП. По полу больные распределились равным образом – по 99 человек. Возраст мужчин колебался от 21 до 70 лет (47,8±10,4 лет), женщин – от 18 до 66 лет (49,2±10,9 лет). На момент анализа данных ЛО средний период наблюдения за больными составил 14,8±11,2 месяцев. Все пациенты обследованы согласно перечню, необходимому для включения в ЛО.
Результаты: 198 пациентов удалось систематизировать согласно 4 группам исхода в ЛО ТП. Первую группу (группу делистинга) составили 19 пациентов (9,6%), клинико-лабораторные показатели которых позволили вывести их из ЛО. Вторая группа была представлена 67 пациентами (33,8%), находящимися в ЛО, при наличии у них положительной клинической динамики на фоне проводимого лечения. В третью группу вошли 39 пациентов (19,7%), у которых была выполнена трансплантация печени. Четвертая группа была представлена больными, у которых на фоне проводимого лечения отмечалась отрицательная динамика – 73 (36,9%) человека, в их числе и пациенты с летальным исходом. За 4 года ведения листа ожидания трансплантации печени, из 198 пациентов, внесенных в лист ожидания, умерли 61 (30,81%). Подавляющее большинство (40 пациентов) погибло от кровотечения из ВРВ и ОППН, 17 человек от печеночной комы и СПБ. В каждой группе представлены особенности распределения пациентов согласно шкале MELD-Na, степени выраженности портальной гипертензии и печеночной энцефалопатии.
Выводы: неотъемлемым условием успешной работы трансплантационного центра являются следующие факторы: планомерная работа с территориями с целью расширения донорской базы, определение новых критериев приоритета пациентов в листе ожидания трансплантации с целью снижения показателя смертности в листе, детальное обследование больного до внесения в лист, формирование базы наблюдения, систематического мониторинга пациентов в пред- и послеоперационном периоде, на этапе реабилитации, а так же на отдаленных сроках с целью выработки эффективного алгоритма наблюдения за реципиентом солидного органа.
Для цитирования:
Коробка В.Л., Пак Е.С., Шаповалов А.М., Кострыкин М.Ю., Ткачев А.В. Оценка четырехлетнего ведения листа ожидания трансплантации печени Ростовской области: перспективы снижения смертности в листе. Медицинский вестник Юга России. 2019;10(3):32-39. https://doi.org/10.21886/2219-8075-2019-10-3-32-39
For citation:
Korobka V.L., Pak E.S., Shapovalov A.M., Kostrykin M.U., Tkachev A.V. Analysis of four-year management of the waiting list for liver transplantation in Rostov region: prospects for reducing mortality of candidates listed for liver transplantation. Medical Herald of the South of Russia. 2019;10(3):32-39. (In Russ.) https://doi.org/10.21886/2219-8075-2019-10-3-32-39
Введение
На сегодняшний день эффективным методом лечения терминального цирроза печени, острой печеночной недостаточности и гепа- тоцеллюлярной карциномы (в рамках ограничительных критериев) общепризнана трансплантация печени (ТП) [1], положительные результаты которой подтверждаются высоким показателем 5-летней выживаемости, достигающей 80 — 90 % [2].
Неотъемлемой частью трансплантации является отбор больных с включением их в лист ожидания (ЛО), в котором осуществляется динамический клинико-лабораторный контроль, непрерывный мониторинг соматического статуса, патогенетическая и симптоматическая терапия, хирургическое лечение при развитии угрожающих жизни больного осложнений [3]. Внесение пациентов в ЛО обосновывается такими критериями, как неотложность и перспективность ТП, а саму трансплантацию следует рассматривать в качестве метода лечения, позволяющего не только продлить жизнь больному, но и значительно улучшить ее качество [4].
Неотложность выполнения ТП определяется моделью конечной стадии заболевания печени (MELD — Model for End Stage Liver Disease), которая включает в себя оценку таких лабораторных показателей как креатинин, билирубин, международное нормализованное отношение (МНО) [5]. Однако эти показатели нужно оценивать по совокупности данных, в том числе данных о наличии у пациентов явной печеночной энцефалопатии (ПЭ), рецидивирующего варикозного кровотечения, резистентного асцита и гепатоцеллюлярной карциномы (ГЦК) [6]. Именно многофакторная оценка позволяет определять приоритетность выполнения трансплантации печени (ТП) у каждого больного из ЛО [7].
Сдерживающим фактором развития трансплантации во всем мире остается дефицит донорских органов [8]. По этой причине время ожидания в листе нередко увеличивается, растет смертность больных, а те пациенты, которые остаются в живых, зачастую подходят к трансплантации в критическом состоянии, что ухудшает её результаты как в периоперационном периоде, так в отдаленные сроки [9].
Из-за отсутствия возможности глобально изменить ситуацию с обеспечением донорскими органами [10] для совершенствования трансплантационной службы в регионе, очевидным является оптимизация ведения ЛО, с определением более четких критериев включения в него больных, а также планомерная работа с территориями для своевременного выявления потенциальных доноров.
Цель исследования — анализ различных вариантов клинического исхода в ЛО ТП (делистинг, смерть, ортотопическая трансплантация печени, улучшение и ухудшение при продолжении наблюдения в листе).
Материалы и методы
Работа проведена на базе Центра хирургии и координации донорства Ростовской областной клинической больницы с использованием клинико-лабораторных и инструментальных данных 198 пациентов из ЛО ТП. По полу больные распределились равным образом — по 99 человек. Возраст мужчин — от 21 до 70 лет (47,8±10,4 лет), возраст женщин — от 18 до 66 лет (49,2±10,9 лет). На момент анализа данных ЛО средний период наблюдения за больными составил 14,8±11,2 месяцев.
Все пациенты обследованы согласно перечню, необходимому для включения в ЛО. Основными критериями включения больных явились следующие:
- наличие острого или хронического заболевания печени, приведшего к декомпенсации соматического состояния пациента;
- наличие острого или хронического заболевания печени, его осложнений, требующих посиндромной и этиопатогенетической терапии;
- наличие осложнений основного заболевания, требующих этапного хирургического лечения и трансплантации печени;
- добровольное согласие пациента на внесение в лист ожидания.
Критериями исключения были следующие:
- выраженная сердечно-легочная патология;
- продолжение приема алкоголя на момент исследования;
- наличие очагов хронической инфекции;
- гепатоцеллюлярная карцинома (за пределами миланских критериев);
- распространенный тромбоз воротной вены и ее магистральных притоков;
- психические заболевания;
- наличие онкологического заболевания в анамнезе (за исключением гепатоцеллюлярной карциномы в пределах миланских критериев);
- отказ пациента от внесения в ЛО.
Причиной включения 83 (41,9 %) пациентов в ЛО стал цирроз печени в исходе вирусных гепатитов (68 — гепатит С (HCV), 15 — гепатит В (HBV)). На долю аутоиммунных заболеваний, приведших к циррозу печени, пришлось 46 наблюдений (23,2 %), алкогольный цирроз имели 40 человек (20,2 %). У 29 человек (14,7 %) цирроз возник на фоне врожденных заболеваний (болезнь Вильсона-Коновалова), вторичного склерозирующего холангита и неустановленных причин. Следует отметить, что из числа больных с вирусной этиологией цирроза печени патогенетическая терапия проводилась 67 (80,7 %) пациентам, из них в 52 случаях получен устойчивый вирусологический ответ.
Отягчающими клиническое течение основного заболевания факторами у 66 человек была острая печеночная недостаточность на фоне хронической, у 26 — тромбоз воротной вены, наличие ПЭ 3 и 4 степени — в 64 случаях, наличие резистентного асцита — в 67 случаях. Гепаторенальный синдром наблюдали у 47 % больных. На момент постановки в лист ожидания 132 пациента предъявляли жалобы на варикозные кровотечения (от 1 до 14 эпизодов). Помимо клинических методов оценки тяжести состояния больных были использованы оценочные шкалы MELD-Na и индекс коморбидности Charlson, позволяющий оценивать вероятность наступления смерти в течение ближайших 10 лет.
В соответствии с диагностическим протоколом у всех больных проводили общие клинические и биохимические исследования крови, мочи, выполняли иммунологическое типирование, метод полимеразной цепной реакции (ПЦР) и иммуноферментный анализ (ИФА) диагностику HBV, HCV, цитомегаловируса (CMV), PGV и вируса Эпштейна-Барр (EBV), оценивали иммунологический статус. Обязательно осуществляли контроль гемостаза и онкоскриниг. У пациентов с генетически обусловленным циррозом печени проводили специфические тесты. При необходимости выполняли анализ асцитической и плевральной жидкостей.
Из инструментальных методов диагностики применяли эзофагогастродуоденофиброскопию (ЭФГДС), колоноскопию (ФКС), эндоскопическую ультрасонографию (ЭУС), ультразвуковое исследование (УЗИ), спиральную компьютерную томографию (СКТ) и магнитно-резонансную томографию (МРТ) органов брюшной полости с болюсным контрастированием. Непрямую эластометрию печени осуществляли во всех случаях, а биопсию — при наличии показаний.
Все пациенты из ЛО по клиническому исходу были разделены на четыре группы. Первую группу (группу делистинга) составили 19 пациентов (9,6 %), клинико-лабораторные показатели которых позволили вывести их из ЛО. Вторая группа была представлена 67 пациентами (33,8 %), находящимися в ЛО, при наличии у них положительной клинической динамики на фоне проводимого лечения. В третью группу вошли 39 пациентов (19,7 %), у которых была выполнена ТП. Четвертая группа была представлена больными, у которых на фоне проводимого лечения отмечалась отрицательная динамика — 73 (36,9 %) человека, в их числе и пациенты с летальным исходом.
Результаты
Анализ каждой клинической группы дал следующие результаты.
В группе делистинга причиной цирроза печени у 47,37 % пациентов были вирусные гепатиты, у 26,32 % — хроническая алкогольная интоксикация, в 15,79 % случаев — криптогенный цирроз и аутоиммунные заболевания у 10,53 % человек.
Согласно шкале MELD-Na, в группе «делистинга» 15,8 % пациентов имели средний балл 15,9, а 84,2 % — 21,2.
Средний показатель индекса коморбидности Charlson в группе составил 8,1±2,6 баллов. Распределение больных выглядело следующим образом:
до 10 баллов — 68,4% больных (медиана 7),
от 10 до 12 баллов— 26,3 % (медиана 11),
13 баллов имел один пациент (5,3 %).
Явная ПЭ наблюдалась у 84,2 % пациентов, из них у одного с печеночной комой, тогда как в 15,8 % случаев признаки энцефалопатии отсутствовали. 84,2 % человек группы имели асцит 1 ст., 15,8 % — асцит 2 ст.
Улучшение самочувствия в группе было отмечено у 31,6 % пациентов: двое с криптогенным циррозом и четверо с циррозом печени в исходе вирусного гепатита C. Положительный результат у них был достигнут благодаря примененной оригинальной методике азиго-портального разобщения (патент РФ 2412657), так как эти больные имели в анамнезе от 1 до 8 эпизодов кровотечения из варикозно расширенных вен пищевода (ВРВП).
Стабильный положительный результат в случае криптогенного цирроза отмечался на фоне комбинации методов экстракорпоральной гемокоррекции (плазмасорбция и продленная вено-венозная гемодиафильтрация). В двух наблюдениях цирроза в исходе хронической HCV инфекции проведенный курс противовирусной терапии и однократное лигирование вен пищевода, а также противовирусная терапия пегилированным интерфероном имели успех. Устойчивый вирусологический ответ у пациентов с HCV- инфекцией получен во всех случаях лечения препаратами прямого действия, которое проводили в течение не менее 6 месяцев
У двоих пациентов с аутоиммунной этиологией цирроза стойкая ремиссия достигнута на фоне терапии Азатио- прином с преднизолоном. Медикаментозная компенсация асцита достигнута у всех больных группы. Среди больных с циррозом печени в исходе хронической алкогольной интоксикации стойкая положительная динамика имела место в 100 % наблюдений на фоне симптоматической терапии и устранения этиологического фактора.
Из числа больных группы «улучшения» в ЛО (67) у 33 (49,25 %) имел место ЦП в исходе хронических вирусных гепатитов, у 17 (25,37 %) в исходе аутоиммунных заболеваний. Систематический прием алкоголя явился причиной ЦП в 11 (16,42 %) случаях, криптогенный цирроз наблюдался у 3 (4,48 %) пациентов, а также по одному наблюдению в данной группе имели болезнь Вильсона-Коновалова, кавернозные гемангиомы печени и эхинококкоз (4,48 %).
Оценка шкалы MELD-Na в группе «улучшения» показала следующее:
до 20 баллов имели 28,4 % пациентов (медиана 16,1), от 20 до 25 балов — 58,2% (медиана 21,8), более 25 баллов имели 13,4 % больных (медиана 26,9). Диапазон индекса коморбидности Charlson колебался от 4 до 14 баллов и, в среднем, составил 9,4±2,4. До 10 баллов имели 52,2 % больных (медиана 6,5), от 10 до 12 баллов — 37,3% (медиана 11), более 12 баллов имели 16,4 % пациентов (медиана 13,5).
Из 67 пациентов группы у подавляющего большинства (94 %) наблюдалась явная ПЭ, из них в трех наблюдениях с печеночной комой. Асцит имели все пациенты, однако его резистентная форма отмечалась у 46,3 % больных, из которых у пяти человек неоднократно проводился лапароцентез. 58,2 % больных в анамнезе имели от 1 до 5 кровотечений из ВРВ пищевода.
Этиологические факторы ЦП у пациентов группы ОТП (39) имели следующее распределение:
- 14 (35,90%) — ЦП в исходе вирусных гепатитов (7- HBV, 7-HCV) с трансформацией в ГЦК в 3х случаях,
- 6 (15,38 %) — ЦП в исходе систематического приема алкоголя,
- 2 (5,13 %) - криптогенный цирроз,
- 11 (28,21 %) - ЦП на фоне аутоиммуных заболеваний,
- 3 (7,69%) - ЦП на фоне врожденных заболеваний,
- 2 (5,13 %) - ЦП вследствие склерозирующего холангита.
Выполнена 1 ретрансплантация печени по поводу развившегося синдрома Бадда-Киари.
Согласно классификации MELD-Na, распределение больных в группе пациентов, перенесших трансплантацию печени, выглядело следующим образом:
до 20 баллов имели 15,4 % пациентов (медиана 17,9), от 20 до 25 баллов — 71,2 % человек (медиана 21,6), более 25 баллов — 12,8 % больных (медиана 27). Диапазон индекса коморбидности Charlson колебался от 4 до 13 баллов и составил 8,5±2,3. До 10 баллов имели 61,5 % больных (медиана 6,5), от 10 до 12 баллов — 28,2 % (медиана 10,5), более 12 баллов имели 10,3 % пациентов (медиана 12,5).
Явная ПЭ из 39 пациентов данной группы наблюдалась у 92,3 % в 2-х случаях с печеночной комой. Резистентную форму асцита имели 66,7 % больных, из которых у двоих при 3 степени проводили лапароцентез.
Кровотечения из ВРВ пищевода в количестве от 1 до 14 были у 21 пациента группы ОТП.
Из 39 пациентов, перенесших ортотопическую трансплантацию печени, 32 пациента в настоящее время находятся в удовлетворительном состоянии, 28 их них вернулись на прежние места работы. Одному пациенту была выполнена ретрансплантация печени по причине развития дисфункции трансплантата на фоне формирования синдрома Бадда-Киари. Более подробная характеристика исходов пациентов после выполнения ОТП представлена в табл. 1.
Таблица 1 / Tablel 1
Клинические исходы 39 трансплантаций печени Ростовской области
Clinical results 39 liver transplantation in the Rostov region
Исход Result | n | % | Срок наблюдения (мес.) Observation period (months) |
|---|---|---|---|
Выздоровление / Convalescence | 32 | 82,05 | 18,00±12,65 |
Отторжение ТП / Rejection | 1 | 2,56 | 12 |
Смерть / Decease | 6 | 15,38 | 23,67±11,70 |
Генерализованный аспергиллез / Generalized Aspergillosis | 1 | 16,67 | 3,18 |
ОППН / Acute renal and hepatic failure | 2 | 33,33 | 6,11 |
ПНТ / Primarily non-functioning graft | 1 | 16,67 | 0,23 |
Рак легкого с mts / Metastatic lung cancer | 1 | 16,67 | 24,4 |
Тромбоз печеночных вен / Hepatic vein thrombosis | 1 | 16,67 | 0,07 |
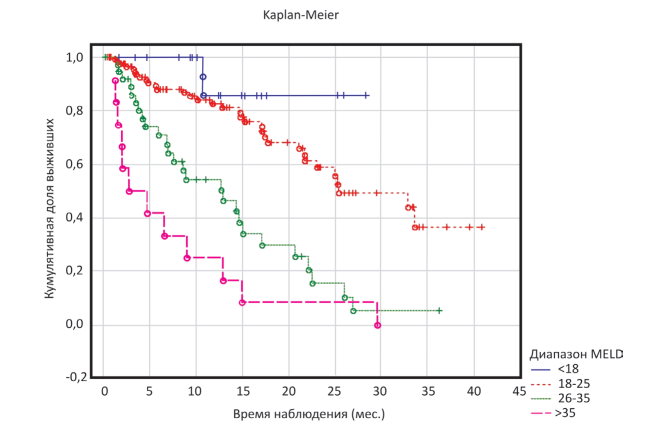
Рисунок 1. Построение непараметрической оценки функции дожития (оценка Каплана-Мейера) 198 пациентов из ЛО ТП согласно группе и значению MELD- Na.
Figure 1. Construction of non-parametric assessment of survival function (Kaplan-Meier assessment) 198 patients from LO TP according to the group and value of MELD-Na.
Из числа больных группы «ухудшения» самочувствия в Л О (12) у 6 пациентов (50,0 %) ЦП наступил в исходе хронических вирусных гепатитов, у 2 (16,67 %) причиной ЦП явилась хроническая алкогольная интоксикация, аутоиммунный ЦП — в четырех наблюдениях (33,33 %).
Пациенты группы ухудшения согласно классификации MELD, распределялись следующим образом: 7 человек — от 18 до 25 баллов, 5 человек — от 26 до 35 баллов.
Согласно индексу коморбидности Charlson, у 5 пациентов (41,66 %) — от 4 до 8 баллов, у 5 (41,66 %) — от 9 до 12, у 2 (16,67 %) — от 13 до 19 баллов. Из 12 пациентов группы ухудшения у всех наблюдалась явная ПЭ (из них один с печеночной комой). У 2 (16,67 %) человек наблюдался асцит 1 ст., у 2 (16,67 %) — асцит 2 ст., у 8 (66,6 7%) — асцит 3 ст., потребовавший проведение лапароцентеза у 4 больных. У 9 больных в анамнезе было от 1 до 3 кровотечений.
Для наглядности, из четырёх группы отдельно проанализированы данные умерших больных (61 случай).
Из числа умерших ЦП в исходе вирусных гепатитов наблюдался у 21 (34,43 %), алкогольный цирроз — в 16 (26,32 %) случаях, криптогенный цирроз — у 8 (13,11 %) пациентов, аутоиммунный генез заболевания — у 12 (19,67 %) больных, генетически детерменированный ЦП — 3 (4,92 %) случая и фульминантная ПН — 1 (1,64 %) наблюдение. Среди умерших, согласно классификации MELD-Na, 2 пациента имели от 16 до 18 баллов, 26 пациентов — от 19 до 25, 21 — от 26 до 35, 12 пациентов — с показателем >35. Диапазон индекса коморбидности у 13 пациентов (21,32 %) — от 4 до 8 баллов, у 39 пациентов (63,93 %) — от 9 до 12, у 9 пациентов (14,76 %) — от 13 до 19. У 12 (19,67 %) человек наблюдался асцит 1 ст., у 13 (21,31 %) — асцит 2 ст., у 36 (59,02 %) — асцит 3 ст., потребовавший проведения лапароцентеза у 30 больных. У 51 больного данной группы в анамнезе было от 1 до 5 кровотечений. У 3 (4,92 %) пациентов отсутствовала явная ПЭ, у 58 (95,09 %) наблюдалась явная ПЭ (из них семеро — с печеночной комой). Наиболее распространенной сопутствующей патологией у больных в ЛО ТП был хронический панкреатит (37 человек (18,69 %)). Остальная сопутствующая патология распределилась следующим образом: гипертоническая болезнь — у 26 человек (13,13 %), миокардиодистрофия — у 19 больных (9,60 %), сахарный диабет — в 18 случаях (9,09 %), ишемическая болезнь сердца — у 17 (8,59 %) и язвенная болезнь — у 11 человек (5,56 %).
Двумя практически равнозначными по частоте причинами смертности в ЛОТП явились кровотечение из ВРВ и ОППН. Более конкретное распределение по причине смерти указано в табл. 2.
Таблица / Table 2
Структура смертности в листе ожидания трансплантации печени
The structure of mortality in the liver transplantation waiting list
Причина смерти Cause of death | n | % |
|---|---|---|
Синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) / Disseminated intravascular coagulation syndrome | 1 | 1,64 |
Инфаркт миокарда / Myocardial infarction | 1 | 1,64 |
Кровотечение из ВРВ / Bleedingfrom esophageal varicose veins | 21 | 34,43 |
Острая печеночно-очечная недостаточность (ОППН) / Acute renal and hepatic failure | 19 | 31,15 |
ОППН, ДВС синдром / Acute renal and hepatic failure, disseminated intravascular coagulation syndrome | 2 | 3,28 |
Печеночная кома / | 9 | 14,75 |
Hepatic coma | ||
Спонтанный бактериальный перитонит, сепсис / Spontaneous bacterial peritonitis, sepsis | 8 | 13,11 |
Обсуждение
Тяжесть состояния пациента и, как следствие, статус неотложности трансплантации определяет шкала MELD-Na. Но для достижения большей объективности отбора, в особенности при наличии явной печеночной энцефалопатии, резистентного асцита с риском спонтанного бактериального перитонита, рецидивирующих кровотечений из ВРВ, каждый критерий должен оцениваться в отдельности. За четыре года ведения листа ожидания трансплантации печени, из 198 пациентов, внесенных в ЛО, умер 61 пациент (30,81 %). Подавляющее большинство (40 пациентов) умерло от кровотечения из ВРВ и ОППН, 17 человек от печеночной комы и СПБ. Конечно, нельзя исключать из внимания территориальные особенности Ростовской области с большими расстояниями от удаленных районов до административного центра (в отдельных случаях до 400 км). Следовательно, для снижения смертности в листе необходима своевременная профилактика кровотечений из ВРВ в виде эндоскопического лигирования, азиго-портального разобщения, выполнения трансюгулярного портосистемного шунтирования, учитывая возможности региона. Терапевтическая концепция требует рассмотрения актуальности назначения/отмены неселективных бета-блокаторов, своевременной индивидуализированной оценки печеночной энцефалопатии, комбинированной диуретической терапии и путей их коррекции, а также своевременного проведения курса противовирусной терапии, направленных на уменьшение смертности в листе, улучшения качества жизни пациента. Также кровотечения из ВРВ, степень асцита и печеночной энцефалопатии должны рассматриваться в дополнение к оценке MELD-Na для достижения прозрачности и справедливости при отборе возможных реципиентов печени. Пациенты с высоким прогностическим коэффициентом десятилетней выживаемости по Charlson нередко умирают гораздо быстрее пациентов с низким коэффициентом. В связи с этим наблюдением учет коморбидного фона пациента, согласно индексу коморбидности Charlson, не актуален для пациентов с декомпенсированным циррозом печени. Несомненно, залогом долгосрочного ведения пациентов в листе ожидания трансплантации печени является не только посиндромная терапия, но также профилактика и лечение метаболических осложнений, сердечно-сосудистых заболеваний, и регулярный скрининг на злокачественные новообразования.
Заключение
Неотъемлемым условием снижения смертности в ЛО ТП и, как следствие, успешной работы трансплантационного центра являются следующие факторы:
- Планомерная работа с территориями с целью расширения донорской базы.
- Определение новых критериев приоритета пациентов в листе ожидания трансплантации с целью снижения показателя смертности в листе.
- Детальное обследование больного до внесения в лист, что позволяет своевременно выявить возможные риски и противопоказания к оперативному лечению, что является особенно важным в условиях дефицита донорских органов.
- Формирование базы наблюдения, систематического мониторинга пациентов в пред- и послеоперационном периоде, на этапе реабилитации, а также на отдаленных сроках с целью выработки эффективного алгоритма наблюдения за реципиентом солидного органа.
Возможным решением проблемы нехватки донорских органов представляется включение в донорский пул ранее непригодных доноров (пожилой возраст, увеличение времени холодовой ишемии, несовместимость по системе АВ0, стеатоз), совершенствование хирургической техники (сплит трансплантация, части печени живого добровольного донора).
Критерии отбора пациентов из ЛО ТП в момент появления донора расширены путем введения бальной системы критериев. В основу формирования системы отбора положен суммарный балл, получаемый путем суммирования промежуточных баллов, таких как: клинического, балла ответа на медикаментозную терапию, балла оценки хирургического и экстракорпорального лечения и балла лабораторного статуса пациента.
С целью тщательного отбора пациентов для внесения в ЛО ТП и непрерывного наблюдения за пациентами, находящимися в ЛО ТП, а так же реципиентами печени, в условиях больницы организован ежедневный прием врача-гепатолога, четко регламентирован график медицинского контроля при постановке в ЛО ТП и после выполнения ОТП.
Наконец, краеугольным камнем успешной работы трансплантологов является своевременность направления пациента в трансплантационный центр, что обеспечивает стратегию корректности отбора пациента и качество предтрансплантационной подготовки.
Список литературы
1. Хубутия М.Ш., Андрейцева О.И., Журавель С.В., Гуляев В.А. и др. Методика формирования листа ожидания трансплантации печени//Трансплантология. 2009. № 1. С. 13-19.
2. Ravaioli M, Grazi GL, Dazzi A, et al.: Survival benefit after liver transplantation: a single European center experience. Transplantation. 2009; 88(6): 826–34.
3. Adam R, Karam V, Delvart V, et al.: Evolution of indications and results of liver transplantation in Europe. A report from the European Liver Transplant Registry (ELTR). J Hepatol. 2012; 57(3): 675–88.
4. Kim WR, Biggins SW, Kremers WK, et al.: Hyponatremia and mortality among patients on the liver-transplant waiting list. N Engl J Med. 2008; 359(10): 1018–26.
5. Botta F., Giannini E., Romagnoli P. et al. MELD scoring system is useful for predicting prognosis in patients with liver cirrhosis and is correlated with residual liver function: A European study//Gut.2003. Vol. 52. P. 134-139.
6. Goldaracena N, Marquez M, Selzner N, et al.: Living vs. deceased donor liver transplantation provides comparable recovery of renal function in patients with hepatorenal syndrome: a matched case-control study. Am J Transplant. 2014; 14(12): 2788–95.
7. Cillo U, Burra P, Mazzaferro V, et al.: A Multistep, Consensus-Based Approach to Organ Allocation in Liver Transplantation: Toward a "Blended Principle Model". Am J Transplant. 2015; 15(10): 2552–61.
8. Toniutto P, Zanetto A, Ferrarese A, et al.: Current challenges and future directions for liver transplantation. Liver Int. 2016.
9. Koch DG, Tillman H, Durkalski V, et al.: Development of a Model to Predict Transplant-free Survival of Patients With Acute Liver Failure. Clin Gastroenterol Hepatol. 2016; 14(8): 1199–1206.e2.
10. Burra P, Freeman R: Trends in liver transplantation 2011. J Hepatol. 2012; 56(Suppl 1): S101–11.
Об авторах
В. Л. КоробкаРоссия
Коробка Вячеслав Леонидович - д.м.н., главный врач; доцент кафедры хирургических болезней ФПК и ППС
Ростов-на-Дону
Е. С. Пак
Россия
Пак Екатерина Сергеевна - врач-гастроэнтеролог; аспирант кафедры Пропедевтики внутренних болезней.
Ростов-на-Дону
А. М. Шаповалов
Россия
Шаповалов Александр Михайлович - к.м.н., врач-хирург.
Ростов-на-ДонуМ. Ю. Кострыкин
Россия
Кострыкин Михаил Юрьевич - к.м.н., врач-хирург.
Ростов-на-Дону
А. В. Ткачев
Россия
Ткачев Александр Васильевич, д.м.н., врач-гастроэнтеролог; проф., зав. кафедрой Пропедевтики внутренних болезней.
Ростов-на-ДонуРецензия
Для цитирования:
Коробка В.Л., Пак Е.С., Шаповалов А.М., Кострыкин М.Ю., Ткачев А.В. Оценка четырехлетнего ведения листа ожидания трансплантации печени Ростовской области: перспективы снижения смертности в листе. Медицинский вестник Юга России. 2019;10(3):32-39. https://doi.org/10.21886/2219-8075-2019-10-3-32-39
For citation:
Korobka V.L., Pak E.S., Shapovalov A.M., Kostrykin M.U., Tkachev A.V. Analysis of four-year management of the waiting list for liver transplantation in Rostov region: prospects for reducing mortality of candidates listed for liver transplantation. Medical Herald of the South of Russia. 2019;10(3):32-39. (In Russ.) https://doi.org/10.21886/2219-8075-2019-10-3-32-39







































