Перейти к:
Опыт комплексной оценки эффективности антигипертензивной терапии в клинической практике
https://doi.org/10.21886/2219-8075-2019-10-3-62-71
Аннотация
Цель исследования: изучить антигипертензивную эффективность новой лекарственной формы периндоприла А - таблетки, диспергируемые в полости рта, в группе пациентов с артериальной гипертонией (АГ) в амбулаторных условиях.
Материала и методы: в исследование было включено 30 пациентов (средний возраст 53,8±0,9 лет) с наличием АГ, диагностированной первично, или с отсутствием контроля АД на фоне предшествующей антигипертензивной терапии. Всем исследуемым назначался периндоприл А в виде диспергируемой формы в дозе 10 мг в монотерапии или в составе комбинации с индапамидом - в случае недостижения целевого АД через 2 недели наблюдения. Общая продолжительность исследования - 3 месяца.
Результаты: к концу наблюдения САД/ДАД снизилось на 35,6±2,3/16,5±1,0 мм рт.ст. Коррекция терапии с добавлением индапамида-ретард потребовалась у 6 (20%) пациентов. Эффективная антигипертензивная терапия сопровождалась достоверным уменьшением суточной (по данным СКАД), внутривизитной, и межвизитной вариабельности САД, которая к концу наблюдения составляла 4,4 мм рт.ст по показателю стандартного отклонения. Использование новой лекарственной формы периндоприла А сопровождалось значительным повышением приверженности к проводимой терапии.
Заключение: применение новой лекарственной формы периндоприла А - таблетки, диспергируемые в полости рта - в монотерапии или комбинации с индапамидом-ретард позволяет повысить эффективность лечения больных с АГ, не имеющих целевых значений АД.
Для цитирования:
Солгалова С.А., Глухова Т.В., Знаменская И.А., Романова И.Б. Опыт комплексной оценки эффективности антигипертензивной терапии в клинической практике. Медицинский вестник Юга России. 2019;10(3):62-71. https://doi.org/10.21886/2219-8075-2019-10-3-62-71
For citation:
Solgalova S.A., Glukhova T.V., Znamenskaya I.A., Romanova I.B. The experience of a comprehensive assessment of the effectiveness of antihypertensive therapy in clinical practice. Medical Herald of the South of Russia. 2019;10(3):62-71. (In Russ.) https://doi.org/10.21886/2219-8075-2019-10-3-62-71
Введение
Артериальная гипертония (АГ) является ведущим фактором риска развития сердечно-сосудистых (инфаркт миокарда, инсульт, ишемическая болезнь сердца (ИБС) , хроническая сердечная недостаточность), цереброваскулярных (ишемический или геморрагический инсульт, транзиторная ишемическая атака) и почечных осложнений (хроническая болезнь почек). Как показали клинические исследования, контроль артериального давления (АД) значительно снижает риск церебральных и кардиальных событий и связанных с ними смертельных исходов, на долю которых в числе умерших от всех причин приходится более 55 % смертей [1]. Вместе с тем, в РФ, по данным ФГБУ «ГНИЦ профилактической медицины» Министерства здравоохранения РФ, эффективно лечатся лишь 22 % больных АГ [2]. Недостатки лечения обычно обусловлены неправильным выбором препаратов или их доз, использованием нерациональных комбинаций препаратов, а также проблемами, связанными с приверженностью к лечению [3].
Широкая распространенность АГ, сохраняющаяся на достаточно высоком уровне частота осложнений, инвалидизация, снижение качества жизни больных инициируют создание и внедрение в клиническую практику новых лекарственных форм препаратов для увеличения удобства приема и повышения приверженности больных к рекомендациям, данными лечащим врачом [4].
В 2012 г. на отечественной фармацевтическом рынке зарегистрирована измененная лекарственная форма препарата периндоприл А (Престариум А — таблетки, диспергируемые в полости рта, — лаборатории Сервье, Франция). Периндоприл А — лидер в отношении уровня доказательности его положительного влияния на функцию эндотелия, и именно с этим эффектом связывают наличие особых показаний к применению препарата при АГ. Он продемонстрировал способность не только снижать АД, но и замедлять поражение органов-мишеней и улучшать прогноз, что убедительно доказано в таких крупных международных клинических исследованиях как PROGRESS, EUROPA, снижение сердечно-сосудистой и общей смертности (ADVANCE, ASCOT, HYVET, EVROPA) [5].
Растворенный в полости рта периндоприл А попадает в желудок, где подвергается гидролизу под воздействием кислой среды и распадается на аргинин и периндоприл. И уже далее периндоприл начинает всасываться в начальных отделах тонкого кишечника, имея такую же фармакинетику, как и таблетированная лекарственная форма. Таким образом, диспергируемый вариант препарата сохраняет все свойства классической лекарственной формы периндоприла А.
Для оценки эффективности, безопасности и переносимости новой формы периндоприла А — таблеток, диспергируемых в полости рта, —было проведено наблюдение за пациентами, принимающими данный лекарственный препарат при АГ в амбулаторных условиях.
В рамках проводимого исследования мы поставили следующие задачи:
- Изучить степень контроля АД на фоне приема формы периндоприла А — таблеток, растворимых во рту.
- Оценить влияние препарата на суточную, внутри и межвизитную вариабельности АД на фоне проводимой терапии.
- Оценить потенциальную потребность пациентов в диспергируемой форме периндоприла А.
- Оценить приверженность к лечению пациентов при приеме новой лекарственной формы периндоприла А.
Материалы и методы
В исследование были включены пациенты в возрасте от 30 лет и старше с наличием АГ, диагностированной первично или отсутствием контроля АД (САД > 140/90 и /или ДАД > 90 мм рт. ст.) на фоне предшествующей моно- или комбинированной антигипертензивной терапии, в том числе с использованием классической формы перин- доприла А в дозе 5 мг.
Все больные подписали письменное согласие на обследование. Исследование было проведено в соответствии с международными стандартами GCP.
В состав группы наблюдения вошли 15 мужчин и 15 женщин (средний возраст 53,8 ± 0,9 лет). Продолжительность заболевания в среднем составляла 5,7 ± 0,6 лет.
У исследуемых выявлены следующие наиболее значимые факторы риска: нарушения липидного спектра у 16 (53,3 %), увеличение ИМТ > 25 у 28 (93,3 %), курение у 8 (26,6 %), малоподвижный образ жизни у 21 (70 %) пациентов. Признаки гипертрофии левого желудочка зарегистрированы у 20 (66,6 %) больных.
Критериями исключения служили непереносимость ИАПФ, участие в любом другом исследовании в течение 30 дней перед набором. Тяжелые сердечно-сосудистые и легочные заболевания, включающие острый инфаркт миокарда, острое нарушение мозгового кровообращения в анамнезе, ИБС (стабильную стенокардию III-IV ФК, нестабильную стенокардию), ХСН, декомпенсированный сахарный диабет II типа, бронхиальную астму, ХОБЛ, хроническую почечную недостаточность, беременность, отёк Квинке в анамнезе, двусторонний стеноз почечных артерий.
После предварительного скрининга, согласно критериям включения/исключения, пациентам, ранее не лечившимся (13 человек), получавшим обычную классическую форму периндоприла А (6 человек) или монотерапию другими ИАПФ (4 человека), назначался периндоприла А, растворимая во рту форма, в дозе 10 мг. У 7 пациентов была проведена замена ИАПФ на 10 мг диспергируемой формы периндоприла А в составе предшествующей комбинированной терапии: ИАПФ+диуретик- у 3-х , ИАПФ+диуретик + бета-адреноблокатор — у 1-го, ИАПФ + бета-адреноблокатор — у 2-х, ИАПФ+агонист имидазолиновых рецепторов — у 1-го из них .
Через 2 недели терапии при недостижении целевого АД у 6 (20 %) человек был добавлен индапамид-ретард (Арифон-ретард лаборатории Сервье, Франция) в дозе 1,5 мг. Общая продолжительность наблюдения составила 3 месяца, в течение которого состоялись 4 визита с измерением АД, определением частоты сердечных сокращений (ЧСС) и оценкой эффективности диспергируемой формы периндоприла А (визит включения через 2 недели, 1 месяц, 3 месяца терапии).
В настоящем исследовании для оценки уровня АД на фоне проводимой терапии применили трехуровневую систему контроля с использованием клинического мониторирования АД (в кабинете врача на определённых этапах лечения — визитах), измерение АД в домашних условиях-самостоятельный контроль АД (СКАД) за 4 недели наблюдения и суточное мониторирование АД (СМАД) в начале наблюдения и через 3 месяца терапии.
Измерение клинического АД и ЧСС
Измерение АД и ЧСС выполнял врач. АД измеряли на одной и той же руке в положении сидя после не менее 10-минутного отдыха. В ходе одного визита выполнялось 3 измерения АД и ЧСС с интервалом 1 мин в положении пациента сидя с расчётом средних показателей.
После каждого визита и перед последним визитом исследуемые выполняли СКАД. Измерение артериального давления проводилось пациентом в течение 7 суток утром (с 6.00 до 9.00) и вечером (с 18.00 до 21.00) по 2 измерения с интервалом 5 минут до приёма пищи с занесением данных в дневники. Все результаты, в том числе рассчитанные средние значения, вносились в дальнейшем врачом в индивидуальную регистрационную карту больного.
СМАД проводилось амбулаторно по общепринятой методике с расчётом средних величин, суточных индексов систолического (САД) и диастолического (ДАД) давления, индексов времени АГ.
Вариабельность АД
Внутривизитная вариабельность САД и ДАД рассчитывалась как стандартное отклонение среднего для 3-х измерений АД на приеме у врача. Межвизитную вариабельность мы оценивали для пар последовательных визитов как стандартное отклонение среднего для средних значений АД. Суточная вариабельность АД определялась как стандартное отклонение (SD) утренних минус вечерние значения, колебаний АД в различные дни (утро-утро, вечер-вечер) с расчетом средних показателей за неделю после каждого визита и перед окончанием исследования по данным СКАД.
Приверженность к терапии оценивалась по анкете комплаентности Батюшина М.М, которую пациенты заполняли самостоятельно на первом и последнем визитах. Приверженность к терапии рассчитывалась в баллах, сумма которых определяла коэффициент комплаентности у каждого участника исследования (0 - 14 баллов - высокий, 15 - 19 баллов - средний, 20 и более баллов - низкий).
Все исследуемые параметры проанализированы с помощью методов описательной статистики. Данные обрабатывались на персональном компьютере при помощи Microsoft Excel и статистического пакета Medstat. Для каждого параметра указывалось число больных, среднее значение, стандартная ошибка. Для анализа данных в случае их нормального распределения использовался критерий t Стьюдента для парных измерений, а в противном случае — непараметрический критерий Манна- Уитни. Статистически значимыми считали различия при значении р < 0,05.
Результаты
Данные клинического контроля АД представлены на рис. 1.
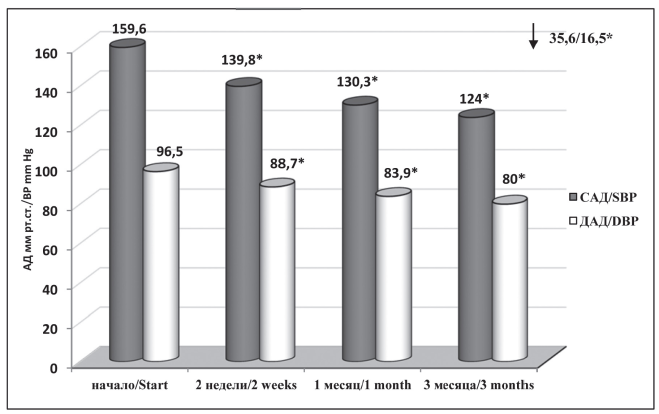
Рисунок 1. Динамика клинического АД на фоне проводимой терапии с использованием диспергируемой формы периндоприла А.
*Достоверность изменений по сравнению с исходным показателем, р < 0,05.
Figure 1. Dynamics of clinical blood pressure on the top of already administered therapy with the use of a dispersible form of perindopril A.
* Reliability of changes compared with an initial index, p < 0,05.
Как видно из полученных результатов, исходное АД составляло, в среднем, по группе 159,6 ± 1,5/96,5 ± 0,8 мм рт.ст. Уже через 2 недели после начала применения диспергируемой формы периндоприла А в составе антигипертензивной терапии отмечалось достоверное снижение САД и ДАД. (р < 0,05). К концу третьего месяца наблюдения абсолютное снижение САД/ДАД составило 35,6 ± 2,3/16,5 ± 1,0 мм рт.ст.
Указанная динамика АД, зарегистрированная на приеме у врача, сопровождалась достоверным уменьшением ЧСС (69,4 ± 1,0 vs 65,6 ± 0,6; р = 0,001).
Коррекция терапии на втором визите потребовалась 6 (20 %) пациентам.
Параллельно с клиническим измерением АД проводился СКАД.
На рис. 2 отражены сравнительные результаты клинического измерения АД и СКАД.
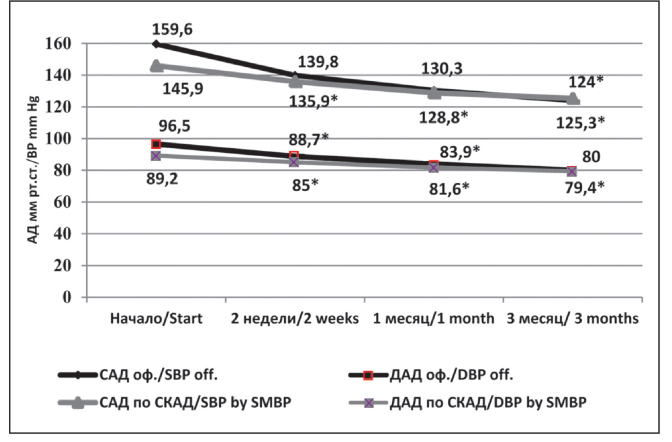
Рисунок 2. Сравнительная динамика уровня клинического АД и АД на фоне проводимой терапии по данным СКАД.
*Достоверность изменений по сравнению с исходным показателем, р < 0,05.
Figure 2. Comparative dynamics of the level of clinical blood pressure and blood pressure on the top of already administered therapy according to SMBP data.
*Reliability of changes compared with an initial index, p < 0,05.
Как видно из представленных данных, средние величины АД, полученные в результате недельного двукратного (утро-вечер) измерения АД в домашних условиях, были аналогичны офисным показателям, повторяли интенсивность снижения АД, и через 3 месяца наблюдения оказались идентичны данным клинического АД. Уже через 2 недели после начала лечения было отмечено достоверное снижение АД до 135,9 ± 1,9/85 ± 1,3 мм рт.ст., через 1 мес. — 128,8 ± 1,4/81,6 ± 1,2, через 3 мес. — 125,3 ± 0,6/79,4 ± 0,8 мм рт.ст.
СМАД выполнено 18 пациентам. По данным СМАД, через 3 месяца исследования среднесуточное САД снизилось на 25,9 ± 1,7 мм рт.ст. (р < 0,001), среднесуточное ДАД — на 11,4 ± 1,4 мм рт.ст. (р < 0,001). Параллельно со снижением уровня АД наблюдалось достоверное уменьшение индекса времени гипертонии САД и ДАД на 27,3 ± 2,4 и 24,7 ± 2,2 соответственно; р < 0,001 (табл. 1). Кроме того, отмечено снижение суточного индекса САД и ДАД (21,1 ± 0,2 vs 16,4 ± 2,1; 23,1 ± 0,6 vs 16,6 ± 2,0 соответственно; р < 0,05).
Таблица / Table 1
Динамика уровня артериального давления на фоне проводимой терапии по данным СМАД.
*Достоверность изменений по сравнению с исходным показателем, р < 0,05
Dynamics of the level of blood pressure on the top of already administered therapy according to DMBP data.
* Reliability of changes compared with an initial index, p < 0,05
Показатели СМАД/ DMBP indicators | Исходно (n=18) Initial (n = 18) | Через 3 мес (n=18) After 3 months (n = 18) |
|---|---|---|
САД среднесуточное/ average daily SBP | 152,1±1,6 | 126,2±0,8* |
ДАД среднесуточное/ average daily DBP | 92,5±0,9 | 81,1±1,1* |
Суточный индекс САД/ Daily index of SBP | 21,1+0,2 | 16,4±2,1* |
Суточный индекс ДАД/ Daily index of DBP | 23,1±0,6 | 16,6±2,0* |
Индекс времени гипертонии САД/ Hypertension time index of SBP | 37,1±2,2 | 9,8±1,2* |
Индекс времени гипертонии ДАД/ Hypertension time index of DBP | 28,8±2,1 | 4,1±0,7* |
Таким образом, при применении различных методов контроля АД на фоне приёма диспергируемой формы периндоприла А, в том числе в комбинации с индапамидомретард, было зарегистрировано достоверное уменьшение АД уже со второй недели терапии с нормализацией САД и ДАД, в целом, по группе через 3 месяца наблюдения и снижением данных показателей за время наблюдения на 35,6/16,5 мм рт.ст. соответственно. Проведенная терапия привела к оптимизации суточного профиля АД у большинства исследуемых.
В Европейских рекомендациях по лечению АГ рекомендовано не только контролировать АД на определенном визите, но и оценивать его изменчивость от визита к визиту, а также в разные дни или недели по суточному СКАД, в связи с чем было решено оценить различные виды вариабельности АД (ВАД) на фоне проводимой антигипертензивной терапии.
Анализ вариабельности АД
В табл. 2 представлены показатели внутривизитной вариабельности САД и ДАД в общей группе наблюдения на фоне лечения.
Таблица / Table 2
Динамика внутривизитной вариабельности САД и ДАД на фоне проводимой терапии с использованием диспергируемой формы периндоприла
А Dynamics of intravisit variability of SBP and DBP on the top of already administered therapy with the dispersible form of perindopril A
Визиты/ Visits | Среднее САД/ДАД/ Mean SBP / DBP | SD мм рт.ст. САД/ДАД/ SD mm Hg SBP / DBP | GV (%) САД/ДАД/ CV (%) SBP / DBP |
|---|---|---|---|
0 | 156,6±1,5/96,5±0,8 | 8,4/4,6 | 5/5 |
1 | 139,8±2,3/88,7±1,2 | 12,9/6,7 | 9/8 |
2 | 130,3±1,7/83,9±1,2 | 9,4/6,3 | 7/8 |
3 | 124±0,8/80±0,7* | 4,6*/4,0* | 4/5 |
*Достоверность изменений по сравнению с исходным показателем, р < 0,05. SD — стандартное отклонение; СУ — коэффициент вариации.
* Significance of change compared with an initial index, p < 0,05. SD — standard deviation; CV — the coefficient of variation.
Как видно из представленных данных, изменения внутривизитной ВАД для САД и ДАД не всегда имели полную линейную зависимость от динамики снижения АД. Достоверное снижение данного показателя (до 4,6/4,0 мм рт.ст.) зарегистрировано только при достижении целевых значений АД у большинства исследуемых к 3-му месяцу лечения.
При анализе межвизитной ВАД (рис. 3 а, б) видно, что наибольшие показатели были между визитом включения и 1-ым (14,0 ± 9,9 и 5,5 ± 3,9 мм рт.ст.), что может быть обусловлено выраженным снижением АД у большинства исследуемых после начала измененной терапии. Достоверное (р < 0,05) уменьшение межвизитной ВАД зарегистрировано в дальнейшем, начиная со 2-го визита (6,7 ± 4,7 и 3,3 ± 2,4 мм рт.ст., для САД и ДАД соответственно) и между 2-м и 3-м визитами (4,4 ± 3,1 и 2,7 ± 1,9 мм рт.ст.).

Рисунок 3. Динамика межвизитной вариабельности САД и ДАД для парных визитов на фоне проводимой терапии с использованием диспергируемой формы периндоприла А.
*Достоверность изменений по сравнению с исходным показателем, р < 0,05.
Figure 3. Dynamics of visit-to-visit variability of SBP and DBP for paired visits on the top of already administered therapy with the dispersible form of perindopril A.
* Reliability of changes compared with an initial index, p < 0.05.
Показатели суточной вариабельности САД и ДАД указаны в табл. 3.
Таблица / Table 3
Суточная вариабельность САД и ДАД по данным СКАД на фоне проводимой терапии с использованием диспергируемой формы периндоприла А.
Daily variability of SBP and DBP according to SMBP data on the top of already administered therapy with the use of a dispersible form of perindopril A.
| 0 визит/ Visit 0 | 1 визит/ Visit 1 | 2 визит/ Visit 2 | 3 визит/ Visit 3 |
|---|---|---|---|---|
В разные дни САД/ДАД/ At different days SBP / DBP | 145,4±2,2/89,2±1,1 | 135,9±1,9*/85,0±1,3* | 128,8±1,4* /81,6±1,2* | 125,3±0,6*/79,4±0,8* |
Утро-вечер САД/ДАД/ Morning - evening SBP / DBP | 3,9±0,6/1,9±0,3 | 2,1±0,4*/1,6±0,2* | 1,3±0,3 */1,7±0,3* | 1,6±0,3*/ 1,3±0,2* |
Утреннее в разные дни САД/ДАД/ Morning BP on different days SBP / DBP | 1,2±0,07/1,0±0,03 | 1,3±0,08/1,1±0,06 | 1,2±0,08/ 1,0±0,04 | 1,2±0,09/1,0±0,04 |
Вечерние в разные дни САД/ДАД/ EveningBP on different days SBP / DBP | 1,1±0,06/1,0±0,05 | 1,2±0,07/1,0±0,04 | 1,1±0,06/ 1,3±0,08 | 1,3±0,09/1,25±0,09 |
*Достоверность изменений по сравнению с исходным показателем, р < 0,05.
* Significance of change compared with baseline, p < 0,05.
По результатам СКАД, начиная со второй недели терапии выявлено достоверное (р < 0,05) и сохраняющееся в течение всего срока наблюдения уменьшение ВАД, измеренного утром и вечером (первый визит — 2,1 ± 0,4 для САД и 1,6 ± 0,2 для ДАД; второй визит — 1,3 ± 0,3 для САД и 1,7 ± 0,3 для ДАД; третий визит — 1,6 ± 0,3 для САД и 1,3 ± 0,2 для ДАД мм рт.ст.), что свидетельствует о стойком снижении уровня АД в течение суток.
Утренние и вечерние колебания САД и ДАД в разные дни (утро — утро, вечер — вечер) были практически одинаковы и не зависели от динамики изменения АД в процессе проводимой терапии.
Таким образом, проведенная оценка различных видов вариабельности САД и ДАД на фоне антигипертензивной терапии в реальной клинической практике показала, что исходная внутривизитная вариабельность и ее динамика на фоне лечения зависели от степени АГ и достижения целевых значений АД. Эффективная антигипертензивная терапия с применением новой лекарственной формы периндоприла А в моно-и комбинированной терапии с индапамидом-ретард в течение трех месяцев сопровождалась достоверным уменьшением межвизитной вариабельности САД с достижением SD, равным 4,4 мм рт.ст. Для оценки суточной вариабельности наиболее показательными были колебания АД, измеренного утром и вечером самим пациентом. Обоснованием создания и использования периндоприла А, растворимого в полости рта, явилась, в первую очередь, возможность увеличения удобства приема лекарства в любых условиях без применения жидкости и незаметно для окружающих, что могло существенно повысить приверженность больных к проводимой терапии.
В настоящем исследовании было решено попытаться ответить на вопрос: «Действительно ли новая лекарственная форма периндоприла А удобна в применении по мнению пациентов?» Так стало возможным оценить потенциальную потребность больных в диспергируемой форме периндоприла А. С этой целью все участники исследования заполнили две анкеты: в период формирования группы наблюдения — анкету по оценке удобства приема любого лекарственного препарата, а после 3-х месячной терапии — анкету по оценке удобства использования растворимого в полости рта периндоприла А.
В начале наблюдения на вопрос «Сложно ли Вам проглотить таблетки без воды (не запивая)?» 22 человека (73,3 %) ответили: «Да». На вопрос «Если нет возможности запить таблетки, то что Вы сделаете?» 18 пациентов (60 %) ответили: «Приму позже», 7 (23,3 %) — «Разжую и проглочу», а 5 (16,7 %) — «Проглочу, не запивая». На вопрос «Представляется ли Вам удобным приём диспергируемых таблеток?» утвердительно ответило большинство (28; 93,3 %) исследуемых.
Повторный опрос больных после завершения терапии при оценке новой лекарственной формы периндоприла А показал следующее: 28 (93,3 % ) респондентов полностью сохранили свое первоначальное мнение и 21 исследуемый (70 %) оказался готов перейти на прием диспергируемой формы периндоприла А в дальнейшем.
Таким образом, использование лекарственной формы периндоприла А — таблеток, диспергируемых в полости рта, — в реальной клинической практике оказалось удобным для большинства пациентов.
Приверженность к терапии
До начала исследования приверженность к терапии в среднем по группе составляла 13,3 ± 1,9 балла, что, по анкете Батюшина М.М., расценивается как высокая. Вместе с тем, только 19 человек (63 %) имели высокую мотивацию к проводимой терапии (средний балл по группе — 6,3 ± 1,0), 3 человека (10 %) — среднюю (15,7 ± 0,6 баллов), а у 8 человек (27 %) приверженность оценивалась по полученным результатам как низкая (29 ± 1,7 баллов по анкете комплаентности). Через 3 месяца, по данным анкетирования, приверженность к терапии в целом по группе достоверно (р < 0,003) увеличилась: средний балл составил 5,8 ± 1,4, а исследуемых с высокой комплаентностью (в среднем, 4,1 ± 0,6 баллов) стало 26 человек (86,7%); низкая приверженность к лечению (38 баллов) сохранилась у одного больного. У пациентов, находящихся на монотерапии периндоприлом А к концу исследования зарегистрирована высокая комплаентность в 100 % случаев (средний показатель по группе — 3,5 ± 0,7 баллов).
Итак, проведенная эффективная терапия АГ с достижением целевых значений АД у всех пациентов сопровождалась значительным повышением у них мотивации к продолжению назначенного лечения.
Обсуждение
Настоящее исследование было проведено для изучения антигипертензивной эффективности новой лекарственной формы периндоприла А — таблеток, диспергируемых в полости рта, — в группе пациентов с артериальной гипертонией в амбулаторных условиях. В процессе наблюдения применили трехуровневую систему контроля с использованием клинического мониторирования АД (в кабинете врача на определённых этапах лечения — визитах), СКАД за 4 недели наблюдения и СМАД через 3 месяца терапии.
По данным офисных измерений, на фоне приёма диспергируемой формы периндоприла А, в том числе в комбинации с идапамидом-ретард, было отмечено достоверное уменьшение АД уже со второй недели терапии, а через 3 месяца снижение составило по САД и ДАД 35,6/16,5 мм рт.ст. соответственно с достижением целевых значений АД у всех участников группы наблюдения.
Экспертами Европейского общества по гипертонии (ESH) и Европейского общества кардиологов (ESC) рекомендуется, помимо офисного измерения АД, проводить и внеофисное, которое включает не только суточное мониторирование АД (СМАД), но и самоконтроль АД (СКАД) [6].
По сравнению с офисным АД, при СКАД имеется множество значений за несколько дней или даже за более продолжительное время, полученных в привычной для пациента обстановке. В отличие от СМАД, СКАД более дешево, более доступно и его легче повторить [7]. Домашнее АД сильнее коррелирует с вызванным АГ поражением органов мишеней, в частности, с гипертрофией левого желудочка, чем офисное АД [8][9]. Последние мета-анализы небольшого числа проспективных исследований, проведенных в общей популяции, в первичном звене медицинской помощи и у больных АГ, свидетельствуют о том, что домашнее АД гораздо лучше помогает прогнозировать сердечно-сосудистую заболеваемость и смертность, чем офисное АД [10][11]. Исследования, в которых выполнялось и СМАД, и СКАД, показывают, что домашнее АД как минимум столь же хорошо коррелирует с поражением органов- мишеней, как амбулаторное АД [8][9].
При оценке результатов СКАД в настоящем исследовании получены величины АД, которые, в целом, были аналогичны офисным показателям и повторяли тенденцию к уменьшению АД на фоне терапии, что свидетельствует о равнозначности этих методов контроля уровня АД при условии соблюдения установленных правил измерения АД в домашних условиях.
Многие исследования свидетельствуют о том, что показатели СМАД являются более чувствительными, чем клинически измеренное АД, предикторами риска сердечнососудистых исходов [12][13][14]. По данным этих исследований преимущество СМАД было продемонстрировано как в общей популяции, так и в различных группах больных АГ (у лиц молодого и пожилого возраста, у женщин и мужчин, у леченых и нелеченых, из группы высокого риска и у пациентов, страдающих сердечно-сосудистыми и почечными заболеваниями).
Использование СМАД для оценки эффективности проводимого лечения, позволило исключить участие в исследовании больных с «гипертонией белого халата». По данным СМАД, которое проводилось дважды — на этапе включения и в конце исследования, — наряду с уточнением динамики АД зарегистрировано положительное влияние проводимой терапии на суточные колебания АД.
В литературе широко обсуждается прогностическое значение вариабельности АД. По данным многих исследований [15][16][17][18][19] наибольшее влияние на прогноз у больных с АГ оказывает межвизитная ВАД, в том числе в развитии инсульта и коронарных осложнений. Среднесрочная ВАД, оцениваемая по данным СКАД, показала свое высокое прогностическое значение в общей популяции в исследовании Finn-Home Study и Охасамском исследовании [20].
В нашем наблюдении осуществлена оценка суточной, внутри- и межвизитной вариабельности АД на фоне антигипертензивной терапии.
Проведённый анализ внутривизитной вариабельности САД и ДАД показал, что исходная внутривизитная вариабельность и ее динамика на фоне лечения зависели от степени АГ с достоверным изменением лишь при достижения целевых значений АД. Эффективная антигипертензивная терапии с применением новой лекарственной формы периндоприла А в моно-и комбинированной терапии с индапамидом-ретард в течение трех месяцев сопровождалось достоверным уменьшением межвизитной вариабельности САД с достижением SD, равным 4,4 мм рт.ст., что, по мнению исследователей, ассоциируется с уменьшением риска смерти от любой причины. Так, по данным популяционного исследования NHANES III, риск смерти от любой причины был на 50 % выше у лиц, у которых (SD) среднего САД для трёх визитов составило более 8,3 мм рт.ст., по сравнению с лицами, у которых SD было менее 4,8 мм рт.ст. [16].
Для оценки суточной вариабельности АД наиболее показательными были колебания АД, измеренного утром и вечером, которые уменьшались по мере нормализации АД, и отражали равномерность изменения АД в течение суток. Утренние и вечерние колебания САД и ДАД в разные дни (утро — утро, вечер — вечер) были практически одинаковы и не зависели от динамики изменения АД в процессе проводимой терапии.
Одним из ведущих факторов неэффективности лекарственной терапии является некорректное соблюдение больными рекомендаций, полученных от врача. Так, по данным исследования ЭПОХА — 2 (2004 г.), в котором были проанализированы результаты терапии 19500 респондентов с АГ из 8 субъектов европейской части РФ, не привержены к терапии были 76,5 % из них. Повышению комплаентности пациентов к фармакотерапии способствует упрощение схем терапии, применение рациональных комбинаций, создание новых усовершенствованных лекарственных форм.
Изучение потенциальной потребности пациентов в новой диспергируемой форме периндоприла А показало, что использование данного препарата в реальной клинической практике удобно для большинства больных, и в процессе терапии зарегистрировано значительное повышение мотивации пациентов к продолжению назначенного лечения, что можно объяснить также эффективной терапией АГ с достижением целевых значений АД.
Заключение
Проведенная трехмесячная терапия АГ с использованием новой лекарственной формы периндоприла А — таблеток, диспергируемых в полости рта, — в моно- или комбинированной терапии привела к достижению целевых значений АД у всех исследуемых, оказалась удобной для большинства пациентов и сопровождалась достоверным уменьшением суточной, внутри- и межвизитной вариабельности АД, что, по-видимому, явилось причиной повышения их мотивации к продолжению назначенного лечения.
Некоторые данные были частично опубликованы в виде тезисов [21][22][23].
Список литературы
1. Чазова И.Е., Ратова Л.Г., Бойцов С.А., Небиеридзе Д.В. Диагностика и лечение артериальной гипертензии (Рекомендации Российского медицинского общества по артериальной гипертонии и Всероссийского научного общества кардиологов) // Системные гипертензии. – 2010 №3. – с. 5-26.
2. Оганов Р.Г., Тимофеева Т.Н., Колтунов И.Е., Константинов В.В., Баланова Ю.А., Капустина А.В., и другие. Эпидемиология артериальной гипертонии в России. Результаты федерального мониторинга 2003-2010 гг. // Кардиоваскулярная терапия и профилактика. – 2011. - №10(1). – С.9-13.
3. Карпов Ю.А., Горбунов В.М., Деев А.Д. Исследование ПРОРЫВ 2: влияние фиксированной комбинации периндоприл/амлодипин на артериальное давление, измеренное в кабинете врача, с помощью суточного мониторирования и самоконтроля, у пациентов с неконтролируемой артериальной гипертонией // Атмосфера. Новости кардиологии. – 2014. - №1. – С.2-8.
4. Леонова М.В. Новые лекарственные формы и системы доставки лекарственных средств: особенности пероральных лекарственных форм. // Лечебное дело. – 2009. № 3. – С. 18–26.
5. Роберто Феррари. Престариум А с точки зрения доказательной медицины. 2014. – 27 с.
6. Рекомендации по лечению артериальной гипертонии Европейского общества по гипертонии (ESH) и Европейского общества кардиологов (ESC), 2013 // Российский кардиологический журнал. – 2014. - № 1 (105). – С. 7-94.
7. Kikuya M, Ohkubo T, Metoki H, Asayama K, Hara A, Obara T, et al. Day-by-day variability of blood pressure and heart rate at home as a novel predictor of prognosis: the Ohasama study. // Hypertension. – 2008. – 52. – Р.1045–1050.
8. Bliziotis IA, Destounis A, Stergiou GS. Home vs. ambulatory and office blood pressure in predicting target organ damage in hypertension: a systematic review and meta-analysis // J Hypertens. – 2012. – 30. – Р.1289–1299.
9. Gaborieau V, Delarche N, Gosse P. Ambulatory blood pressure monitoring vs. self-measurement of blood pressure at home: correlation with target organ damage // J Hypertens. – 2008. – 26. – Р.1919–1927.
10. Stergiou G.S., Siontis K.C., Ioannidis J.P. Home blood pressure as a cardiovascular outcome predictor: it’s time to take this method seriously. Hypertension 2010; 55:1301–1303.
11. Ward AM, Takahashi O, Stevens R, Heneghan C. Home measurement of blood pressure and cardiovascular disease: systematic review and meta-analysis of prospective studies. J Hypertens. – 2012. – 30. - Р.449–456.
12. Boggia, J., Li, Y., Thijs, L., Hansen, T., Kikuya, M., Björklund-Bodegård, K., et al. Prognostic accuracy of day vs. night ambulatory blood pressure: a cohort study // Lancet. - 2007. Vol. 370. - P. 1219–1229.
13. Conen D, Bamberg F. Noninvasive 24-h ambulatory blood pressure and cardiovascular disease: a systematic review and meta-analysis // J. Hypertens. – 2008. – 26. – Р.1290–1299.
14. Fagard R.H., Celis H., Thijs L., Staessen J.A., Clement D.L., De Buyzere M.L., et al. Daytime and night-time blood pressure as predictors of death and cause-specific cardiovascular events in hypertension // Hypertension. – 2008. – 51. – Р. 55–61.
15. Rothwell, P., Howard, S., Dolan, E., O'Brien, E., Dobson, J., Dahlöf, B., et al. Prognostic significance of visit-to-visit variability, maximum systolic blood pressure and episodic hypertension // Lancet. – 2010. – 375. Р.895—905.
16. Muntner, P., Shimbo, D., Tonelli, M., Reynolds, K., Arnett, D. and Oparil, S. The relationship between visit-to-visit variability in systolic blood pressure and all-cause mortality in the general population: findings from NHANES III, 1988 to 1994 // Hypertension. – 2011. – 57. Р. 160—166.
17. Webb A., Fischer U., Mehta Z., Rothwell P.M. Effects of antihypertensive drug class on interindividual variation in blood pressure and risk of stroke: a systematic review and meta-analysis. // Lancet. - 2010. – 375. Р.906—915.
18. Rothwell P.M. Limitations of usual pressure hypothesis and the importance of variability, instability and episodic hypertension. // Lancet. – 2010. – 375. – Р. 938— 948.
19. Mancia G., Facchetti R., Parati G., Zanchetti A. Visit-to-visit blood pressure variability in the European Lacidipine Study on Atherosclerosis: methodological aspects and effects of antihypertensive treatment. // J Hypertens. - 2012. – 30. – Р.1241—1251.
20. Кобалава, Ж.Д., Котовская Ю.В., Троицкая Е.А. Межвизитная вариабельность артериального давления: клиническое и прогностическое значение, практическое применение/ Ж.Д. Кобалава, Ю.В. Котовская, Е.А. Троицкая. - Москва 2013. – 23 с.
21. Глухова Т.В., Солгалова С.А., Путренок Л.С. Исследование вариабельности артериального давления в клинической практике. // Здоровье населения и среда обитания : материалы научно-практической конференции. 19-я ежегодная Неделя медицины Ставрополья. – Ставрополь : Ставропольское издательство «Параграф», 2015. – 184 с.
22. Глухова Т.В., Солгалова С.А. Вариабельность артериального давления: значение в амбулаторной практике. // Актуальные вопросы современной медицины и гериатрии: материалы VII межрегиональной научно-практической гериатрической конференции врачей первичного звена здравоохранения Северо-Кавказского федерального округа, I межрегиональной научно-практической гериатрической конференции врачей первичного звена здравоохранения Республики Крым. – Ставрополь – Симферополь: Изд-во СтГМУ, 2016. – 278 с.
23. Глухова Т.В., Солгалова С.А. Характеристика приверженности терапии больных с артериальной гипертонией. // Актуальные вопросы современной медицины: материалы научно-практических конференций Форума, посвященного 50-летию дополнительного профессионального медицинского образования на Северном Кавказе. Часть I. – Ставрополь: Изд-во СтГМУ, 2015. – 328 с.
Об авторах
С. А. СолгаловаРоссия
Солгалова Светлана Александровна - к.м.н., доцент кафедры медико-социальной экспертизы, реабилитации с курсом гериатрии/
СтавропольТ. В. Глухова
Глухова Татьяна Вениаминовна - к.м.н, доцент кафедры терапии с курсом диетологии.
СтавропольИ. А. Знаменская
Знаменская Илона Александровна - к.м.н, доцент кафедры госпитальной терапии.
СтавропольИ. Б. Романова
Романова Ирина Борисовна - кафедра госпитальной терапии.
СтавропольРецензия
Для цитирования:
Солгалова С.А., Глухова Т.В., Знаменская И.А., Романова И.Б. Опыт комплексной оценки эффективности антигипертензивной терапии в клинической практике. Медицинский вестник Юга России. 2019;10(3):62-71. https://doi.org/10.21886/2219-8075-2019-10-3-62-71
For citation:
Solgalova S.A., Glukhova T.V., Znamenskaya I.A., Romanova I.B. The experience of a comprehensive assessment of the effectiveness of antihypertensive therapy in clinical practice. Medical Herald of the South of Russia. 2019;10(3):62-71. (In Russ.) https://doi.org/10.21886/2219-8075-2019-10-3-62-71







































