Перейти к:
Эффективность комплексной терапии у пациентов с а- и гипогаммаглобулинемией.
https://doi.org/10.21886/2219-8075-2018-9-4-57-62
Аннотация
Цель: оценка эффективности применения Полимурамила в комплексной с ВВИГ терапии пациентов с ОВИН и Х-АГГ с недостаточной эффективностью заместительной терапии.
Материалы и методы: под наблюдением находилось 10 пациентов с недостаточной эффективностью заместительной терапии ВВИГ, получающие комплексную терапию ВВИГ и иммуномодулятор Полимурамил в дозе 200 мкг / 0,5 мл № 5 внутримышечно через день. С помощью проточной цитофлюориметрии до начала лечения, сразу после и через 3 месяца оценивали поверхностные и внутриклеточные маркеры клеток врожденного и приобретенного иммунного ответа, содержание сывороточных иммуноглобулинов класса А, M, G– в реакции радиальной иммунодиффузии в геле по Манчини, кислородзависимую метаболическую активность нейтрофилов в НСТ-тесте и проводили сравнительный анализ полученных данных.
Результаты и выводы: показано, что у пациентов с генетически опосредованным дефектом гуморального звена на фоне комплексной терапии с применением Полимурамила регистрируется активация врожденного и адаптивного иммунитета, что подтверждается, помимо лабораторных показателей, снижением частоты обострений хронических воспалительных заболеваний.Ключевые слова
Для цитирования:
Кролевец Д.И., Сизякина Л.П., Андреева И.И., Яковлев А.А., Баштовая О.А. Эффективность комплексной терапии у пациентов с а- и гипогаммаглобулинемией. Медицинский вестник Юга России. 2018;9(4):57-62. https://doi.org/10.21886/2219-8075-2018-9-4-57-62
For citation:
Krolevets D.I., Sizyakina L.P., Andreeva I.I., Yakovlev A.A., Bashtovaya O.A. Efficiency of complex therapy in patients with a- and hypogammaglobulinemia. Medical Herald of the South of Russia. 2018;9(4):57-62. (In Russ.) https://doi.org/10.21886/2219-8075-2018-9-4-57-62
Введение
Первичные иммунодефициты (ПИД) — многочисленная группа генетически обусловленных заболеваний, приводящих к нарушению каскада иммунных реакций и последующей восприимчивостью к инфекциям, предрасположенностью к развитию аутоиммунной и лимфопролиферативной патологии [1]. Эти заболевания характеризуются ранним началом и хронизацией процесса, торпидностью к традиционным методам лечения и необходимостью проведения иммунореабилитации в течение всей жизни [2].
По данным Европейского общества по ПИД (ESID), иммунодефицитные состояния с нарушением продукции антител — наиболее часто встречающаяся патология, которая составляет более 50 % от общего количества генетически обусловленных иммунодефицитов [3]. Из них наиболее распространенные нозологии — общевариабельная иммунная недостаточность (ОВИН) и Х-сцепленная агаммаглобулинемия (Х-АГГ). Клинически для пациентов с этими диагнозами характерны рецидивирующее течение хронических инфекционных заболеваний, таких как отиты, синуситы, бронхиты, пиелонефриты с частотой обострений до 8-10 раз в год, а также патология ЖКТ, суставной синдром, васкулиты, дерматиты [4]. В случае отсутствия адекватно подобранной терапии заболевания могут осложняться тяжелыми и затяжными вариантами течения. Золотым стандартом лечения пациентов с ПИД гуморального звена является регулярное применение заместительной терапии внутривенными иммуноглобулинами (ВВИГ) в поддерживающей дозе [5]. Однако при недостаточной эффективности ВВИГ и развитии обострений хронических воспалительных заболеваний для профилактики осложнений показано применение антибактериальных препаратов [6]. Учитывая достаточно высокую частоту обострений и необходимость продолжительного применения антибиотиков, актуальным является поиск альтернативных методов поддержания более длительной ремиссии у пациентов с недостаточной эффективностью заместительной терапии ПИД гуморального звена [7]. Учитывая, что в отсутствии или при снижении функции гуморального звена иммунной системы неизбежны существенные компенсаторные изменения в клеточном, одним из вариантов стабилизации состояния пациентов может быть воздействие на функциональную активность и адаптивные возможности клеточного звена. С этой целью возможно применение иммуномодуляторов, в частности, Полимурамила, который, являясь активатором врожденного звена иммунной системы, стимулирует бактерицидную активность лейкоцитов, выработку цитокинов и хемокинов макрофагами и дендритными клетками, повышает функциональную активность естественных киллеров [8].
Цель исследования — оценка эффективности применения Полимурамила в комплексной терапии с ВВИГ у пациентов с ОВИН и Х-АГГ с недостаточной эффективностью заместительной терапии ВВИГ.
Материалы и методы
На базе НИИ Клинической иммунологии РостГМУ под наблюдением находятся 25 пациентов, из которых у 10 человек, несмотря на постоянную заместительную терапию ВВИГ, высокая частота рецидивов обострений хронических заболеваний. Критериями включения являлись подтвержденный диагноз первичного иммунодефицита, продолжительность заместительной терапии ВВИГ в дозе 0,4 г/кг веса пациента до начала исследования, минимум, в течение года, достижение нормального претрансфузионного уровня сывороточного IgG более 5 г/л в течение последних 3-х месяцев. Для подтверждения недостаточной эффективности стандартного лечения проводился анализ предоставленной медицинской документации, данные объективных осмотров, результаты оценок иммунного статуса. Лечение оценивали как недостаточно эффективное в случае, если частота обострений хронических заболеваний в течение года превышала 5 раз, что в два раза больше нормальных показателей заболеваемости в популяции.
Пациентам, помимо общепринятой терапии ВВИГ, назначали Полимурамил в дозе 200 мкг / 0,5 мл № 5 внутримышечно через день. До начала комплексной терапии, сразу после и через 3 месяца проводили оценку иммунного статуса. Обследование включало фенотипический анализ иммунокомпетентных клеток, в том числе определение внутриклеточного содержания Гранзима В, экспрессии HLA DR, TLR2, TLR4 на моноцитах периферической крови методом иммунофлюоресценции с учетом результатов на проточном лазерном цитофлюориметре «FC 500» (Becman Coulter, США) с использованием соответствующих моноклональных антител. Кислород-зависимую метаболическую активность нейтрофилов оценивали в НСТ-тесте, содержание сывороточных иммуноглобулинов класса A, M, G — в реакции радиальной иммунодиффузии в геле по Манчини. Исследование проведено в соответствии с международными стандартами GCP.
Сравнение средних уровней в группах проводилось с помощью критерия Вилкоксона для связанных выборок. Различия признавались статистически значимыми на уровне p<0,05. Расчеты выполнялись в R (версия 3.2, R Foundation for Statistical Computing, Vienna, Austria).
Результаты
Проведенный клинический анализ состояния наблюдаемых пациентов показал, что в течение трех месяцев после начала курса комплексной терапии обострения хронических воспалительных заболеваний обнаружены только у 3 из 10 человек, тогда как до его проведения они отмечались у 8 из 10 пациентов. У одного пациента обнаружено обострение пиелонефрита, купируемое антибактериальной терапией в течение 7 дней, у двух других отмечены обострения хронического бронхита, тогда как до начала комплексной терапии у 8 из 10 пациентов отмечались обострения хронического бронхита с продолжительным применением антибиотиков (14±4 дня).
Так, например, у пациентки Б. в течение трех месяцев до начала комплексной терапии каждый месяц регистрировалось обострение бронхита с необходимостью применения антибиотиков в течение, минимум, 10 дней, кроме того, она предъявляла жалобы на боли при мочеиспускании и повышение температуры, не сопровождающиеся другими клиническими симптомами. Таким образом, до начала комплексного лечения у нее зарегистрированы 4 обострения хронических заболеваний. В течение последующих трех месяцев на фоне комплексной терапии при клинических осмотрах регистрировались единичные хрипы в легких, остальные показатели в пределах нормы, состояние удовлетворительное. За это время единожды обращалась к врачу урологу с жалобами на боли при мочеиспускании, обострение было купировано однократным применением антибиотика и курсом диуретического средства растительного происхождения.
При сравнительной оценке результатов иммунологического тестирования до начала терапии и сразу после курса Полимурамила значительных отличий в показателях как врожденного, так и адаптивного иммунного ответа не выявлено (табл. 1). При сравнении результатов исследования до начала комплексной терапии и через три месяца после нее выявленыизменения в показателях маркеров поздней активации Т-лимфоцитов: существенное увеличение количества CD3+HLA DR+-лимфоцитов (19 % ± 4.06 %) по отношению к исходному уровню (7.01 % ± 1.07 %) (табл. 1, рис. 1) и CD8+HLA DR+ -клеток (18.9 % ± 4.04 %), что значительно выше стартовых показателей (6.3 % ± 1.17 %) (табл. 1, рис. 2). Кроме того, в моноци- тарном звене через 3 месяца после применения препарата определяется рост экспрессии TLR 4 от 21.2 % ± 2.3 % до 43.7 % ± 3.81 % (табл. 1, рис. 3). Также отмечается снижение уровня циркулирующих иммунных комплексов на фоне комплексной терапии до 20±6.21 у.е. по сравнению с исходным содержанием (38.1 ± 7.85 у.е.) (табл. 1, рис. 4).
Таблица/ Table 1.
Сравнительная характеристика параметров иммунной системы пациентов с Х-АГГ и ОВИН до начала комплексного лечения, по окончании и через 3 месяца после курса Полимурамила
Comparative characteristics of the parameters of the immune system of patients with XLA and CVID before the beginning of complex treatment, at the end and 3 months after the course of Polymuramil
| До терапии Before therapies | По окончании курса At the end of course | Через 3 месяца после курса 3 months after the course |
|---|---|---|---|
CD3+ | 80.9 ± 2.4 | 82 ± 3.12 | 80 ± 2.06 |
CD3+HLA DR+, % | 7.01 ± 1.07 | 4 ± 2.19 | 19 ± 4.06* |
CD4+,% | 35 ± 3.35 | 36.9 ± 4.23 | 34.7 ± 3.59 |
CD4+CD25, % | 2.73 ± 0.62 | 2.82 ± 0.7 | 2.56 ± 0.3 |
CD4+CD25+Foxp3+, % | 1.63 ± 0.33 | 1.69 ± 0.62 | 1.41 ± 0.18 |
CD8+, % | 44.9 ± 3.74 | 48.2 ± 5.18 | 44.2 ± 4.06 |
CD8+Gr+,% | 34.1 ± 5.39 | 20.2 ± 5.66 | 28.2 ± 3.66 |
CD8+HLA DR,% | 6.3 ± 1.17 | 3.9 ± 2.04 | 18.9 ± 4.04* |
CD16+, % | 9.7 ± 1.72 | 8.3 ± 2.19 | 9.3 ± 1.69 |
CD16+GR+, % | 8.1 ± 1.8 | 8.5 ± 2.37 | 6.7 ± 1.37 |
CD14+HLA DR+,% | 68.5 ± 6.37 | 58.5 ± 7.16 | 68.5 ± 5.66 |
TLR 2,% | 75 ± 4.09 | 73.7 ± 3.64 | 75.7 ± 4.78 |
TLR 4,% | 21.2 ± 2.3 | 32.7 ± 3.81 | 43.7 ± 3.81* |
ЦИК | 38.1 ± 7.85 | 30 ± 8.21 | 20 ± 6.21* |
IgA | 0.36 ± 0.23 | 0.43 ± 0.23 | 0.33 ± 0.23 |
IgM | 0.84 ± 0.057 | 0.9 ± 0.08 | 1.02 ± 0.065 |
IgG | 8.27 ± 0.93 | 7.4 ± 1.13 | 7.4 ± 1.13 |
НСТсп | 98.2 ± 3.3 | 100 ± 4.32 | 103 ± 3.42 |
Кст | 1.58 ± 0.036 | 1.56 ± 0.019 | 1.57 ± 0.026 |
*Примечание: статистически достоверные отличия при p<0,05.
*Note: statistically significant differences atp <0.05.
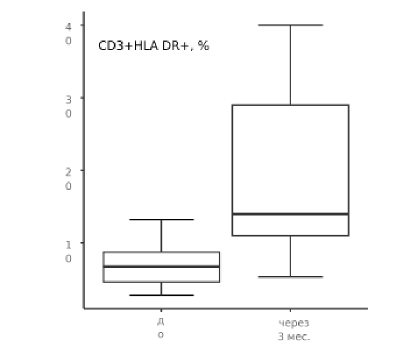
Рисунок 1. Уровень CD3+HLA DR+-лимфоцитов, % до начала комплексной терапии и через 3 месяца после курса Полимурамила.
Figure 1. CD3+HLA DR+lymphocytes level, % before the beginning of the complex therapy and 3 months after the course of Polymuramil.
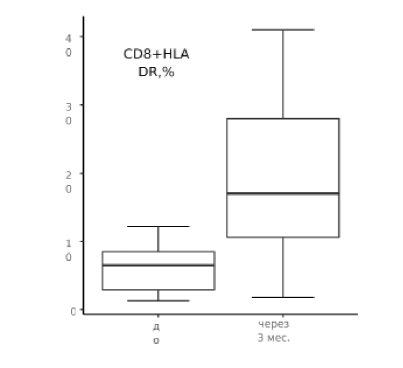
Рисунок 2. Уровень CD8+HLA DR+-лимфоцитов, % до начала комплексной терапии и через 3 месяца после курса Полимурамила.
Figure 2. CD8+HLA DR+lymphocytes level, % before the start of complex therapy and 3 months after the course of Polymuramil.
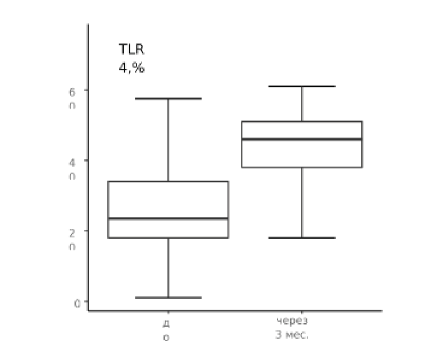
Рисунок 3. Уровень CD14+284+-моноцитов, % до начала комплексной терапии и через 3 месяца после курса Полимурамила.
Figure 3. The level of CD14+284+-monocytes, % before the start of complex therapy and 3 months after the course of Polymuramil.
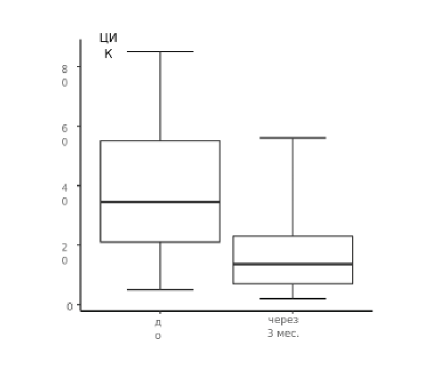
Рисунок 4. Уровень циркулирующих иммунных комплексов, (у.е.) до начала комплексной терапии и через 3 месяца после курса Полимурамила.
Figure 4. The level of circulating immune complexes, before the beginning of complex therapy and 3 months after the course of Polymuramil.
Обсуждение
Таким образом, оценка клинических проявлений у пациентов с а(гипо)гаммаглобулинемией на фоне комплексного лечения показала, что частота обострений хронических воспалительных заболеваний после применения препарата значительно сократилась, а клиническая симптоматика обострений характеризовалась менее выраженной тяжестью течения, что определяется увеличением качественных характеристик клеточного звена иммунного ответа. Анализ полученных данных выявил значительное повышение маркеров активации лимфоцитов, что свидетельствует об индукционных свойствах изучаемого иммуномодулятора за счет увеличения активационных потенций клеточного звена адаптивного иммунитета у пациентов с ПИД. Помимо этого, стабилизация состояния пациентов может быть связана с определяемым выраженным снижением циркулирующих иммунных комплексов, что косвенно отражает усиление элиминационных возможностей иммунной системы. Это заключение подтверждает и значительное увеличение экспрессии TLR4 на моноцитах, что свидетельствует об активации функций фагоцитарного звена.
В заключение стоит отметить, что у пациентов с генетически опосредованным дефектом гуморального звена на фоне комплексной терапии с применением Полимурамила регистрируется активация врожденного и адаптивного иммунитета, что подтверждается снижением частоты обострений хронических воспалительных заболеваний.
Список литературы
1. Хаитов Р.М. Аллергология и иммунология: национальное руководство: краткое издание. – М.: ГЭОТАР-Медиа, 2012.
2. Сизякина Л.П., Андреева И.И. Компенсаторные реакции иммунной системы при дефекте синтеза антител – агаммаглобулинемии // Российский аллергологический журнал. – 2016. -№2. - С.15-18.
3. Bousfha A., Jeddane L., Picard C., et al. Te 2017 IUIS Phenotypic Classifcation for Primary Immunodefciencies // Journal of Clinical Immunology. 2018;38(1):129–143. DOI:10.1007/s10875-017-0465-8
4. Abbott J. K., Gelfand E. W. Common variable immunodefciency: diagnosis, management, and treatment // Immunology and Allergy Clinics. 2015;35(4):637-658. DOI: 10.1016/j. iac.2015.07.009
5. Латышева Е.А., Латышева Т.В., Мартынова И.А. Оценка эффективности и безопасности препарата иммуноглобулина для внутривенного введения И.Г. ВЕНА у пациентов с преимущественным нарушением синтеза антител // Российский аллергологический журнал. –2016. –№1. – С.16-22.
6. Хаитов Р.М., Ильина Н.И. Клиническая иммунология и аллергология. Федеральные клинические рекомендации. - М.: Фармус Принт Медиа, 2015.
7. Сизякина Л.П., Андреева И.И. Первичная агаммаглобулинемия как модель кооперативных взаимосвязей гуморального и клеточного звеньев иммунной системы // Иммунология. – 2016. – №1. – С.14-16. DOI:10.18821/0206-4952-2016-37-1-14-16
8. Пащенков М.В., Алхазова Б.И., Львов В.Л., Пинегин Б.В. Применение ингибиторного анализа для изучения механизмов действия мурамилпептидного иммуномодулятора «Полумурамил». // Медицинская иммунология. - 2013. - №1 - С. 21-28.
Об авторах
Д. И. КролевецРоссия
аспирант кафедры клинической иммунологии и аллернологии ФПК и ППС РостГМУ
Л. П. Сизякина
Россия
д.м.н., профессор, зав.кафедрой клинической иммунологии и аллергологии ФПК и ППС РостГМУ
И. И. Андреева
Россия
д.м.н., доцент кафедры клинической иммунологии и аллергологии ФПК и ППС РостГМУ
А. А. Яковлев
д.м. н., профессор, заведующий кафедрой гастроэнтерологии и эндоскопии с курсом клинической фармакологии ФПК и ППС
О. А. Баштовая
аспирант кафедры гастроэнтерологии и эндоскопии с курсом клинической фармакологии ФПК и ППС
Рецензия
Для цитирования:
Кролевец Д.И., Сизякина Л.П., Андреева И.И., Яковлев А.А., Баштовая О.А. Эффективность комплексной терапии у пациентов с а- и гипогаммаглобулинемией. Медицинский вестник Юга России. 2018;9(4):57-62. https://doi.org/10.21886/2219-8075-2018-9-4-57-62
For citation:
Krolevets D.I., Sizyakina L.P., Andreeva I.I., Yakovlev A.A., Bashtovaya O.A. Efficiency of complex therapy in patients with a- and hypogammaglobulinemia. Medical Herald of the South of Russia. 2018;9(4):57-62. (In Russ.) https://doi.org/10.21886/2219-8075-2018-9-4-57-62







































