Перейти к:
Редкий дебют миеломной болезни в виде острого повреждения почек
https://doi.org/10.21886/2219-8075-2026-17-1-5-10
Аннотация
В статье представлена история болезни пациентки Б., 63 года, с нетипичным дебютом миеломной болезни в виде развития острого почечного повреждения. Описание клинического случая редкого дебюта миеломной болезни очень важно для представления врачам различных специальностей, поскольку демонстрирует вариабельность течения внекостных поражений при данном заболевании, а также особенности вовлечения почечной ткани в процесс. В частности, классический вариант цилиндровой нефропатии у пациентки Б. был маскирован отсутствием патологических изменений в моче и признаков накопления парапротеина в крови, что снижает вероятность правильной диагностики и, следовательно, вовремя начатого лечения. Важно отметить, что описанные изменения в почечной ткани свидетельствуют о выраженной нефротоксичности парапротеина и стремительности развития событий в отношении почечного повреждения.
Ключевые слова
Для цитирования:
Батюшин М.М., Нестеренко И.Н., Белобородова Т.П., Страхова Н.Б., Левицкая Е.С. Редкий дебют миеломной болезни в виде острого повреждения почек. Медицинский вестник Юга России. 2026;17(1):5-10. https://doi.org/10.21886/2219-8075-2026-17-1-5-10
For citation:
Batiushin M.M., Nesterenko I.N., Beloborodova T.P., Strakhova N.B., Levitskaya E.S. Rare onset of myeloma disease in the form of acute kidney injury. Medical Herald of the South of Russia. 2026;17(1):5-10. (In Russ.) https://doi.org/10.21886/2219-8075-2026-17-1-5-10
Введение
Поражение почек при миеломной болезни характеризуется своим клиническим разнообразием. Описаны случаи цилиндровой нефропатии (cast-nephropathy), AL-амилоидоза почек, С3-гломерулопатии, острого и хронического гиперурикемического тубулоинтерстициального нефрита, мочекаменной болезни, тромботической микроангиопатии с поражением почечной ткани, тромбоза и тромбоэмболии ветвей и ствола почечной артерии, лекарственных поражений и другие случаи [1][2]. При некоторых формах миеломной болезни почечные проявления являются не просто результатом осложнения болезни, а её клиническим проявлением. В частности, при миеломе лёгких цепей Бенс-Джонса их появление в моче наблюдается на ранних стадиях гиперсекреции ламбда- и каппа-цепей патологическим плазмоцитарным клоном.
Цилиндровая нефропатия из всего спектра гаммапатий ренального значения является, как правило, маркером миеломной болезни. Весь спектр различных вариантов гаммапатий ренального значения и подходы к их дифференциальной диагностике детально представлены в национальном консенсусе [3]. Цилиндровая нефропатия, как правило, протекает с тяжёлыми функциональными расстройствами почечной функции в виде острого повреждения почек (ОПП) и острой болезни почек (ОБП), возможна также трансформация в хроническую болезнь почек и формирование диализ-зависимости [4]. Патогенетическая суть цилиндровой нефропатии заключается в том, что профильтровавшиеся парапротеины в мочевом пространстве образуют комплексы с уромодулином и образовавшаяся субстанция в виде цилиндров заполняет канальцы, замедляя или полностью останавливая люминальный поток мочи, приводя к полной обструкции [5]. Также поражение почек при цилиндровой нефропатии отчасти может быть объяснено преренальными эффектами гиповолемии, отёком почек («нефросаркой») или тромбозом почечной вены, а также прямой тубулярной токсичностью лёгких цепей иммуноглобулинов и фильтруемых белков плазмы в целом [6][7]. Ниже рассмотрен редкий клинический случай необычного дебюта миеломной болезни.
Описание клинического случая
Пациентка Б., 63 года, поступила в отделение гемодиализа с жалобами на выраженную слабость, головокружение, отсутствие аппетита, снижение диуреза до 600 мл в сутки.
Из анамнеза стало известно, что заболеваниями почек ранее не болела, в течение последних девяти лет отмечала развитие артериальной гипертензии (в среднем артериальное давление — 160/90 мм рт. ст.), корригируемой периндоприлом+индапамидом. В октябре 2018 г. при случайном обследовании в поликлинике по месту жительства обнаружено повышение сывороточного креатинина до 163 мкмоль/л, мочевины — до 9,0 ммоль/л, анализы мочи не сдавала. В ноябре 2018 г. при повторном обследовании: уровень креатинина повысился до 308 мкмоль/л, мочевой кислоты — до 541 ммоль/л, гемоглобин был 120 г/л, в анализах мочи отклонений от нормы не отмечалось, по данным ультразвукового исследования, размеры почек обычные, толщина паренхимы — 18–20 мм, чашечно-лоханочная система не расширена. 29.11.2018 г. при повторном обследовании: уровень креатинина сыворотки вырос до 1100 мкмоль/л, мочевины — до 43,2 ммоль/л, изменений в анализах мочи не наблюдалось, водовыделительная функция почек была сохранена. Пациентка госпитализирована по скорой помощи, был установлен диагноз «Острое повреждение почек 3 ст., ренальное, неуточнённого генеза». Начато лечение гемодиализом. По лабораторным данным: анемия (гемоглобин — 97–83 г/л), уровень креатинина сыворотки — 1150 мкмоль/л, мочевины — 43,2 ммоль/л, общего белка — 70 г/л, по остальным показателям без отклонений от нормы. В общем анализе мочи: уд. вес — 1005, белка нет, лейкоциты — 3–5×, эритроциты — 0–1×.
17.12.2018 г. в связи с сохраняющейся диализ-зависимостью пациентка переведена в отделение гемодиализа.
При поступлении в ходе объективного обследования: состояние средней степени тяжести, кожные покровы бледной окраски, без элементов сыпи, периферические лимфатические узлы не увеличены, пальпируется увеличенная щитовидная железа до 1 степени, безболезненная. Пульс — 74 ударов в минуту, артериальное давление (АД) = 130/80 мм рт. ст. Тоны сердца ритмичны, приглушены. В лёгких дыхание везикулярное, частота дыхательных движений — 16 в минуту. Живот мягкий, безболезненный, печень у края рёберной дуги, селезёнка не пальпируется. Почки не пальпируются, область их безболезненна, периферических отёков нет. Суточный диурез составил 600 мл в сутки.
С целью диагностического поиска причины ОПП было назначено дополнительное обследование.
17.12.2018 г. проведено ультразвуковое исследование (УЗИ) почек. Заключение: размеры обеих почек находятся в нормальном диапазоне (согласно возрасту), паренхима — 17 мм, симптом «выделенных» пирамид, чашечно-лоханочная система не расширена.
17.12.2018 г. выполнено УЗИ органов брюшной полости. Заключение: размеры печени не увеличены, правая доля — 130×155 мм, левая доля — 60×80 мм, эхогенность повышена, паренхима диффузно-неоднородная; поджелудочная железа — 20×12×22 мм, контуры ровные, эхогенность повышена, структура диффузно-неоднородная. Желчный пузырь — 50×25 мм, стенка уплотнена, содержимое неоднородное, холедох — 6 мм, селезенка — 95×48 мм, однородной структуры.
27.12.2018 г. проведена эхокардиография. Заключение: склероз аорты, створок аортального и митрального клапанов, нарушение диастолической функции левого желудочка 1 типа, свободной жидкости в перикарде нет, сократительная функция миокарда левого желудочка сохранена.
Заключение ультразвуковой допплерографии почечных артерий от 27.12.2018 г.: брюшной отдел аорты и почечных артерий проходимы, стенка утолщена, с признаками невыраженного кальциноза (наружный диаметр брюшной аорты — до 27 мм, стволов почечных артерий — до 5 мм), кортикальный кровоток с обеих сторон умеренно снижен, индекс резистентности с обеих сторон умеренно повышен, без значимой асимметрии (0,73–0,84), умеренное внутриорганное снижение скорости кровотока в бассейне почечных артерий с обеих сторон.
Заключение фиброгастродуоденоскопии от 26.12.2018 г.: дуодено-гастральный рефлюкс, луковица двенадцатиперстной кишки гиперемирована, по всем стенкам петехии, лимфоидные фолликулы.
Заключение ультразвукового исследования щитовидной железы от 27.12.2018 г.: обе доли печени нормальных размеров и формы, структура умеренно диффузно-неоднородная, в нижней трети левой доли печени лоцируется округлое образование 13×9 мм, неоднородной структуры, с чёткими контурами, в режиме цветного доплеровского картирования установлен перинодулярный тип.
Лабораторно-инструментальные исследования щитовидной железы позволили определить коллоидный зоб, 2 класс, эутиреоз.
Электрофорез белков сыворотки крови от 19.12.2018 года: общий белок — 66 г/л; альбумин — 60,5%; альфа 1 — 6,54%; альфа 2 — 9,9%; бета 1 — 5,10%; бета 2 — 4,19%; гамма-глобулин — 13,6%. На электрофореграмме отмечается незначительное повышение альфа 1 и снижение бета 1 фракций глобулинов.
По остальным показателям (билирубин, аланин- и аспартат-аминотрансферраза, щелочная фосфатаза, мочевая кислота, холестерин, С-реактивный белок, коагулограмма, сывороточное железо) отклонений от нормы не регистрировалось, или они были незначительными.
В общих анализах мочи отмечалось снижение удельного веса 1005–1004, отсутствие белка, осадок мочи в норме. Суточная протеинурия достигала 0,22 г/сутки.
Поскольку причина ОПП была не ясна, 19.12.2018 г. пациентке была выполнена пункционная нефробиопсия.
Описание нефробиоптата. Светооптически: клубочки без патологических изменений, малокровные, перигломерулярный фиброз, атрофия — от 70 до 90% канальцев, гиалиново-капельная дистрофия эпителия одиночных проксимальных канальцев, в просвете эктазированных канальцев множество белковых цилиндров, местами имеющих «зернистый» или «лучистый» вид. Белковые массы, накапливающиеся в просветах канальцев с перифокальной гигантоклеточной многоядерной реакцией. Единичные цилиндры в канальцах окрашены в кирпично-красный цвет и дают позитивное свечение в поляризованном свете. Капиллярные петли, базальные мембраны канальцев, стенки сосудов отрицательные при окраске на амилоид.
Иммунофлюоресцентная микроскопия: IgA — слабо положительное свечение (+) в канальцах и отсутствует в клубочках, IgG — слабо положительное свечение (+) в канальцах и отсутствует в клубочках, С3 — слабо положительное свечение (+) в одиночных канальцах, Карра — слабо положительное сечение (+), немногочисленные цилиндры в одиночных канальцах, Lambda — выраженное свечение (+++), многочисленные ярко флуоресцирующие цилиндры в большом количестве канальцев.
Электронная микроскопия: толщина и ультраструктура базальных мембран капилляров в пределах нормы, депозиты не обнаружены, в интерстиции выявлена обильная инфильтрация лимфоидными элементами, в просвете канальцев белковое содержимое.
Заключение по данным исследования почечного биоптата: морфологическая картина может наблюдаться при каст-нефропатии (цилиндровой нефропатии) при плазмоклеточной дискразии, болезни отложения легких цепей, В-клеточной лимфоме, также отмечается терминальный нефросклероз с атрофией более 70% канальцев, гипертензивная ангиопатия.
На рисунке 1 представлены результаты морфологического анализа нефробиоптата.
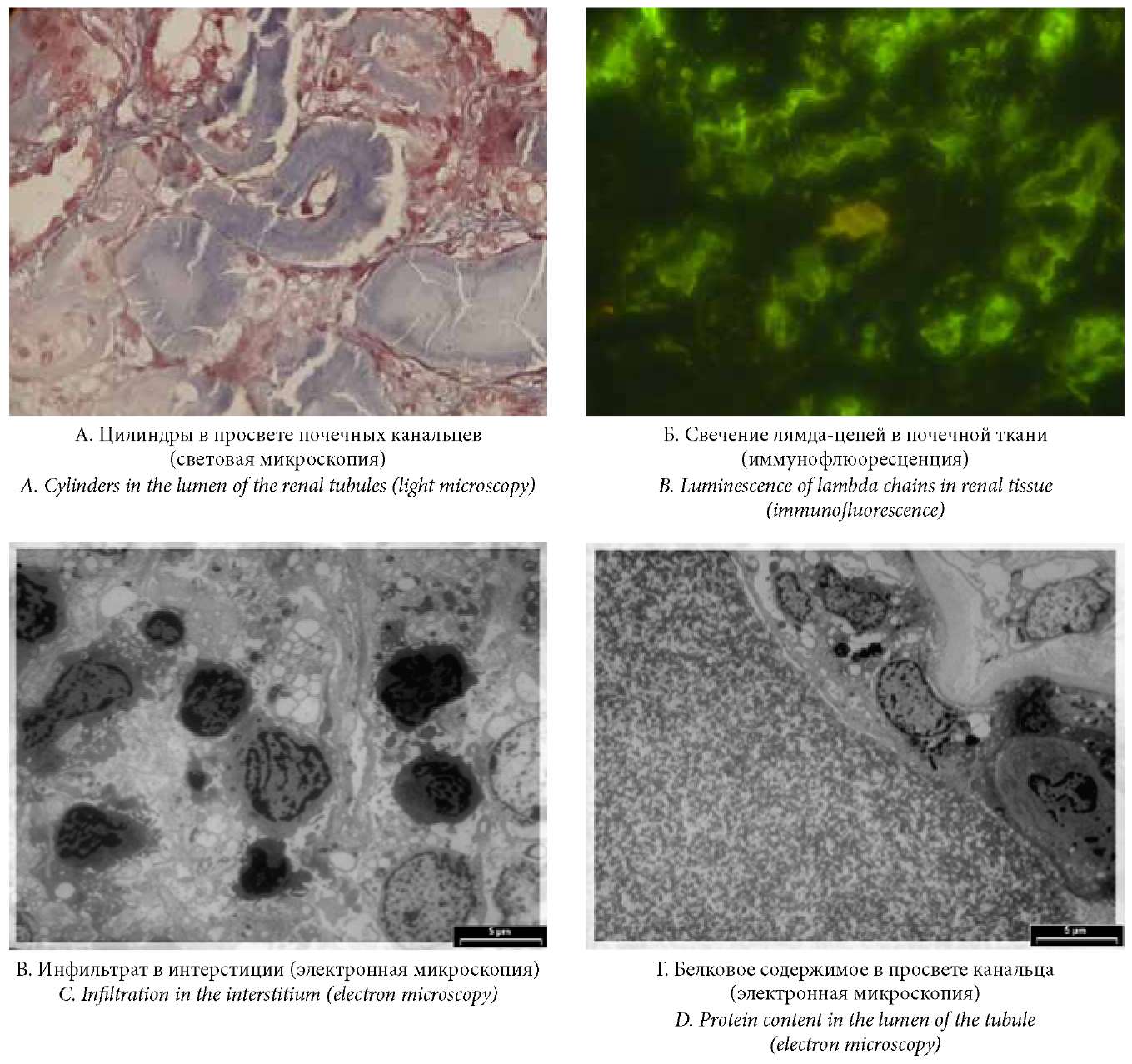
Рисунок 1. Результаты морфологического анализа нефробиоптата (изображение авторов)
Figure 1. Results of morphological analysis of nephrobiopsy specimen (Photograph of the authors)
Пациентка выписана из отделения гемодиализа с диагнозом “Цилиндровая-нефропатия (нефробиопсия от 19.12.2018 г.). Острое повреждение почек 3 стадии, ренальное с трансформацией в ХБП 5Д стадию. Заместительная почечная терапия (лечение программным гемодиализом). Артериальная гипертензия 3 стадии, медикаментозно контролируемая АГ, риск 4 (очень высокий)».
В течение данной госпитализацию выяснить причину развития повреждения почек не удалось, рекомендована антигипертензивная терапия с продолжением выполнения процедур программного гемодиализа.
Повторный электрофорез белков сыворотки от 11.01.2019 г.: общий белок — 58г/л, альбумин — 37 г/л, альфа 1 — 5,66%; альфа 2 — 9,17%; бета 1 — 4,75%; бета 2 — 4,45%; гамма-глобулин — 14,58%. На электрофореграмме методом иммунотипирования обнаружен патологический белок в виде легких цепей лямбда.
При рентгенологическом исследовании костей черепа и грудной клетки от 10.01.2019 г. очаговых и деструктивных изменений не определялось.
При выполнении стернальной пункции было установлено следующее: костный мозг выглядел нормоклеточным, миелоидный росток угнетен, лимфоцитов было 3,4%, плазматических клеток — 7,4% эритроидный росток расширен, с дисплазией: двухядерные межклеточные мостики, эритропоэз по нормобластическому типу, мегакариоциты с отшнуровкой тромбоцитов.
При проведении трепатобиопсии крала подвздошной кости установлено 15% плазматических клеток.
Окончательный клинический диагноз — «Множественная миелома IIIВ стадия. Осложнение: цилиндровая-нефропатия (нефробиопсия от 19.12.2018 г.). Острое повреждение почек 3-е стадии, ренальное с трансформацией в ХБП 5Д стадию. Заместительная почечная терапия (лечение программным гемодиализом). Сопутствующее: артериальная гипертензия 3 стадии, медикаментозно контролируемая АГ, риск 4 (очень высокий)».
Обсуждение
Особенностью данного клинического случая является то, что первым проявлением множественной миеломы явилось ОПП, послужившее основанием для выполнения биопсии почки. При этом отмечалось отсутствие каких-либо патологических изменений в анализах мочи, нормальный и даже сниженный уровень общего белка крови, отсутствие очагов деструкции в костях свода черепа. Объяснением такого атипичного течения миеломной болезни следует считать быстрый прирост синтеза парапротеинов опухолевым клоном сравнительно небольших размеров с крайне высокой степенью их нефротоксичности и способности к агглютинации в канальцевом пространстве с развитием его обструкции.
В отечественной и зарубежной литературе описаны случаи дебюта миеломной болезни в виде цилиндровой нефропатии с ОПП, однако в большинстве описаний наблюдется патологический мочевой осадок и признаки гаммапатии по данным электрофереграмм с иммунотипированием [8]. В нашем случае мочевой осадок был нормальным и первое исследование электрофореграммы не дало положительного результата в отношении верификации гаммапатии, что существенно осложнило нозологическую верификацию почечного процесса.
Отсутствие исходно протеинурии, а дебют в виде ОПП требует пояснений, включающих в себя рассмотрение возможных патогенетических особенностей поражения почек у данного пациента. Поскольку морфологически наличие цилиндровой нефропатии было доказано, то отсутствие протеинурии в дебюте поражения почек, вероятно, объясняется молниеносным поражением органа, но с превалированием на начальном этапе вазо- и тубулотоксических эффектов парапротеинов над обструктивными вследствие цилиндровой бострукции, которые присоединились позже.
Парапротеины при миеломной болезни в ряде случаев обладают крайне выраженными токсическими свойствами, как в отношении почечной микрососудистой сети, так и канальцев [9][10]. Лёгкие цепи вызывают воспаление с привлечением лейкоцитов, высвобождением активных форм кислорода и цитокинов, способны активировать процессы аутофагии и апоптоза с развитием канальцевого некроза [5].
При проведении нефробиопсии у нашего пациента была обнаружена атрофия эпителия 70–90% канальцев с явлениями гидропической дистрофии в оставшемся эпителии, что является морфологическим подтверждением агрессии парапротеинов в отношении канальцевого эпителия. И последующая трансформация ОПП в ХБП С5Д явилась конечным результатом такого необратимого воздействия на канальцевый эпителий [11].
Ещё одной особенностью описанного клинического случая явилось отсутствие признаков накопления парапротеина по данным электрофореза белков крови и мочи при первом обследовании и появление их уже в последующем. По данным литературы, при впервые выявленной миеломной болезни вероятность обнаружения признаков накопления парапротеинов в крови составляет примерно 91,5% [12]. Отсутствие наглядного диагностически чувствительного накопления парапротеина у нашего пациента свидетельствует о его крайне выраженной нефротоксичности, которая объясняет поражение почек уже на ранних стадиях гиперсекреции парапротеина. Явления ОПП в дебюте миеломной болезни наблюдаются примерно в 16,6% случаев и, как правило, свидетельствуют о неблагопритной почечном прогнозе течения болезни, а в качестве объяснения данному феномену случит высокая нефротоксичность парапротеинов у данной категории пациентов [13].
Заключение
Таким образом, представленный клинический случай редкого дебюта миеломной болезни демонстрирует вариабельность течения внекостных поражений при данном заболевании, а также особенности вовлечения почечной ткани в процесс. В частности, классический вариант цилиндровой нефропатии в данном случае был маскирован отсутствием патологических изменений в моче и признаков накопления парапротеина в крови, что свидетельствует в выраженной нефротоксичности парапротеина у данного пациента и стремительности развития событий в отношении почечного повреждения.
Список литературы
1. Захарова Е. В., Зыкова А. С., Макарова Т. А., Леонова Е.С., Никитина Е.Н. и др. Моноклональные гаммапатии почечного значения и парапротеинемические поражения почек при злокачественных лимфопролиферативных заболеваниях – клинико-морфологическая характеристика 197 пациентов одного центра. Нефрология и диализ. 2024;26(1):55-70. DOI: 10.28996/2618-9801-2024-1-55-70.
2. Храброва М.С., Добронравов В.А., Смирнов А.В. Поражения почек, ассоциированные с моноклональными гаммапатиями: одноцентровое исследование. Нефрология. 2018;22(6):38-46. DOI: 10.24884/1561-6274-2018-22-6-38-46
3. Смирнов А.В., Афанасьев Б.В., Поддубная И.В., Добронравов В.А., Храброва М.С. и др. Моноклональная гаммапатия ренального значения: консенсус гематологов и нефрологов России по введению нозологии, диагностике и обоснованности клон-ориентированной терапии. Нефрология. 2019;23(6):9-28. DOI: 10.36485/1561-6274-2019-23-6-9-28
4. Рехтина И.Г., Голицина Е.П., Варламова Е.Ю., Варшавский В.А., Киреева А.А. и др. Морфологические и иммунохимические особенности нефропатий при множественной миеломе с тяжелой почечной недостаточностью. Терапевтический архив. 2013;85(3):80 85.
5. Mene P, Stoppacciaro A, Lai S, Festuccia F. Light Chain Cast Nephropathy in Multiple Myeloma: Prevalence, Impact and Management Challenges. Int J Nephrol Renovasc Dis. 2022;15:173-183. DOI: 10.2147/IJNRD.S280179.
6. Thajudeen B, Rubin MF. Hemodynamic acute kidney injury in immunoglobulin A nephropathy: nephrosarca theory revisited. Am J Med. 2013;126(12):e13–4. DOI: 10.1016/j.amjmed.2013.07.033.
7. Oyama Y, Iwafuchi Y, Morioka T, Narita I. Acute kidney injury associated with minimal change nephrotic syndrome in an elderly patient successfully treated with both fluid management and specific therapy based on kidney biopsy findings. Case Rep Nephrol Dial. 2020;10(1):42–50. DOI: 10.1159/000507426
8. Бородина Л.В., С.А. Козакова, Рыбас А.В. Случай миеломной болезни, дебютировавшей острым повреждением почек. Терапия. 2024;10(S1,73):36.
9. Рехтина И.Г., Казарина Е.В., Столяревич Е.С., Двирнык В.Н., Куликов С.М., Менделеева Л.П. Прогностическое значение фиброза интерстиция в нефробиоптате в обратимости острого почечного повреждения при цилиндровой нефропатии у пациентов с множественной миеломой. Нефрология и диализ. 2019;21(3):312-319. DOI: 10.28996/2618-9801-2019-3-312-319.
10. Sanders PW. Mechanisms of light chain injury along the tubular nephron. J Am Soc Nephrol. 2012;23(11):1777–1781. DOI: 10.1681/asn.2012040388.
11. Ying WZ, Wang PX, Aaron KJ, Basnayake K, Sanders PW. Immunoglobulin light chains activate nuclear factor κB in renal epithelial cells through a Src-dependent mechanism. Blood. 2011;117(4):1301–1307. DOI: 10.1182/blood-2010-08-302505.
12. Li L, Han C, Yu X, Cai Y, Cao Y, et al. Experimental Characteristics of Patients with Newly Diagnosed Multiple Myeloma. Altern Ther Health Med. 2023;29(8):529-533.
13. Liu X, Hu Q, Zheng Y, Tang W, Niu T. Incidence, Clinical Features, and Prognostic Value of New-Onset Renal Impairment in Multiple Myeloma. Cancer Med. 2025;14(21):e71361. DOI: 10.1002/cam4.71361.
Об авторах
М. М. БатюшинРоссия
Батюшин Михаил Михайлович, д.м.н., профессор, профессор кафедры внутренних болезней №2
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
И. Н. Нестеренко
Россия
Нестеренко Ирина Николаевна, врач-нефролог, Ростовская областная клиническая больница, ассистент кафедры реконструктивной, сердечно-сосудистой, торакальной, челюстно-лицевой хирургии и трансплантологии
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Т. П. Белобородова
Россия
Белобородова Татьяна Петровна, врач-нефролог отделения, хронического гемодиализа
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Н. Б. Страхова
Россия
Страхова Наталья Борисовна, заведующий отделением хронического гемодиализа
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Е. С. Левицкая
Россия
Левицкая Екатерина Сергеевна, д.м.н., доцент, заведующий кафедрой медицинской реабилитации, профессор кафедры внутренних болезней № 2
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Рецензия
Для цитирования:
Батюшин М.М., Нестеренко И.Н., Белобородова Т.П., Страхова Н.Б., Левицкая Е.С. Редкий дебют миеломной болезни в виде острого повреждения почек. Медицинский вестник Юга России. 2026;17(1):5-10. https://doi.org/10.21886/2219-8075-2026-17-1-5-10
For citation:
Batiushin M.M., Nesterenko I.N., Beloborodova T.P., Strakhova N.B., Levitskaya E.S. Rare onset of myeloma disease in the form of acute kidney injury. Medical Herald of the South of Russia. 2026;17(1):5-10. (In Russ.) https://doi.org/10.21886/2219-8075-2026-17-1-5-10
JATS XML







































