Перейти к:
Клинико-иммунологические аспекты первой атаки рассеянного склероза (клинически изолированный синдром)
https://doi.org/10.21886/2219-8075-2026-17-1-87-96
Аннотация
Цель: выявление клинических и иммунологических предикторов ранней конверсии у пациентов с клинически изолированным синдромом (КИС). Материалы и методы: анализ медицинской документации и лабораторных данных 320 пациентов, обработка данных одно- и двухфакторный дисперсионный анализ (ANOVA), непараметрический критерий c2 (хи-квадрат), параметрический и непараметрический (Спирмена) корреляционный анализ, ранговый критерий Манна — Уитни. Результаты: возраста дебюта — 13–71 год, средний — 36,4±8 лет; Me=36 лет. У 60 пациентов (18,7 %) дебют в возрасте 50 лет и старше. Полифокальный дебют выявлен у 84,4%, у большинства пациентов конверсия наступала через 12 месяцев и более. Во врождённом иммунитете увеличение CD16+Gr+, % 7,8 [5,2;9,1], CD14+289+ 12 [4;20], инверсия НСТ-теста 155 [139;171] (р < 0,05). В адаптивном иммунитете — повышение CD3+HLA DR+,% 3 [2;5,4], CD8+Gr+20 [15;27], CD19+, %9 [7;12], увеличение ЦИК, у. е. 60 [47;84] (р < 0,05) снижение CD4+CD25+, % 1,3 [1,0;2,2], CD19+CD5+, %0,6 [0,3;0,9] (р < 0,05). Выявлены широкие граница возраста дебюта, с тенденцией к повышению среднего возраста, с преобладанием полифокального варианта. Во врождённом иммунитете повышение моноцитов, экспрессирующих CD14+289+, с уменьшением способности к антибактериальной защите, снижение активационной способности моноцитов, повышение цитотоксических функций натуральных киллеров, снижение адаптационных резервов нейтрофильного звена с инверсией коэффициента НСТ-теста. Изменения адаптивного иммунитета приводят к инверсии иммуно-регуляторного индекса (увеличения клеток с цитотоксическим эффектом, нарушению соотношения В1/В2 лимфоцитов и их дискоординации). В гуморальном звене дискоординация процессов антителогенеза. Выводы: выявлены клинические и иммунологические маркеры ранней конверсии КИС в рассеянный склероз.
Ключевые слова
Для цитирования:
Сизякина Л.П., Гончарова З.А., Ярош Н.М., Маркова Е.А. Клинико-иммунологические аспекты первой атаки рассеянного склероза (клинически изолированный синдром). Медицинский вестник Юга России. 2026;17(1):87-96. https://doi.org/10.21886/2219-8075-2026-17-1-87-96
For citation:
Sizyakina L.P., Goncharova Z.A., Yarosh N.M., Markova E.A. Clinical and immunological aspects of the first attack of multiple sclerosis (clinically isolated syndrome). Medical Herald of the South of Russia. 2026;17(1):87-96. (In Russ.) https://doi.org/10.21886/2219-8075-2026-17-1-87-96
Введение
Рассеянный склероз (РС) в настоящее время является хроническим аутоиммунным заболеванием, социальная значимость которого обусловлена страданием лиц молодого возраста, и клинически проявляется рецидивами с последующими ремиссиями и/или прогрессированием неврологической симптоматики [1].
Согласно Всемирной эпидемиологической базе данных больных РС (Atlas MS, 2023 г.) число людей, живущих с заболеванием, достигло в 2023 г. 2,9 млн человек. Большинство заболевает в возрасте от 20 до 50 лет, хотя РС также встречается у детей и лиц старших возрастных групп [1].
Этиология и патогенез заболевания многообразны и представляют собой неиссякающий интерес для исследователей во многих областях медицинских знаний [2]. Дискуссионный уровень выявления причин развития РС является следствием не полностью изученных клинико-иммунологических характеристик различных фенотипов заболевания. Многие исследования направлены на поиск новых биомаркеров и предикторов течения аутоиммунных заболеваний [3][4].
При этом иммунологические механизмы формирования различных фенотипов при первой атаке демиелинизирующего заболевания — клинически изолированного синдрома (КИС) —практически не определены, а их изучение может также внести существенный вклад как в оптимизацию диагностики, прогнозирования конверсии КИС в РС, а так и в повышение эффективности проводимой терапии.
У 85% пациентов заболевание начинается с КИС [5]. Данные литературы о времени до перехода из КИС в РС существенно различаются. Одни авторы указывают на достаточно короткий промежуток времени до конверсии в РС (в среднем 11 месяцев) [6], другие — на временной промежуток 2 –3 года [7]. По данным Brownlee W.J. [8], при среднем сроке наблюдения более 5 лет только 45% пациентов с КИС трансформируется в РС.
Для установки диагноза используются критерии McDonald W.I. (2017, 2024), основной концепцией которых является доказательство диссеминации симптомов в пространстве и во времени [5]. Критерии включают неврологическое обследование пациентов, наличие олигоклональных полос (ОКП) в ликворе, магнитно-резонансную томографию (МРТ), а также проведение дифференциально-диагностического поиска для исключения других заболеваний.
В ряде клинических исследований показано, что применение препаратов, изменяющих течение РС, у пациентов с КИС замедляет развитие когнитивного дефицита при РС [9]. Для пациентов с КИС прогноз течения заболевания и скорости конверсии значительно вариабелен и трудно предсказуем.
Исследование первого клинического эпизода демиелинизации актуально для определения тактики ведения пациентов, выявления фенотипов с риском быстрой трансформации в РС. Комплексный анализ биомаркеров, предикторов течения, является основополагающим для изучения РС, позволяя выделить основные фенотипы и возможность прогнозирования развития заболевания. Поиск информативных и доступных иммунологических маркеров может помочь в идентификации предикторов быстрой конверсии КИС в РС.
В патогенезе РС играют роль как врождённый, так и адаптивный иммунные ответы. Иммунологические особенности КИС включают активацию иммунной системы и воспалительные процессы в ЦНС [10–12]. Это может проявляться в повышенном уровне воспалительных маркеров и аутоантител в крови и/или спинномозговой жидкости пациента. Однако их наличие у больных с КИС, особенности врожденного и адаптивного иммунитета, обусловливающие степень формирования аутоиммунного процесса, скорость конверсии в РС, варианты течения (моно- и полифокальный), практически не выявлены, а имеющиеся данные противоречивы, во многом носят дискуссионный характер [6][13], в связи с этим была поставлена цель выявление клинических и иммунологических аспектов клинически изолированного синдрома.
Материалы и методы
Настоящее проспективное лонгитудинальное исследование проводилось с сентября 2014 г. по январь 2023 г. на базе ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России. Применение методов исследования было представлено и одобрено на заседании ЛНЭК ФГБОУ ВО РостГМУ МЗ России № 13/14 от 11.09.2014 г. Исследование проведено в соответствии с международными стандартами GCP.
На первом этапе проведен анализ результатов исследований когорты пациентов (432 больных) с единичным эпизодом неврологической симптоматики («Клинически изолированный синдром»).
Критерии включения: наличие неврологической симптоматики (поражение головного и/или спинного мозга), характерной и/или не исключающей РС. Длительность симптоматики — не менее 24 часов. Критерии исключения — наличие признаков лихорадки или инфекции, признаки энцефалопатии.
По результатам анализа историй болезни был проведён второй этап исследования, в который были включены 320 больных с диагнозом «Клинически изолированный синдром», обследованных в клинике РостГМУ.
Клинический метод включал сбор жалоб, анамнеза заболевания и катамнеза, наличие/отсутствие сопутствующей патологии, исследование неврологического статуса по шкалам EDSS и FS. Все пациенты (100%) лично осмотрены автором. Ретроспективно оценивались амбулаторные карты и выписки из историй болезни стационарных больных (архивный метод).
Лабораторные методы исследования состояли из общеклинического анализа крови, биохимического анализа крови (определение трансаминаз, общего белка, креатинина, мочевины, общего билирубина, коагулограммы, СРБ), общего анализа мочи и анализа по Нечипоренко, общего и биохимического анализа (включающий определение глюкозы и хлоридов) ликвора.
Нейровизуализационное исследование включало оценку результатов МРТ головного и спинного (по показаниям) мозга на высокопольных аппаратах с индукцией постоянного поля (аппаратах «Tomikon S50 Avance» («Bruker» Германия), «Signa HDx» («GE Healthcare», США) и «Achieva» с индукцией постоянного поляPilips Ingenia 1,5 и 3,0 Тл).
Иммунологические методы осуществлялись с помощью мультипараметрической многоцветной проточной цитофлюориметрии (Т-лимфоциты (CD3⁺ клетки, их CD4⁺ и CD8+⁺ субпопуляции), CD3⁺HLA DR, CD4⁺HLA DR, CD3⁺25⁺, CD8⁺Gr⁺), В-лимфоциты(CD19⁺), CD19⁺CD5⁺, CD16⁺, CD16⁺Gr⁺, CD4⁺CD25⁺, CD14⁺282⁺, CD14⁺284⁺, CD14⁺ 289⁺, CD14⁺ HLA DR⁺, NBТ-тест (НСТ-тест спонтанный, у.е., НСТ-тест стимулированный, у.е., коэффициентстимуляции, ед.), селективной преципитации (ЦИК у.е.), определение олигоклональных IgG в сыворотке и ликворе методом изоэлектрофокусирующего электрофореза с иммуноблоттингом.
Статистические методы были выполнены с использованием программы STATISTICA 12.0 (2014), программы MS Exсel, одно- и двухфакторного дисперсионного анализа (ANOVA), непараметрического критерия χ² (хи-квадрат), параметрического и непараметрического (Спирмена) корреляционного анализа, рангового критерия Манна-Уитни. Расчёты выполнялись в R Foundation for Statistical Computing (версия 3.2, Vienna, Austria).
Результаты
С учётом наличия объективных и субъективных причин, затрудняющих раннюю диагностику и необходимости своевременного определения долгосрочного прогноза, сохраняется актуальность изучения клинической картины дебюта РС. Мы проанализировали динамику клинического течения заболевания в течение 8 лет с акцентом на симптомы дебюта и оценку показателей иммунологического профиля сыворотки крови, характеризующих состояние врождённого и адаптивного звеньев иммунной системы.
В группу исследования включены 320 человек обоих полов в возрасте от 13 лет до 71 года с различными фенотипами КИС. Среди пациентов преобладали женщины (р < 0,0001) (n=201). Мужчины составили 119 человек. Соотношение мужчин и женщин — 1:1,7 (соответственно 36,8 % и 63,1%), как представлено на рисунке 1, что отличается от соотношения больных при РС (1:2, 1:3)

Рисунок 1. Распределение пациентов по полу. На рисунке отмечено процентное соотношение, женщины — 63%, мужчины — 37% (составлено авторами)
Figure 1. Distribution of patients by gender. The figure shows the percentage: women — 63%, men — 37% (complied by the authors)
Данный факт, по нашему мнению, объясняется более мягким течением заболевания и (вследствие этого) низкой обращаемостью и приверженностью обследования у женщин. Подтверждением могут служить данные, полученные ранее в популяции Ростовской области [14]. Интервал дебют-диагноз у мужчин (3,1 ± 0,7 года) меньше, чем у женщин (4,0±0,7 года), таким образом диагноз “РС” мужчинам верифицировался раньше (р<0,05). Возраст дебюта заболевания варьировался в широких границах (13–71 год), средний возраст дебюта в общей группе больных с КИС оказался достаточно высоким (±SD=36.4 ± 8 лет; Me=36 лет). В исследованиях предыдущих лет [14][15] возраст дебюта был достоверно меньше, что коррелирует с данными литературы [16][17]. Средний возраст дебюта — 36,4±8 лет (Me=36 лет). Минимальный возраст начала заболевания — 13 лет, самый поздний — 71 год. Только у 71,3% пациентов первые симптомы РС появились в типичном для РС возрасте от 18 до 50 лет (рис. 2). Распределение пациентов по возрасту дебюта было асимметричным со смещением в сторону средних возрастных категорий с двумя пиковыми возрастными периодами (15–20 и 30–40 лет), являющимися характерными для РС. У 28,7% больных заболевание началось в детском (до 18 лет) возрасте или в 50 лет и старше (поздний дебют), что отражает общемировую тенденцию о расширении возрастных границ РС в последние годы [18][19].
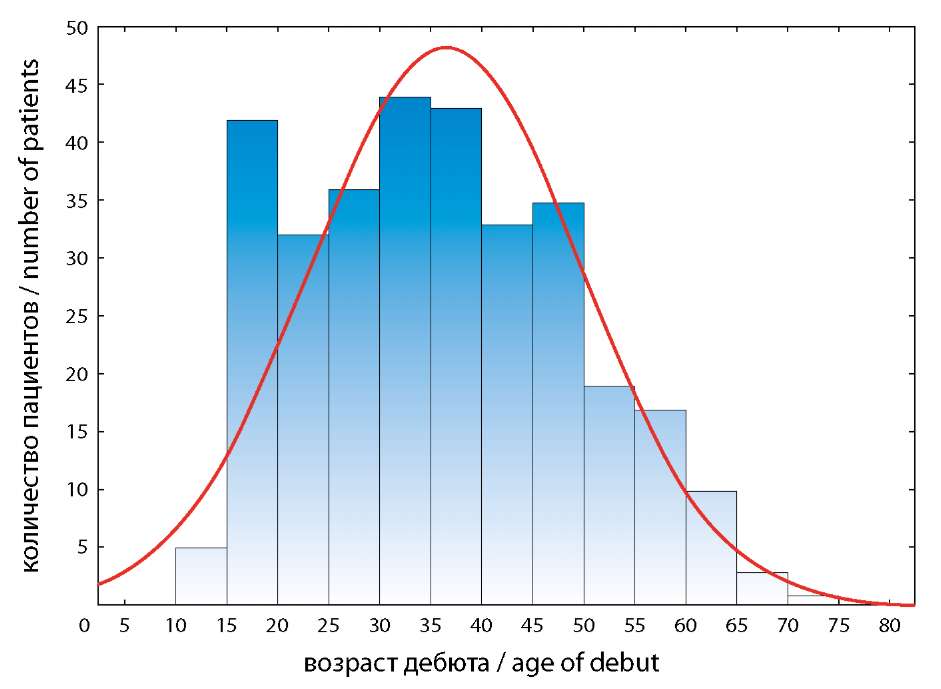
Рисунок 2. Распределение пациентов по возрасту дебюта заболевания (составлено авторами)
Figure 2. Distribution of patients by age of disease onset (complied by the authors)
Особое внимание привлекла подгруппа с первично-прогрессирующим РС (60 пациентов, 18,7% общей группы) в связи со значительным ростом заболеваемости в данной возрастной группе в последнее десятилетие. Эпидемиологическое исследование в популяции Ростовской области 2013 г. [15] выявило всего 1% больных с первично-прогрессирующим РС. С учётом имеющихся в литературе данных о худшем прогнозе в данной подгруппе и особенностях выбора патогенетической терапии данный фенотип представляет особый интерес особенно с точки зрения изучения иммунопатегенеза.
Сравнительный анализ клинико-демографических характеристик больных с КИС выявил полифокальный вариант дебюта РС, считающийся неблагоприятным фактором долгосрочного прогноза, у подавляющего большинства пациентов (84,4 %). Вероятно, пациенты с легче протекающим монофокальным дебютом (15,6%) реже обращаются к неврологу на стадии КИС. В анализируемой когорте преобладали пациенты с активным КИС (78,2 n = 250), неактивный вариант КИС зарегистрирован у 21,3 % (70 пациентов).
Известно, что раннее наступление конверсии хуже для прогноза заболевания с учётом этого больные были разделены на 3 группы в зависимости от скорости конверсии. У 37,8 % (121 пациент) обследуемых конверсия наступила в течение 12 месяцев, у 55,3 % (177 пациентов) скорость конверсии в РС составила12 месяцев и более, у 22 пациентов (6,8 %) по настоящее время конверсия заболевания не наступила.
Изученные клинико-демографические данные выявили особенности клинической картины в виде преобладания симптомов поражения ствола мозга и пирамидной системы у мужчин, у женщин преобладали мозжечковые нарушения и атипичные симптомы дебюта заболевания. Конверсия в РС у мужчин наступает быстрее (11,7 ± 8,2 месяца), чем у женщин (13,2 ± 8,1 месяцев) (р < 0,05).
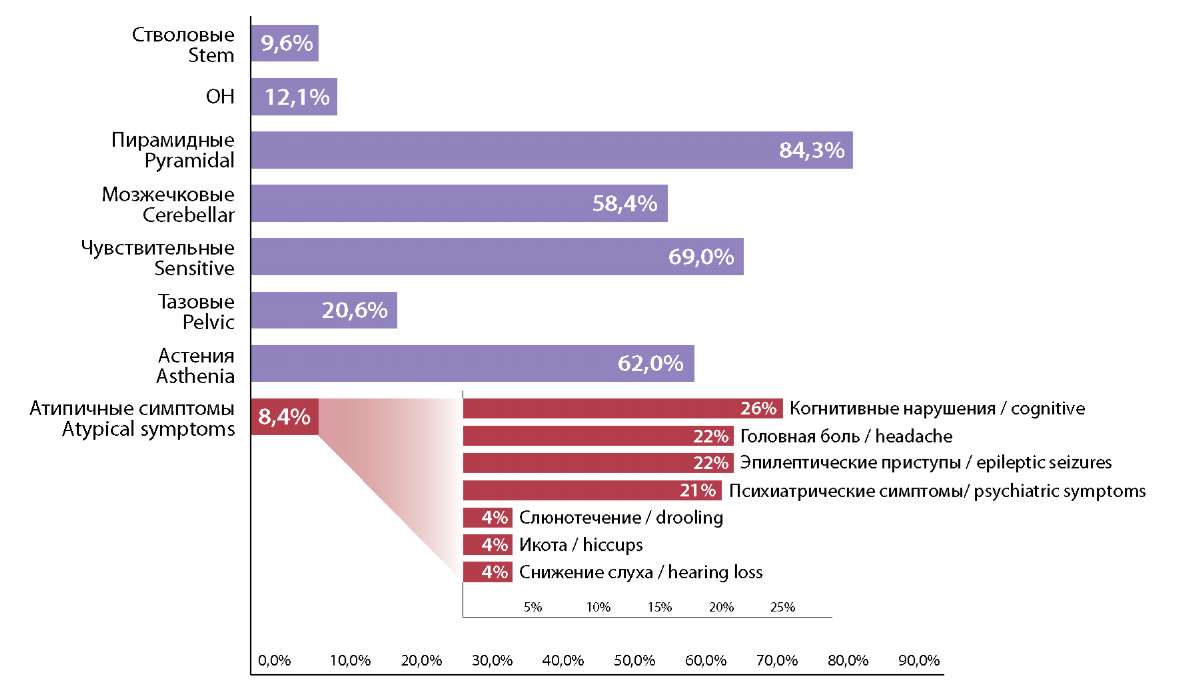
Рисунок 3. Частота встречаемости симптомов дебюта у больных с КИС (составлено авторами)
Figure 3. Frequency of occurrence of symptoms at onset in patients with CIS (complied by the authors)
Обращает внимание частая встречаемость астенического синдрома — 62 % (168 больных с КИС). Астенический синдром чаще регистрировали у мужчин (57% случаев), чем у женщин (49,7 %) (р < 0,05). Данный симптом в последние годы активно изучается, встречается у 90 % больных с РС [20][21]. С учётом полученных нами данных астенический синдром является ранним проявлением заболевания уже на стадии дебюта, изучение его патофизиологии представляет интерес, так как исключает такие потенциально значимые триггерные факторы, как нейродегенерация и влияние препаратов, изменяющих течение РС.
«Атипичный» дебют (головная боль, астения, депрессия тревога, диссомния) зарегистрирован нами у 27 больных с КИС (8,4%). С появлением концепции продромального периода заболевания данные симптомы рассматриваются как важные ранние признаки, возникающие за много лет до развития типичных признаков демиелинизации [21], являются подтверждением гипотезы, что патофизиологические процессы в ЦНС начинаются задолго до развития клинической манифестации [11]. Средний балл EDSS составил 2,6±1,0 балла.
С целью выявления особенностей иммунного статуса у больных с КИС, предикторов конверсии КИС в РС (как возможных биомаркеров прогноза заболевания), нами проанализированы показатели врождённого и приобретённого иммунитетов у пациентов с КИС.
Таблица / Table 1
Показатели врождённого иммунитета у пациентов с КИС (M±SD, ME+[LQ;UQ]) (составлено авторами)
Innate immunity parameters in patients with CIS (M±SD, ME+[LQ;UQ]) (complied by the authors)
Пациенты с КИС Patients with CIS (n=65) | Здоровые доноры Healthy donors (n=50) | Р-критерий P-test | |
CD16⁺, % | 10 [ 7;15] | 11 [ 10;15] | р > 0,05 |
CD16⁺×10⁹/л CD16⁺×10⁹/l | 0,17 [ 0,02; 0,2] | 0,2 [ 0,05; 0,3] | |
CD16⁺Gr⁺, % | 7,8 [ 5,2;9,1] | 5 [ 3;9] | р < 0,05 |
CD16⁺Gr⁺×10⁹/л CD16⁺Gr⁺×10⁹/l | 0,14 [ 0,09;0,2] | 0,095 [ 0,06;0,14] | |
CD14⁺HLA DR⁺, % | 57 [ 46;80] | 72 [ 62;80] | р > 0,05 |
CD14⁺HLA DR⁺×10⁹/л CD14⁺HLA DR⁺×10⁹/l | 0,2 [ 0,08;0,3] | 0,28 [ 0,1;0,5] | |
CD14⁺ 282⁺, % | 0,5 [ 0,3;1,0] | 58[ 45;71] | р > 0,05 |
CD14⁺282⁺×10⁹/л CD14⁺282⁺×10⁹/l | 6,1 [ 4;10] | 0,7[ 0,5;1,1] | |
CD14⁺ 284⁺, % | 19 [ 5,3;42] | 40[ 36;45] | р > 0,05 |
CD14⁺284⁺×10⁹/л CD14⁺284⁺×10⁹/l | 0,03[ 0,06;0,1] | 0,041[ 0,03;0,08] | |
CD14⁺ 289⁺, % | 12 [ 4;20] | 8,6[ 6,9;11] | р < 0,05 |
CD14⁺289⁺×10⁹/л CD14⁺289⁺×10⁹/l | 0,9 [ 0,18;0,25] | 0,81 [ 0,16;0,2] | |
НСТ-тест спонтанный, у.е. NST spontaneous test, c.u. | 97 [ 83;108] | 95,1 [ 94;96,2] | р > 0,05 |
НСТ-тест стимулированный, у.е. NST-stimulated test, c.u. | 155 [ 139;171] | 166 [ 164;167,6] | р < 0,05 |
Коэффициент стимуляции, ед. Stimulation coefficient, units | 1,6 [ 1,5;1,7] | 1,75 [ 1,73;1,77] | р < 0,05 |
Из наиболее существенных изменений во врождённом иммунитете пациентов с первыми проявлениями демиелинизирующего заболевания следует отметить повышение содержания моноцитов, экспрессирующих CD14⁺289⁺подобные рецепторы, с уменьшением способности к антибактериальной защите, снижение активационной способности моноцитов, повышение цитотоксических функций натуральных киллеров, снижение адаптационных резервов нейтрофильного звена с инверсией коэффициента НСТ-теста.
Таблица / Table 2
Показатели адаптивного иммунитета у пациентов с КИС (M±SD, ME+[LQ;UQ]) (составлено авторами)
Adaptive immunity parameters in patients with CIS (M±SD, ME+[LQ;UQ]) (complied by the authors)
Пациенты с КИС Patients with CIS (n=65) | Здоровые доноры Healthy donors (n=50) | P-критерий P-test | |
CD3⁺,% | 76 [ 71;79] | 75 [ 72;77] | р > 0,05 |
CD3⁺×10⁹/л CD3⁺×10⁹/l | 0,25 [ 0,19;0,3] | 0,26 [ 0,18;0,3] | |
CD3⁺HLA DR⁺,% | 3 [ 2;5,4] | 1,25 [ 0,92;1,8] | р < 0,05 |
CD3⁺HLA DR⁺ ×10⁹/л CD3⁺HLA DR⁺ ×10⁹/l | 0,4 [ 0,2;0,6] | 0,3 [ 0,1;0,6] | |
CD4⁺,% | 46 [ 40;50] | 45 [ 38;47] | р > 0,05 |
CD4⁺ ×10⁹/л CD4⁺ ×10⁹/l | 1,08 [ 0,9;1,1] | 1,05 [ 0,9;1,1] | |
CD4⁺HLA DR⁺ ×10⁹/л CD4⁺HLA DR⁺ ×10⁹/l | 1,35 [ 0,98;2,23] | 1,3 [ 1,23;1,4] | р > 0,05 |
CD 4⁺HLA DR⁺ ×10⁹/л CD 4⁺HLA DR⁺ ×10⁹/l | 0,3 [ 0,25;0,71] | 0,3 [ 0,2;0,7] | |
CD4⁺CD25⁺, % | 1,3 [ 1,0;2,2] | 2,7 [ 2,3;3,5] | р < 0,05 |
CD4⁺CD25⁺ ×10⁹/л CD4⁺CD25⁺ ×10⁹/l | 0,25 [ 0,04-0,32] | 0,87 [ 0,043-0,3] | |
CD8⁺,% | 29 [ 26;34] | 24 [ 20;28] | р < 0,05 |
CD8⁺×10⁹/л CD8⁺×10⁹/l | 0,7 [ 0,5;0,8] | 0,6 [ 0,49;0,74] | |
CD8⁺Gr⁺ | 20 [ 15;27] | 13,5 [ 11.5;15,2] | р < 0,05 |
CD19⁺, % | 9 [ 7;12] | 7 [ 5;10] | р < 0,05 |
CD19⁺×10⁹/л CD19⁺×10⁹/l | 0,5 [ 0,4;0,51] | 0,41 [ 0,35;0,45] | |
CD19⁺CD5⁺, % | 0,6 [ 0,3;0,9] | 1,2 [ 0,9;1,4] | р < 0,05 |
CD19⁺CD5⁺×10⁹/л CD19⁺CD5⁺×10⁹/l | 0,09 [ 0,03;0,4] | 0,02 [ 0,01;0,3] | |
IgA г/л IgA g/l | 2,1 [ 1,8;2,29] | 1,7 [ 1,3;1,9] | р < 0,05 |
IgM г/л IgM g/l | 1,32 [ 1,15;1,51] | 1,1 [ 0,9;1,3] | р < 0,05 |
IgG г/л IgG g/l | 11,28 [ 10,6;12,1] | 11 [ 10;12] | р > 0,05 |
ЦИК у.е. CIC, u.e. | 60 [ 47;84] | 32 [ 26;59] | р < 0,05 |
Рассматривая динамику изменений показателей адаптивного иммунитета, мы должны отметить, что хотя процессы созревания Т-клеток практически не нарушены, статистически достоверно повышаются активационные способности (преимущественно поздней активации). Аналогичным образом при нормальном содержании Т-хелперов (CD4⁺) следует подчеркнуть их низкую способность к процессам ранней активации, в то же время поздняя активационная активность практически не изменена.
Наиболее существенные изменения — повышение CD8⁺ лимфоцитов, а также выраженное нарастание их цитотоксической активности — происходят в эффекторном звене иммунной системы. Выявленные изменения в соотношении клеток хелперного и эффекторного звеньев адаптивного иммунитета приводят к инверсии иммуно-регуляторного индекса в сторону увеличения клеток с цитотоксическим эффектом, нарушению соотношения В1/В2 лимфоцитов и их дискоординации. В гуморальном звене имеет место дискоординация процессов антителогенеза.
269 больным после клинического и соматического обследования было проведено ликворологическое обследование с определением олигоклональных полос (IgG) в ликворе. Первый тип синтеза (поликлональный) был выявлен у 117 человек (44%). Интервал «дебют-конверсия» в данной группе был максимальным и составил 25 месяцев.
У 117 человек (44%) был выявлен первый тип синтеза (поликлональный). Из них 50 мужчин (42,7%), 67 женщин (57,3%). Интервал «дебют-конверсия» в данной группе составил 25 месяцев.
У 148 больных (53%) определены второй и третий типы синтеза олигоклональных IgG, специфичные для РС и подтверждающие данный диагноз на момент исследования. В данной подгруппе был 51 мужчина (34,4%) (средний возраст — 34±11,5 г.) и 97 женщин (65,6%) (средний возраст — 35±12,6 л.). Соотношение мужчин к женщинам составило 1:1,7. У данных пациентов после верификации 2-го типа синтеза сразу подтверждена конверсия в РС.
Определение ОКП является доказательством перехода от КИС к ремиттирующему РС. На сегодняшний день определение ОКП позволяет диагностировать достоверный РС на этапе КИС, согласно критериям МсDonald W.I 2017.
Распределение типов синтеза олигоколональных IgG у всех пациентов представлено на рисунке 4 (n=269).
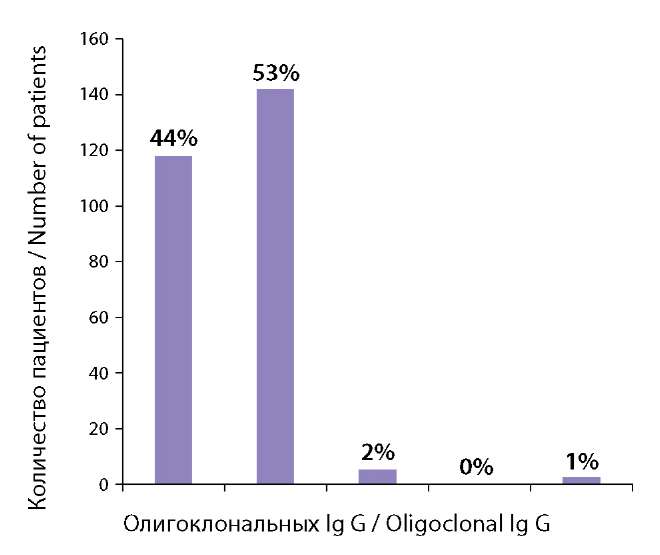
Рисунок 4. Распределение типов синтеза олигоклональныхIg G у всех пациентов (1.1 тип синтеза ОКП в ликворе; 2.2 тип синтеза ОКП в ликворе; 3.3 тип синтеза ОКП в ликворе; 4.4 тип синтеза ОКП в ликворе; 5.5 тип синтеза ОКП в ликворе (составлено авторами)
Figure 4. Distribution of the types of synthesis of oligoclonal Ig G in all patients (1. type 1 synthesis of OCP in cerebrospinal fluid; 2. type 2 synthesis of OCP in cerebrospinal fluid; 3. type 3 synthesis of OCP in cerebrospinal fluid; 4. type 4 synthesis of OCP in cerebrospinal fluid; 5. type 5 synthesis of OCP in cerebrospinal fluid (complied by the authors)
Установлено, что 2-й тип синтеза имел место более чем у половины пациентов с КИС (53%), что доказывает важность использования данного диагностического маркера для ранней диагностики РС. У 44% больных выявлен 1-й тип синтеза, не подтверждающий, но и не исключающий в последующем конверсию в РС. На остальные типы синтеза приходится около 3% пациентов. Доли олигоклональных IgG (1 тип синтеза) и олигоклональных IgG(2 тип синтеза) достоверно различаются (р < 0,05).
У большинства (53%) больных с КИС определён специфичный для РС и подтверждающий данный диагноз на момент исследования 2-й и 3-й типы синтеза олигоклональных IgG, что доказывает важность использования данного диагностического маркера для ранней диагностики РС. 2-й и 3-й типы синтеза олигоклональных IgG у женщин встречались чаще (у 48,2% по сравнению с 42,8% у мужчин, р < 0,05). 1-й тип синтеза чаще, чем 2-й, встречался у пациентов с оптическим невритом и симптомами, считающимися нехарактерными, редкими для РС (снижение слуха, эпилептические приступы, когнитивные и поведенческие нарушения). 2-й тип синтеза, определяющий у данных больных конверсию КИС, указывающий на высокую активность аутоиммунного процесса, наоборот, был ассоциирован с типичной для РС симптоматикой (пирамидная, мозжечковая, чувствительная и др.).
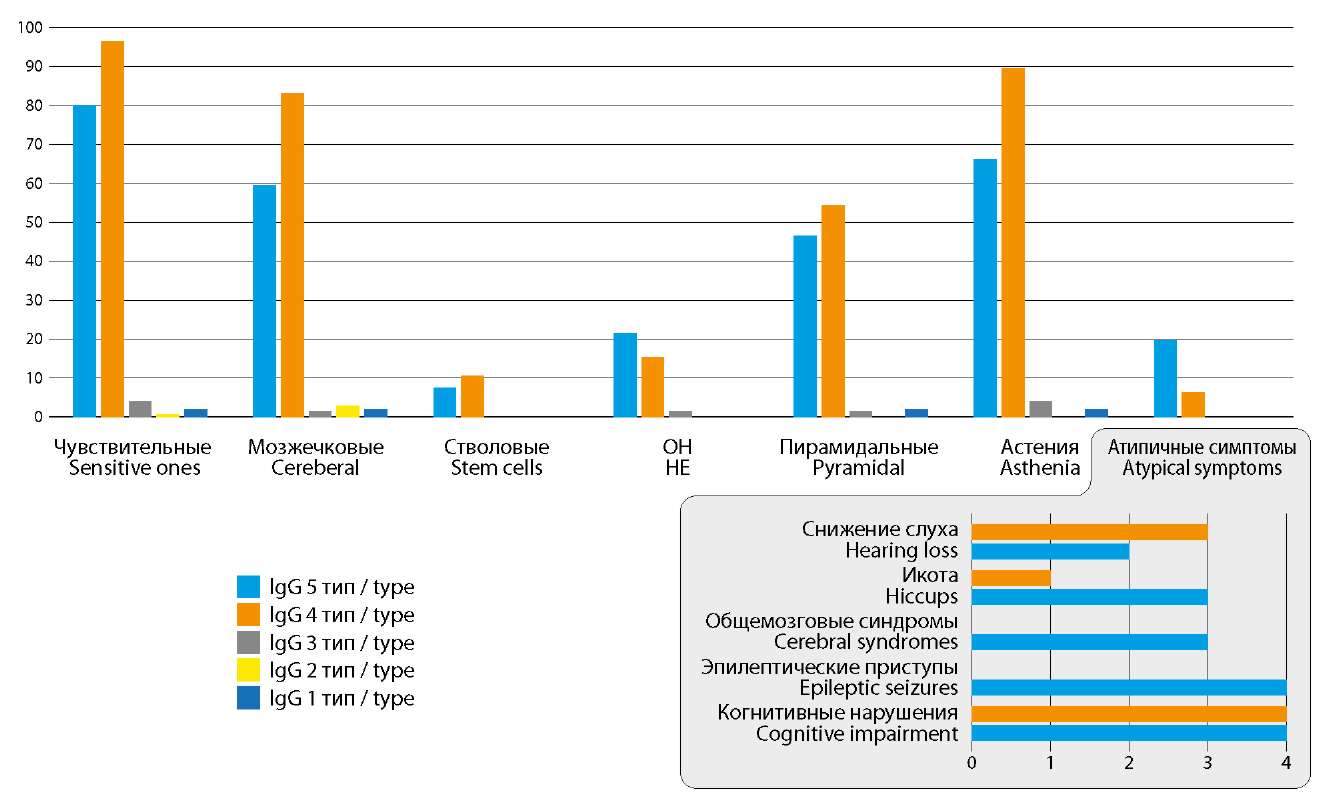
Рисунок 5. Распределение симптомов у пациентов с различными вариантами олигоклональных IgG (составлено авторами)
Figure 5. Distribution of symptoms in patients with different variants of oligoclonal IgG (complied by the authors)
На рис. 6 представлены данные о скорости конверсии у пациентов с различными типами синтеза ОКП в анализируемой когорте. Анализ Каплан-Майера демонстрирует вероятность конверсии в РС у пациентов с 1-м типом синтеза ОКП.
У 121 пациента второе обострение зарегистрировано в течение первого года от начала заболевания (37,8%). У 177 больных (55,3%) конверсия в РС произошла спустя более чем 1 год (12 мес. и более) от появления первых симптомов.

Рисунок 6. Вероятность конверсии КИС в РС у пациентов с различным типом синтеза (составлено авторами)
Figure 6. Probability of conversion of CIS to MS in patients with different types of synthesis (complied by the authors)
Несмотря на высокую специфичность и чувствительность ОКП, на сегодняшний день нет ни одного теста, который может со 100%-ми специфичностью и чувствительностью ответить на вопрос о том, имеется ли у больного с КИС конверсия в РС. Наличие атипичных форм РС, гетерогенность и коморбидность у пациентов определяют необходимость индивидуального подхода к каждому клиническому случаю с оценкой всех имеющихся данных (анамнеза заболевания и жизни, клинической картины, данных инструментальной, лабораторной диагностики). Особую значимость в данной ситуации приобретают, с нашей точки зрения, оценка иммунного статуса, оценка наличия герпесвирусной инфекции, ликворологическое обследование.
Обсуждение
Анализ клинико‑иммунологических характеристик пациентов с КИС выявил, что соотношение полов составляет 1: 1,7 (мужчины: женщины). Это является типичным и для рассеянного склероза, что соответствует общемировым данным, описанным в работах Гусева Е.И. и соавт., Klotz L. и соавт. [1][21].
В клинической картине дебюта преобладают пациенты с полифокальным вариантом начала заболевания (84,4% случаев), являющимся прогностически неблагоприятным фактором для долгосрочного прогноза РС, что коррелирует с данными Amato M.P. и соавт. [17]. Интервал «дебют-конверсия» у данных пациентов составил 12,6±7,2 месяца, средний балл по шкале EDSS составил 2,6±1,0 балла, что меньше, чем в исследовании Гончаровой З.А. и Погребновой Ю.Ю., что говорит о улучшении диагностики на этапе КИС [14][15].
Выявлены существенные изменения на ключевых этапах формирования иммунного ответа, включая процесс распознавания антигенов, созревание и дифференцировку иммунокомпетентных клеток, выраженную активацию эффекторного звена иммунной системы. Часть этих изменений была выявлена и в работе Liu R и соавт. [10].
Во врождённом иммунитете уже на стадии КИС определяются следующие значимые сдвиги в клеточном составе и активности: выраженное увеличение цитотоксической активности лимфоцитов; повышение количества моноцитов, экспрессирующих маркеры CD14⁺284⁺ и CD14⁺289⁺; усиление процессов поздней активации иммунных клеток; нарушение физиологического соотношения субпопуляций В1‑ и В2‑лимфоцитов.
При анализе динамики показателей адаптивного иммунитета можно отметить,что, несмотря на практически неизменённые процессы созревания Т‑клеток, наблюдается статистически достоверное повышение их активационных способностей преимущественно в фазе поздней активации.Схожая картина выявляется и в отношении Т‑хелперов: при их нормальном количественном содержании отмечается сниженная способность к ранней активации, тогда как показатели поздней активационной активности остаются практически неизменными, полученные нами результаты сопоставимы с данными, опубликованными в исследовании Afzali A.M. [12].
Таким образом, у пациентов с КИС наблюдается комплекс клинико‑иммунологических нарушений, затрагивающих как количественные, так и функциональные параметры иммунной системы уже на ранних стадиях заболевания.
Маркеры ранней конверсии клинически изолированного синдрома в рассеянный склероз:
- Клинические: полифокальный дебют с преобладанием пирамидной, мозжечковой симптоматики, тазовых нарушений, астенического синдрома; активный КИС.
- Нейровизуализационные: наличие очагов демиелинизации в спинном мозге, наличие рентгенконстрастных очагов.
Полученные данные согласуются с результатми Oh J. и соавт. [19]. Пол и возраст дебюта не влияют на скорость конверсии. В иммунной системе маркерами ранней конверсии является- увеличение моноцитов, экспрессирующих CD14⁺284⁺- CD14⁺289⁺-, CD8⁺-лимфоцитов и их цитотоксической активности, соотношения В1/В2 лимфоцитов, повышения антителогенеза IgA, IgM, ОКП в ликворе. Совокупность выявленных изменений выявлена впервые, согласно проведенному поиску литературы.
Выводы
Клинико‑иммунологические характеристики пациентов с КИС и маркеры его конверсии в рассеянный склероз
- В клинической картине КИС обнаруживаются гендерные различия, типичные и для РС (соотношение мужчин и женщин — 1:1,7 ). В 84,4% случаев отмечается полифокальный вариант начала болезни, что расценивается как прогностически неблагоприятный фактор в отношении долгосрочного прогноза РС, при этом интервал «дебют-конверсия» составил 12,6±7,2 месяца. Средний балл по шкале EDSS — 2,6±1,0 балла.
- У пациентов с КИС существенные отклонения наблюдаются на ключевых этапах формирования иммунного ответа и затрагивают как процессы распознавания антигенов, созревания и дифференцировки иммунокомпетентных клеток, так и активацию эффекторного звена иммунной системы. Во врождённом иммунитете выраженное повышение цитотоксической активности лимфоцитов; увеличение количества моноцитов, экспрессирующих маркеры CD14⁺284⁺ и CD14⁺289⁺; усиление процессов поздней активации иммунных клеток; нарушение физиологического соотношения субпопуляций В1 и В2 лимфоцитов.
- Маркерами ранней конверсии КИС в РС являются полифокальный дебют с преобладанием пирамидной симптоматики, мозжечковой симптоматики, тазовых нарушений, астенического синдрома, активный КИС, а также увеличение количества моноцитов, экспрессирующих CD14⁺284⁺-, CD14⁺289⁺-; CD8⁺-лимфоцитов (с повышением их цитотоксической активности), изменение соотношения субпопуляций В1/В2 лимфоцитов, повышение уровня: IgA; IgM, ОКП (олигоклональных комплексов) в ликворе.
Список литературы
1. Гусев Е.И., Демина Т.Л. Рассеянный склероз. Consilium Medicum. 2000;2(2):76-84. eLIBRARY ID: 27327186 EDN: XAAAID
2. Martinez B, Peplow PV. MicroRNAs in blood and cerebrospinal fluid as diagnostic biomarkers of multiple sclerosis and to monitor disease progression. Neural Regen Res. 2020;15(4):606-619. https://doi.org/10.4103/1673-5374.266905
3. Camara-Lemarroy CR, Silva C, Metz LM, Cerchiaro G, Greenfield J, et al. Multimodal peripheral fluid biomarker analysis in clinically isolated syndrome and early multiple sclerosis. Mult Scler Relat Disord. 2021;50:102809. https://doi.org/10.1016/j.msard.2021.102809
4. Nova A, Fazia T, Beecham A, Saddi V, Piras M, et al. Plasma Protein Levels Analysis in Multiple Sclerosis Sardinian Families Identified C9 and CYP24A1 as Candidate Biomarkers. Life (Basel). 2022;12(2):151. https://doi.org/10.3390/life12020151
5. Thompson AJ, Banwell BL, Barkhof F, Carroll WM, Coetzee T, et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol. 2018;17(2):162-173. https://doi.org/10.1016/S1474-4422(17)30470-2
6. Çinar BP, Özakbaş S. Prediction of Conversion from Clinically Isolated Syndrome to Multiple Sclerosis According to Baseline Characteristics: A Prospective Study. Noro Psikiyatr Ars. 2018;55(1):15-21. https://doi.org/10.29399/npa.12667
7. Gaetani L, Fanelli F, Riccucci I, Eusebi P, Sarchielli P, et al. High risk of early conversion to multiple sclerosis in clinically isolated syndromes with dissemination in space at baseline. J Neurol Sci. 2017;379:236-240. https://doi.org/10.1016/j.jns.2017.06.008
8. Brownlee WJ, Altmann DR, Alves Da Mota P, Swanton JK, Miszkiel KA, et al. Association of asymptomatic spinal cord lesions and atrophy with disability 5 years after a clinically isolated syndrome. Mult Scler. 2017;23(5):665-674. https://doi.org/10.1177/1352458516663034
9. Cree B, Timothy L. Clinically isolated syndrome: evaluation, risk stratification, and treatment decisions. Adv Stad Med. 2008;8(8):257-265.
10. Liu R, Du S, Zhao L, Jain S, Sahay K, et al. Autoreactive lymphocytes in multiple sclerosis: Pathogenesis and treatment target. Front Immunol. 2022;13:996469. https://doi.org/10.3389/fimmu.2022.996469
11. Britze J, Larsen MH, Pedersen AG, Rosthøj S, Bach Søndergaard H, et al. Temporal Dynamics of Plasma Neurofilament Light in Blood Donors With Preclinical Multiple Sclerosis. Neurol Neuroimmunol Neuroinflamm. 2025;12(1):e200335. https://doi.org/10.1212/NXI.0000000000200335
12. Afzali AM, Korn T. The role of the adaptive immune system in the initiation and persistence of multiple sclerosis. Semin Immunol. 2025;78:101947. https://doi.org/10.1016/j.smim.2025.101947
13. Jokubaitis VG, Spelman T, Kalincik T, Izquierdo G, Grand'Maison F, et al. Predictors of disability worsening in clinically isolated syndrome. Ann Clin Transl Neurol. 2015;2(5):479-491. https://doi.org/10.1002/acn3.187
14. Гончарова З.А., Погребнова Ю.Ю. Идиопатические воспалительные демиелинизирующие заболевания: оптимизация ранней диагностики, предикторы течения. Южно-Российский журнал терапевтической практики. 2021;2(2):80-87. https://doi.org/10.21886/2712-8156-2021-2-2-80-87
15. Бахтиярова К.З., Гончарова З.А. Рассеянный склероз в Республике Башкортостан и Ростовской области: сравнительная эпидемиологическая характеристика. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2014;114(2-2):5-9. eLIBRARY ID: 21369646 EDN: RZQLAP
16. Weinshenker BG, Bass B, Rice GP, Noseworthy J, Carriere W, et al. The natural history of multiple sclerosis: a geographically based study. 2. Predictive value of the early clinical course. Brain. 1989;112(Pt 6):1419-1428. https://doi.org/10.1093/brain/112.6.1419. PMID: 2597989.
17. Amato MP, Ponziani G. A prospective study on the prognosis of multiple sclerosis. Neurol Sci. 2000;21(4 Suppl 2):S831-8. https://doi.org/10.1007/s100720070021
18. Лащ Н.Ю., Павликов А.Е., Бойко А.Н. Развитие рассеянного склероза у лиц старше 50 лет. Журнал неврологии и психиатрии им. С.С. Корсакова. 2023;123(9):21-25. https://doi.org/10.17116/jnevro202312309121
19. Oh J, Giacomini PS, Yong VW, Costello F, Blanchette F, Freedman MS. From progression to progress: The future of multiple sclerosis. J Cent Nerv Syst Dis. 2024;16:11795735241249693. https://doi.org/10.1177/11795735241249693
20. Myhr KM, Riise T, Vedeler C, Nortvedt MW, Grønning R, et al. Disability and prognosis in multiple sclerosis: demographic and clinical variables important for the ability to walk and awarding of disability pension. Mult Scler. 2001;7(1):59-65. https://doi.org/10.1177/135245850100700110
21. Kantarci O, Siva A, Eraksoy M, Karabudak R, Sütlaş N, et al. Survival and predictors of disability in Turkish MS patients. Turkish Multiple Sclerosis Study Group (TUMSSG). Neurology. 1998;51(3):765-772. https://doi.org/10.1212/wnl.51.3.765
22. Klotz L, Saraste M, Airas L, Kuhlmann T. Multiple sclerosis: 2024 update. Free Neuropathol. 2025;6:14. https://doi.org/10.17879/freeneuropathology-2025-6762
Об авторах
Л. П. СизякинаРоссия
Сизякина Людмила Петровна, д.м.н., профессор, заведующая кафедрой клинической иммунологии и аллергологии ФПК и ППС
г. Ростов-на-Дону
Конфликт интересов:
Автор статьи Л.П. Сизякина входит в состав редакционной коллегии журнала «Медицинский вестник Юга России». Статья прошла принятую в журнале процедуру рецензирования независимыми экспертами. Об иных конфликтах интересов авторы не заявляли.
З. А. Гончарова
Россия
Гончарова Зоя Александровна, д.м.н., профессор, заведующая кафедрой нервных болезней и нейрохирургии
г. Ростов-на-Дону
Конфликт интересов:
О конфликтах интересов автор не заявлял.
Н. М. Ярош
Россия
Ярош Наталья Михайловна, врач-невролог неврологического отделения РостГМУ
г. Ростов-на-Дону
Конфликт интересов:
О конфликтах интересов автор не заявлял.
Е. А. Маркова
Россия
Маркова Елена Алексадровна, врач-невролог неврологического отделения РостГМУ
г. Ростов-на-Дону
Конфликт интересов:
О конфликтах интересов автор не заявлял.
Рецензия
Для цитирования:
Сизякина Л.П., Гончарова З.А., Ярош Н.М., Маркова Е.А. Клинико-иммунологические аспекты первой атаки рассеянного склероза (клинически изолированный синдром). Медицинский вестник Юга России. 2026;17(1):87-96. https://doi.org/10.21886/2219-8075-2026-17-1-87-96
For citation:
Sizyakina L.P., Goncharova Z.A., Yarosh N.M., Markova E.A. Clinical and immunological aspects of the first attack of multiple sclerosis (clinically isolated syndrome). Medical Herald of the South of Russia. 2026;17(1):87-96. (In Russ.) https://doi.org/10.21886/2219-8075-2026-17-1-87-96
JATS XML







































