Перейти к:
Сравнительная эффективность различных способов назначения розувастатина и эзетимиба в комбинации с ингибиторами PCSK9
https://doi.org/10.21886/2219-8075-2024-15-2-81-89
Аннотация
Цель: сравнительная оценка эффективности комбинированной гиполипидемической терапии розувастатином и эзетимибом в фиксированной и раздельной комбинациях с ингибиторами PCSK9 у больных очень высокого сердечно-сосудистого риска.
Материалы и методы: 65 участников исследования были разделены на 2 группы в зависимости от способа комбинированной липидснижающей терапии и наблюдались 5 месяцев на 6 визитах. Оценивалась эффективность гиполипидемического ответа в каждой из исследуемых групп.
Результаты: в группе с раздельным назначением гиполипидемических препаратов целевых значений холестерина липопротеинов низкой плотности (ХС ЛПНП) достигло 50% больных, уровень ХС ЛПНП в процессе 5 месяцев лечения снизился на 38,22 % с 2,25 [1,82; 2,47] ммоль/л до 1,39 [1,21; 1,59] ммоль/л (p<0,001). В группе с фиксированной комбинацией розувастатина и эзетимиба 61,29% участников исследования достигло целевых диапазонов ХС ЛПНП, концентрация ХС ЛПНП снизилась на 47,46% с 2,36 [1,92; 2,57] ммоль/л до 1,24 [1,18; 1,56] ммоль/л (p<0,001). При проведении логистического регрессионного анализа показана достоверная ассоциация женского пола с более высоким риском не достигнуть целевых диапазонов ХС ЛПНП (χ²<0,001; ОШ 0,13 95 % ДИ 0,04–0,39; p<0,001).
Заключение: использование фиксированной комбинации розувастатина и эзетимиба в сочетании с ингибиторами PCSK9 у больных с очень высоким сердечно-сосудистым риском позволяет на 9,24% интенсивнее снижать концентрацию ХС ЛПНП относительно лекарственной схемы с раздельным приемом препаратов.
Для цитирования:
Кузнецов А.А., Маль Г.С., Сараев И.А. Сравнительная эффективность различных способов назначения розувастатина и эзетимиба в комбинации с ингибиторами PCSK9. Медицинский вестник Юга России. 2024;15(2):81-89. https://doi.org/10.21886/2219-8075-2024-15-2-81-89
For citation:
Kuznetsov A.A., Mal G.S., Saraev I.A. Comparative effectiveness of different methods of prescribing rosuvastatin and ezetimibe in combination with PCSK9 inhibitors. Medical Herald of the South of Russia. 2024;15(2):81-89. (In Russ.) https://doi.org/10.21886/2219-8075-2024-15-2-81-89
Введение
Несмотря на значительный прогресс в области диагностики и лечения сердечно-сосудистых заболеваний (ССЗ), болезни системы кровообращения на протяжении длительного времени занимают лидирующие позиции в структуре смертности населения нашей страны [1]. Безусловно, за последние 20 лет удалось добиться снижения данного показателя почти в 2 раза (с 927 до 570 случаев на 100 тысяч населения)1, однако кардио-васкулярная патология всё ещё представляет существенную опасность, снижая продолжительность и ухудшая качество жизни. Также стоит отметить, что, согласно прогнозам Всемирной организации здравоохранения, ситуация не улучшится в течение ближайших 30 лет2.
В ходе проведения многочисленных популяционных исследований [2], с результатами которых согласуются результаты Российского эпидемиологического исследования ЭССЕ-РФ [3], показано, что наиболее распространённым модифицируемым фактором риска ССЗ является дислипидемия, которая была выявлена более чем у половины населения нашей страны независимо от возраста. Эпидемиологическое многоцентровое исследование INTERHEART продемонстрировало, что наибольший вклад в развитие первого инфаркта миокарда внесли нарушения липидного обмена [4]. Патогенез ССЗ базируется на процессах атеросклероза, формирование и течение которого напрямую зависят от концентрации атерогенных липопротеидов в плазме крови. Согласно актуальным клиническим рекомендациям по диагностике и коррекции нарушений липидного обмена VIII пересмотра от 2023 г., целевые диапазоны холестерина липопротеидов низкой плотности (ХС ЛПНП) зависят от категории относительного сердечно-сосудистого риска (ССР) [5].
На сегодняшний день достигнуты серьёзные успехи в отношении контроля уровня ХС ЛПНП, однако, как показали результаты исследований DYSIS и DA VINCI [6–8], значительная доля пациентов с очень высоким ССР не достигает необходимых целевых значений ХС ЛПНП. Более 40 лет первой линией фармакотерапии нарушений липидного обмена являются ингибиторы 3‑гидрокси‑3‑метилглутарил-Кофермент А редуктазы —статины, а одним из наиболее мощных препаратов этой группы — розувастатин. Его эффективность и безопасность была доказана в ходе проведения программы GALAXY, которая включила в себя 18 многоцентровых рандомизированных исследований [9]. Применение розувастатина в максимальной дозе 40 мг/сут. позволяет снизить уровень ХС ЛПНП до 50%, но, как показывает реальная клиническая практика в исследованиях EUROASPIRE IV и EUROASPIRE V, этого недостаточно для достижения целевых концентраций у пациентов с дислипидемиями [10][11].
При неэффективности монотерапии статинами рекомендуется добавлять в лечение эзетимиб — селективный ингибитор всасывания холестерина в кишечнике [5]. Комбинированная гиполипидемическая терапия с эзетимибом позволяет дополнительно снизить концентрацию ХС ЛПНП до 21-27% [12]. Однако добавление в лечение второго препарата может уменьшать приверженность больных к назначенной схеме лечения. С целью повышения уровня комплаентности у больных, получающих комбинированную гиполипидемическую терапию, можно рассмотреть применение лекарственных средств с фиксированной комбинацией различных препаратов. Для сравнения эффективности двух способов назначения липидснижающей терапии в 2019 г. было проведено ретроспективное когортное исследование по изучению тенденции назначения статинов и эзетимиба в виде фиксированной комбинации или отдельных таблеток, в котором показано, что назначение розувастатина и эзетимиба в виде фиксированного сочетания на 9% эффективнее снижает уровень ХС ЛПНП [13].
Наряду с блокаторами всасывания и продукции холестерина в печени при недостижении целевых диапазонов ХС ЛПНП рекомендуется добавление в терапию генно-инженерных гиполипидемических лекарственных средств, моноклональных антител — ингибиторов плазменного белка пропротеиновой конвертазы субтилизин-кексинового типа 9 (PCSK9), позволяющих добиться достижения целевых значений ХС ЛПНП более чем у 90% больных [14]. Однако на сегодняшний день применение этой группы препаратов ограничено в связи с их высокой стоимостью и низкой доступностью в регионах. При этом в научной литературе нет данных об эффективности применения ингибиторов PCSK9 в составе тройной комбинированной гиполипидемической терапии с различными способами назначения статинов и эзетимиба.
Цель исследования — сравнительная оценка эффективности комбинированной гиполипидемической терапии розувастатином и эзетимибом в фиксированной и раздельной комбинациях с ингибиторами PCSK9 у больных очень высокого ССР.
Материалы и методы
В сравнительное проспективное открытое исследование были включены 65 больных с очень высоким ССР, требующих интенсивной гиполипидемической терапии (37 мужчин и 28 женщин) в возрасте от 40 до 79 лет, средний возраст участников составил 61,11±10,55 года. Исследование проводилось в 2022–2023 гг. на базе кардиологического отделения ГБУЗ МО «Московская областная больница им. проф. Розанова В.Н.». Протокол исследования получил одобрение локального этического комитета ФГБОУ ВО «Курский государственный медицинский университет» Минздрава России (протокол № 3 от 16.03.2020), соответствовал принципам, изложенным в Хельсинкской декларации Всемирной медицинской ассоциации «Этические принципы медицинских исследований с участием человека в качестве испытуемого» и требованиями надлежащей клинической практики. Участие в исследовании было добровольным, все пациенты подписали информированное согласие.
Критерии включения пациентов в настоящее исследование: первичная дислипидемия, недостижение целевых диапазонов ХС ЛПНП, рекомендованных актуальными клиническими рекомендациями по диагностике и коррекции нарушений липидного обмена VIII пересмотра [5] в процессе 8 недель применения комбинированной гиполипидемической терапией высокоинтенсивной дозы розувастатина и эзетимиба. Критерии невключения: индивидуальная непереносимость любого компонента проводимой тройной гиполипидемической терапии, терминальная хроническая сердечная недостаточность (по Василенко-Стражеско), ожирение 3 степени. Критерий исключения — отказ больного от продолжения исследования.
За 8 недель до начала исследования все его участники были разделены на 2 группы в зависимости от способа получения комбинированной гиполипидемической терапии. В первую группу вошли 46 человек, которым был назначен розувастатин в дозе 40 мг/сут. и эзетимиб 10 мг/сут. в двух таблетках, во вторую группу — 49 больных, которым была назначена фиксированная комбинация розувастатина и эзетимиба в дозе 40+10 мг/сут. в одной таблетке («ЗЕНОН», АО «Санофи-авентис груп», Франция). В процессе проведения лечения комбинацией розувастатина и эзетимиба в первой группе целевых значений ХС ЛПНП достигли 12 человек, во второй группе — 18 пациентов, в связи с чем они были исключены из дальнейшего исследования. Назначение ингибиторов PCSK9 потребовалось 34 больным в группе с раздельным приемом розувастатина/ эзетимиба и 31 пациенту в группе с фиксированным сочетанием гиполипидемических препаратов. Всем участником исследования был назначен алирокумаба («PRALUENT», АО «Санофи-авентис груп», Франция) в дозе 150 мг по стандартной схеме: 1 инъекция в 14 суток подкожно, с последующим контролем эффективности гиполипидемического ответа в течение 5 последующих визитов 1 раз в месяц (медиана периода наблюдения после начала лечения ингибиторами PCSK9 составила 5 месяцев). Участники исследования обеих групп на момент скрининга были сопоставимы по полу, возрасту, основным факторам риска, фоновым и сопутствующим заболеваниям, показателям липидного спектра (табл. 1).
Таблица / Table 1
Клиническая характеристика исследуемых групп на момент скрининга
Clinical characteristics of the studied groups at the time of screening
Показатели Indicators | Все пациенты All patients (n=65) | Раздельный приём Separate reception (n=34) | Фиксированная комбинация Fixed combination (n=31) | p |
Возраст, годы Age, years | 61,11±10,55 | 60,5 [ 52,25; 70,5] | 62 [ 55; 70] | 0,56 |
Мужчины / женщины Men / women | 37/28 | 20/14 | 17/14 | 0,94 |
Ишемическая болезнь сердца, n (%) Coronary heart disease, n (%) | 62 (95,38) | 32 (94,12) | 30 (96,77) | 0,93 |
Артериальная гипертензия, n (%) Arterial hypertension, n (%) | 64 (98,46) | 33 (97,06) | 31 (100) | 0,96 |
Курение, n (%) Smoking, n (%) | 45 (69,23) | 21 (61,76) | 24 (77,42) | 0,27 |
Отягощённая наследственность по ССЗ, n (%) Burdened heredity by CVD, n (%) | 22 (33,85) | 9 (26,47) | 13 (41,94) | 0,29 |
Сахарный диабет 2 типа, n (%) Type 2 diabetes mellitus, n (%) | 17 (26,15) | 10 (29,41) | 7 (22,58) | 0,73 |
Ожирение 1–2 степени, n (%) Obesity of 1–2 degrees, n (%) | 26 (40) | 12 (35,29) | 14 (45,16) | 0,58 |
ОХ, ммоль/л TCh, mmol/l | 5,03±0,45 | 4,95 [ 4,6; 5,36] | 5,12 [ 4,68; 5,46] | 0,49 |
ХС ЛПНП, ммоль/л LDL cholesterol, mmol/l | 2,24±0,43 | 2,25 [ 1,82; 2,47] | 2,36 [ 1,92; 2,57] | 0,78 |
ХС ЛПВП, ммоль/л HDL cholesterol, mmol/l | 1,1±0,13 | 1,17 [ 0,98; 1,22] | 1,08 [ 1,02; 1,2] | 0,47 |
ТГ, ммоль/л TG, mmol/l | 2,26±0,39 | 2,2 [ 1,92; 2,57] | 2,32 [ 2,03; 2,6] | 0,41 |
Примечание: ССЗ — сердечно-сосудистые заболевания; ОХ — общий холестерин; ХС ЛПНП — холестерин липопротеидов низкой плотности; ХС ЛПВП — холестерин липопротеидов высокой плотности; ТГ — триглицериды; p — достоверность различий между группами.
Note: CVD — cardiovascular diseases; TCh — total cholesterol; LDL cholesterol — low-density lipoprotein cholesterol; HDL cholesterol — high-density lipoprotein cholesterol; TG — triglycerides; p-values — significant differences between respective groups.
Пробы крови для биохимических исследований забирались однократно из локтевой вены утром натощак через 12 часов после приёма пищи. Анализ проводили на автоматическом биохимическом анализаторе Mindray BS-120 (Китай). Из показателей липидного обмена оценивали уровень общего холестерина (ОХ), ХС ЛПНП, холестерина липопротеинов высокой плотности (ХС ЛПВП) и триглицеридов (ТГ).
Статистическая обработка полученных в исследовании данных проводилась с использованием компьютерной программы «SPSS 23.0» (IBM, США). Проверка нормальности распределения проводилась методом Колмогорова-Смирнова с поправкой Лиллиефорса или при помощи теста Шапиро-Уилка (при числе исследуемых в группах менее 50). При нормальном распределении количественные показатели представлены как M±SD, где M — арифметическое среднее, SD — стандартное отклонение; для показателей с распределением отличным от нормального — в виде медианы и интерквартильного размаха (Me [Q1; Q3]). Для показателей, характеризующих качественные признаки, указывались абсолютное число и/или относительная величина в процентах. Для оценки сопоставимости между двумя исследуемыми группами по количественным показателям использовали критерии Манна-Уитни, для зависимых выборок использовали критерий Вилкоксона и t-критерий Стьюдента — для оценки гиполипидемического ответа среди всех участников исследования. Различия считались статистически значимыми при p<0,05. Сравнительный анализ качественных параметров использовался с применением χ² Пирсона либо точного теста Фишера. С целью оценки влияния некоторых признаков на исходы лечения определялось отношение шансов (ОШ, odds ratio) по стандартной методике и указанием 95 %-го доверительного интервала (ДИ).
Результаты
На момент начала лечения алирокумабом все пациенты были сопоставимы по показателям липидного профиля (рис. 1) и основным коморбидным состояниям. В процессе проведения исследования у пациентов не было зарегистрировано острых сердечно-сосудистых событий или смертельного исхода. До начала лечения алирокумабом все больные на протяжении 8 недель получали двойную гиполипидемическую терапию розувастатином и эзетимибом и не достигли целевых значений ХС ЛПНП, рекомендованных актуальными клиническими рекомендациями по диагностике и коррекции нарушений липидного обмена VIII пересмотра [5]. До этого 44,62 % (n=29) участников настоящего исследования ранее принимали статины и 16,92 % (n=11) – в высокоинтенсивных дозах, 4,62 % (n=3) ранее принимали эзетимиб в стандартной дозе 10мг/сут.
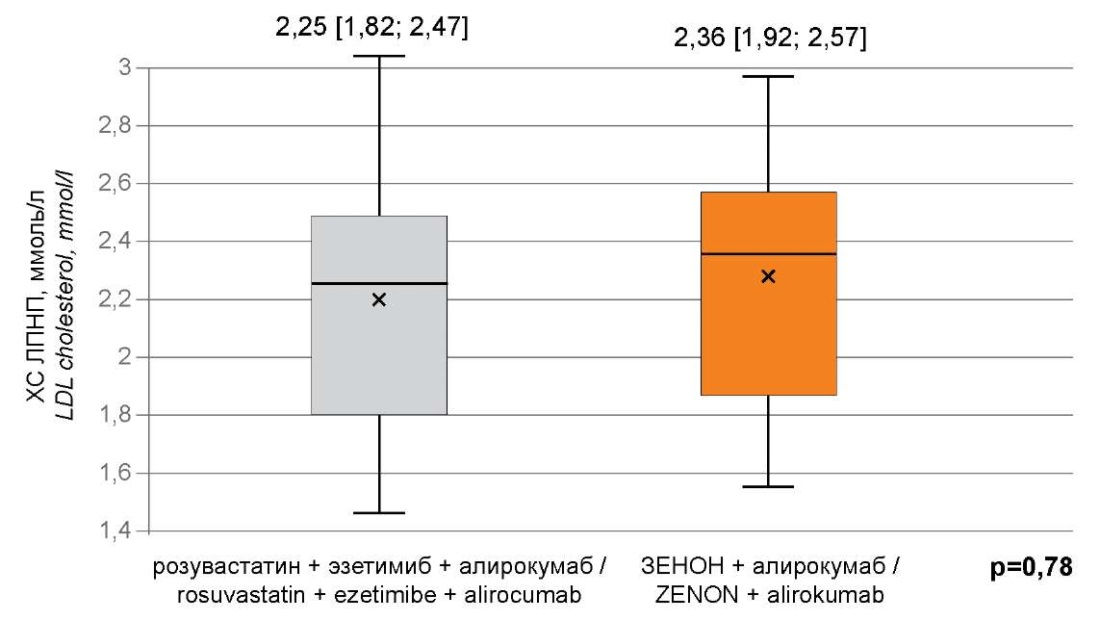
Рисунок 1. Концентрация ХС ЛПНП в исследуемых группах
на момент начала исследования.
Figure 1. The concentration of LDL cholesterol in the study groups
at the time of the start of the study.
Примечание: ХС ЛПНП — холестерин липопротеидов низкой плотности;
p — значение критерия Манна-Уитни.
Note: LDL cholesterol — low-density lipoprotein cholesterol;
p-values — the value of the Mann-Whitney criterion.
За время наблюдения целевых диапазонов ХС ЛПНП достигло 50% больных (n=17) в группе с раздельным приёмом розувастатина и эзетимиба и 61,29% пациентов (n=19) в группе с фиксированной комбинацией этих препаратов. Концентрация ХС ЛПНП среди всех участников исследования в процессе 5 месяцев применения тройной гиполипидемической терапии розувастатином, эзетимибом и алирокумабом снизилась на 38,39% с 2,24±0,43 ммоль/л до с 1,38±0,31 ммоль/л (p<0,001) (рис. 2). При этом в группе больных с раздельным приемом розувастатина и эзетимиба наблюдался менее выраженный гиполипидемической эффект по всем показателям липидного профиля. Уровень ХС ЛПНП у больных в этой группе понизился на 38,22% с 2,25 [ 1,82; 2,47] ммоль/л до 1,39 [ 1,21; 1,59] ммоль/л (p<0,001), ОХ снизился на 29,49% с 4,95 [ 4,6; 5,36] ммоль/л до 3,49 [ 3,32; 3,72] ммоль/л (p<0,001), уровень ХС ЛПВП повысился на 2,56% с 1,17 [ 0,98; 1,21] ммоль/л до 1,2 [ 1,01; 1,25] ммоль/л (p<0,001), ТГ снизились на 18,64% с 2,2 [ 1,92; 2,57] ммоль/л до 1,79 [ 1,48; 1,95] ммоль/л (p<0,001). Напротив, в группе с фиксированной комбинацией розувастатина и эзетимиба наблюдалось более эффективное снижение концентрации ХС ЛПНП у наблюдаемых пациентов на 47,46% с 2,36 [ 1,92; 2,57] ммоль/л до 1,24 [ 1,18; 1,56] ммоль/л (p<0,001), ОХ на 37,5% с 5,12 [ 4,68; 5,46] ммоль/л до 3,2 [ 2,97; 3,37] ммоль/л (p<0,001), повышение уровня ХС ЛПВП на 6,48% с 1,08 [ 1,02; 1,2] ммоль/л до 1,15 [ 1,06; 1,26] ммоль/л (p<0,001), снижение ТГ на 25,43% с 2,32 [ 2,03; 2,6] ммоль/л до1,73 [ 1,44; 2,03] ммоль/л (p<0,001) (рис. 3). Динамика изменения показателей липидного спектра по визитам представлена в табл. 2.
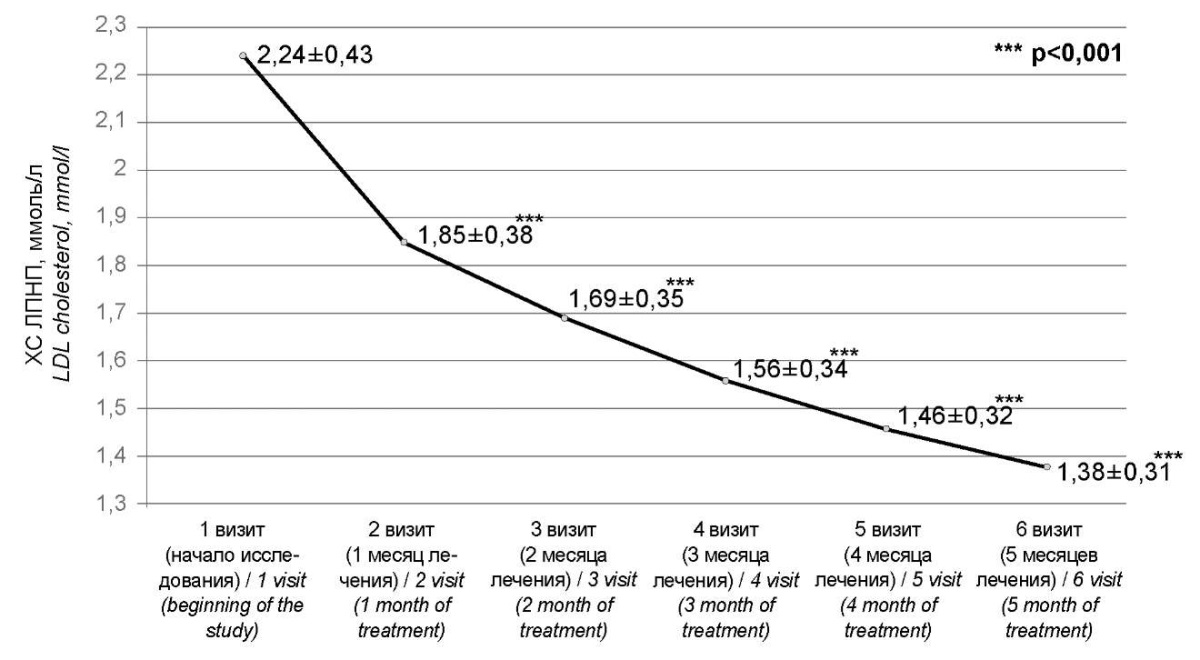
Рисунок 2. Динамика изменения ХС ЛПНП среди всех участников исследования.
Figure 2. Dynamics of changes in LDL cholesterol among all study participants.
Примечание: ХС ЛПНП — холестерин липопротеидов низкой плотности;
p — значение критерия Стьюдента для зависимых выборок.
Note: LDL cholesterol — low-density lipoprotein cholesterol;
p-values — the value of the Student's criterion for dependent samples.
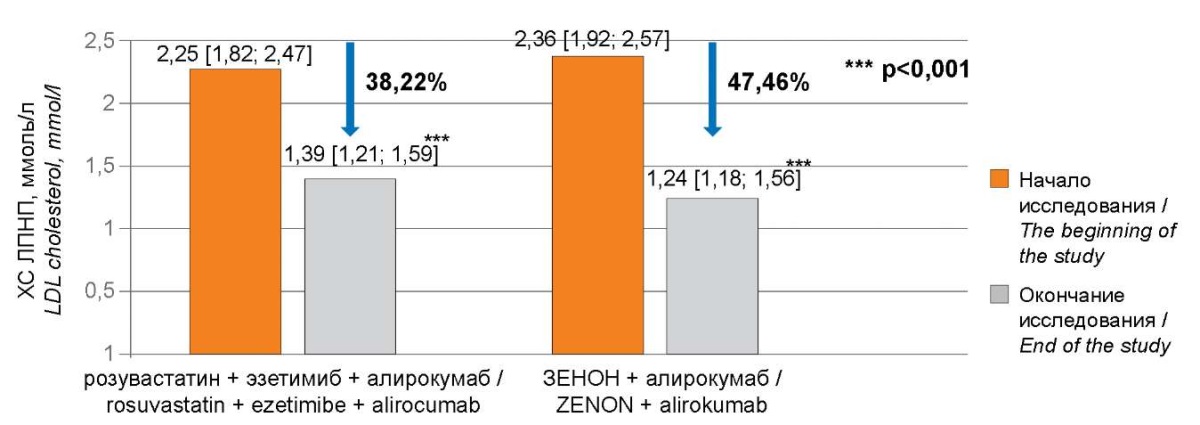
Рисунок 3. Снижение ХС ЛПНП в исследуемых группах.
Figure 3. Reduction of LDL cholesterol in the study groups.
Примечание: ХС ЛПНП — холестерин липопротеидов низкой плотности;
p — значение критерия Вилкоксона.
Note: LDL cholesterol — low-density lipoprotein cholesterol;
p-values — the value of the Wilcoxon criterion.
Таблица / Table 2
Динамика изменения показателей липидного спектра
в рассматриваемых группах в процессе проведения исследования
Dynamics of changes in lipid spectrum indicators
in the groups under consideration during the study
Показатели Indicators | 1 визит (скрининг) 1 visit (screening) | 2 визит (1 месяц лечения) 2 visit (1 month of treatment) | 3 визит (2 месяца лечения) ) 3 visit (2 month of treatment) | 4 визит (3 месяца лечения)) 4 visit (3 month of treatment) | 5 визит (4 месяца лечения)) 5 visit (4 month of treatment) | 6 визит (5 месяцев лечения)) 6 visit (5 month of treatment) | ||||||
Значение Meaning | Значение Meaning | p | Значение Meaning | p | Значение Meaning | p | Значение Meaning | p | Значение Meaning | p | ||
ОХ, ммоль/л TCh, mmol/l | Не фикс Not a fix | 4,95 [ 4,6; 5,36] | 4,39 [ 4,23; 4,8] | <0,001 | 4,13 [ 4,04; 4,31] | <0,001 | 3,9 [ 3,81; 4,03] | <0,001 | 3,61 [ 3,52; 3,81] | <0,001 | 3,49 [ 3,32; 3,72] | <0,001 |
Фикс Fix | 5,12 [ 4,68; 5,46] | 4,48 [ 4,22; 4,83] | <0,001 | 4,08 [ 3,98; 4,21] | <0,001 | 3,78 [ 3,59; 3,94] | <0,001 | 3,45 [ 3,19; 3,63] | <0,001 | 3,2 [ 2,97; 3,37] | <0,001 | |
ХС ЛПНП, ммоль/л LDL cholesterol, mmol/l | Не фикс Not a fix | 2,25 [ 1,82; 2,47] | 1,88 [ 1,48; 2,14] | <0,001 | 1,69 [ 1,37; 1,97] | <0,001 | 1,55 [ 1,33; 1,77] | <0,001 | 1,48 [ 1,27; 1,66] | <0,001 | 1,39 [ 1,21; 1,59] | <0,001 |
Фикс Fix | 2,36 [ 1,92; 2,57] | 1,81 [ 1,55; 2,13] | <0,001 | 1,63 [ 1,42; 1,93] | <0,001 | 1,42 [ 1,32; 1,78] | <0,001 | 1,31 [ 1,22; 1,66] | <0,001 | 1,24 [ 1,18; 1,56] | <0,001 | |
ХС ЛПВП, ммоль/л HDL cholesterol, mmol/l | Не фикс Not a fix | 1,17 [ 0,98; 1,21] | 1,17 [ 0,99; 1,23] | <0,001 | 1,16 [ 1; 1,23] | <0,001 | 1,17 [ 0,99; 1,23] | <0,001 | 1,18 [ 1,05; 1,23] | <0,001 | 1,2 [ 1,01; 1,25] | <0,001 |
Фикс fix | 1,08 [ 1,02; 1,2] | 1,1 [ 1,01; 1,22] | <0,001 | 1,11 [ 1,02; 1,23] | <0,001 | 1,13 [ 1,04; 1,25] | <0,001 | 1,13 [ 1,05; 1,25] | <0,001 | 1,15 [ 1,06; 1,26] | <0,001 | |
ТГ, ммоль/л TG, mmol/l | Не фикс Not a fix | 2,2 [ 1,92; 2,57] | 2,02 [ 1,81; 2,38] | <0,001 | 1,91 [ 1,72; 2,28] | <0,001 | 1,87 [ 1,64; 2,2] | <0,001 | 1,83 [ 1,58; 2,07] | <0,001 | 1,79 [ 1,48; 1,95] | <0,001 |
Фикс Fix | 2,32 [ 2,03; 2,6] | 2,16 [ 1,87; 2,46] | <0,001 | 2,08 [ 1,73; 2,31] | <0,001 | 2,01 [ 1,64; 2,23] | <0,001 | 1,89 [ 1,57; 2,17] | <0,001 | 1,73 [ 1,44; 2,03] | <0,001 | |
Примечание: ОХ — общий холестерин; ХС ЛПНП — холестерин липопротеидов низкой плотности; ХС ЛПВП — холестерин липопротеидов высокой плотности; ТГ — триглицериды; p — достоверность различий между группами.
Note: TCh — total cholesterol; LDL cholesterol — low-density lipoprotein cholesterol; HDL cholesterol — high-density lipoprotein cholesterol; TG — triglycerides; p-values — significant differences between respective groups.
С целью обнаружения качественных признаков, ассоциированных с менее выраженным лекарственным ответом на проводимое лечение, был проведён однофакторный логистический регрессионный анализ с такими факторами, как возраст, гендерная принадлежность, наличие ишемической болезни сердца, артериальной гипертензии, сахарного диабет 2 типа, ожирения 1–2 степени, отягощённой наследственности по ССЗ, привычки курения. В ходе проведения регрессионного анализа показана достоверная ассоциация женского пола с более высоким риском не достигнуть целевых диапазонов ХС ЛПНП. Среди больных, достигших целевых значений ХС ЛПНП, было 8 (22,22 %) женщин и 28 (77,78 %) мужчин (χ²<0,001; ОШ 0,13 95 % ДИ 0,04–0,39; p<0,001) (рис. 4).
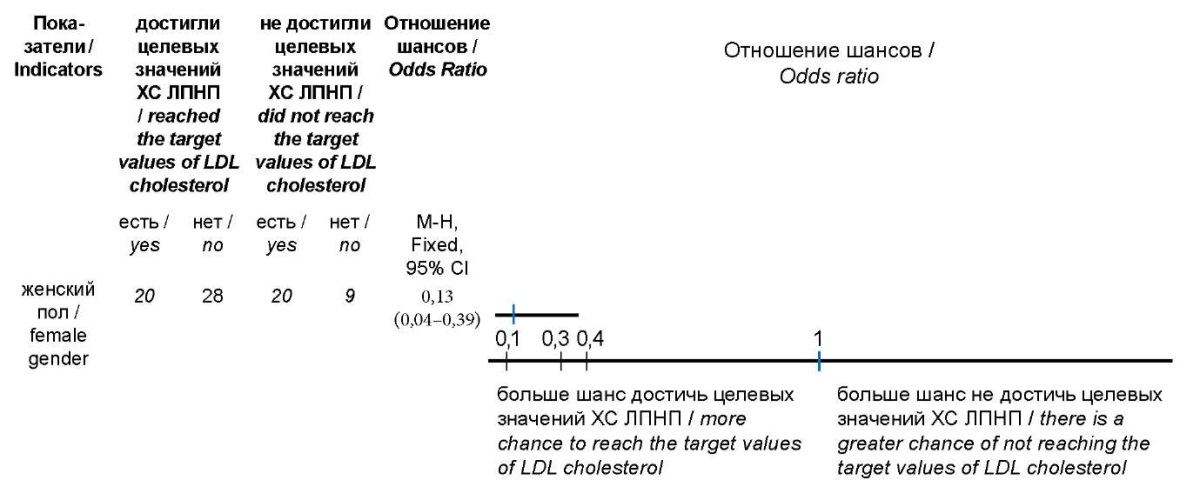
Рисунок 4. Отношение шансов показателей,
ассоциированных с более высоким риском
недостижения целевых концентраций ХС ЛПНП.
Figure 4. The ratio of the odds of indicators associated with a higher risk
of not reaching the target concentrations of LDL cholesterol.
Примечание: ХС ЛПНП — холестерин липопротеидов низкой плотности.
Note: LDL cholesterol — low-density lipoprotein cholesterol.
Обсуждение
На сегодняшний день мы обладаем весомой доказательной базой в концепции эффективности применения «политаблеток» с фиксированными комбинациями лекарственных препаратов. Согласно результатам таких исследований, как UMPIRE [15], IMPACT [16], CNIC [17], у больных, принимающих многокомпонентные препараты, наблюдается достоверное снижение сердечно-сосудистых рисков на фоне повышения приверженности к лечению. При этом, несмотря на потенциальную пользу и наличие определённой доказательной базы, отсутствие рандомизированных клинических исследований многокомпонентных лекарственных препаратов ограничивает дальнейшее внедрение данного подхода в клиническую практику. Тем не менее, последнее десятилетие ознаменовалось созданием множества средств с фиксированными комбинациями медикаментозных средств, в том числе направленных на достижение целевых значений липопротеидов.
В ходе проведения настоящего исследования показано повышение эффективности тройной гиполипидемической терапии с фиксированной комбинацией розувастатина и эзетимиба на 9,24% относительно группы больных с раздельным приемом препаратов, что согласуется результатами ретроспективного анализа двух способов назначения гиполипидемической терапии, проведенного в 2019 г., где эффектность фиксированного способа назначения розувастатина и эзетимиба была на 9% выше раздельной схемы приёма препаратов [13] и результатами исследования The Multiceneter Randomized Study of Rosuvastatin and Ezetimibe (MRS-ROSE), в ходе которого показано более эффективное снижение уровня ХС ЛПНП при фиксированном применении розувастатина и эзетимиба [18]. Особенностью нашего исследования явилась комбинация двух способов назначения розувастатина и эзетимиба с алирокумабом.
Результаты настоящего исследования согласуются с результатами ранее проводимых нами исследований по применению тройной гиполипидемической терапии статином, эзетимибом и алирокумабом, однако ранее в наших исследованиях мы использовали аторвастатин в максимально переносимой дозе 40–80мг/сут. [19–21].
В течение 5 месяцев применения комбинированной гиполипидемической терапии 55,38% участников исследования достигли целевых диапазонов ХС ЛПНП, что не согласуется с результатами исследования FOURIER, где в ходе проведения тройной комбинированной гиполипидемической терапии целевых значений ХС ЛПНП достигло 97% участников исследования, что может быть связано с более длительным наблюдением за пациентами (2,2 года) и менее амбициозными целевыми границами ХС ЛПНП (<1,8 ммоль/л) [22].
В нашем исследовании показано, что достигнутый гиполипидемический эффект через 1 месяц после добавления в лечение алирокумаба, сохранялся на всем протяжении исследования, что может говорить о стабильности изучаемых показателей и свидетельствует об отсутствии необходимости постоянного контроля показателей липидного спектра у лиц с дислипидемией, что согласуется с результатами наблюдательного исследования OSLER-1, в котором на протяжении 48 месяцев наблюдали за пациентами, получающими ингибиторы PCSK9. В исследовании было показано отсутствие «эффекта затухания» в ходе длительного применения ингибиторов PCSK9, что, вероятнее всего, связано с отсутствием иммуногенности у данной группы препаратов [23].
Доказано, что пациенты женского пола имеют более высокий риск недостижения целевых значений ХС ЛПНП, что не согласуется с исследованием, выполненным в 2020 г. в ФГБНУ «ЦКБ РАН», где мужчины имели более высокий шанс недостижения целевых границ ХС ЛПНП (χ2=0,004; ОШ 0,157; 95 % ДИ 0,043-0,572), что может быть связано с более низкой статистической силой этого исследования (49 больных наблюдались 10 недель) [24].
Таким образом, применение фиксированной комбинации розувастатина в максимально переносимой дозе и эзетимиба в сочетании с ингибиторами PCSK9 сопровождалось более эффективным снижением уровня липопротеидов по отношению к тройной гиполидемической терапии со свободными комбинациями лекарственных препаратов.
Заключение
Согласно результатам данного исследования, использование фиксированной комбинации розувастатина и эзетимиба в тройной комбинированной гиполипидемической терапии с ингибиторами PCSK9 у больных с очень высоким ССР позволяет на 9,24% интенсивнее снижать концентрацию ХС ЛПНП относительно лекарственной схемы с раздельным приемом препаратов.
Представляется целесообразным делать выбор в пользу назначения липидснижающих средств в виде фиксированных комбинаций, особенно у пациентов с низкой приверженностью к терапии.
1. https://www.gks.ru/folder/12781 (accessed: 09.09.2023).
2. https://www.who.int/data/gho/data/themes/mortality-and-global-health-estimates/ghe-leading-causes-of-death (accessed: 09.09.2023)
Список литературы
1. Roth GA, Mensah GA, Johnson CO, Addolorato G, Ammirati E, et al. Global Burden of Cardiovascular Diseases and Risk Factors, 1990-2019: Update From the GBD 2019 Study. J Am Coll Cardiol. 2020;76(25):2982-3021. Erratum in: J Am Coll Cardiol. 2021;77(15):1958-1959. https://doi.org/10.1016/j.jacc.2020.11.010.
2. Watts GF, Catapano AL, Masana L, Zambon A, Pirillo A, Tokgözoğlu L. Hypercholesterolemia and cardiovascular disease: Focus on high cardiovascular risk patients. Atheroscler Suppl. 2020;42:e30-e34. https://doi.org/10.1016/j.atherosclerosissup.2021.01.006
3. Бойцов С.А., Драпкина О.М., Шляхто Е.В., Конради А.О., Баланова Ю.А., и др. Исследование ЭССЕ-РФ (Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в регионах Российской Федерации). Десять лет спустя. Кардиоваскулярная терапия и профилактика. 2021;20(5):3007. https://doi.org/10.15829/1728-8800-2021-3007
4. Yusuf S, Hawken S, Ounpuu S, Dans T, Avezum A, et al. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): case-control study. Lancet. 2004;364(9438):937-52. https://doi.org/10.1016/S0140-6736(04)17018-9
5. Ежов М.В., Кухарчук В.В., Сергиенко И.В., Алиева А.С., Анциферов М.Б., и др. Нарушения липидного обмена. Клинические рекомендации 2023. Российский кардиологический журнал. 2023;28(5):5471. https://doi.org/10.15829/1560-4071-2023-5471
6. Gitt AK, Lautsch D, Ferrières J, De Ferrari GM, Vyas A, et al. Cholesterol target value attainment and lipid-lowering therapy in patients with stable or acute coronary heart disease: Results from the Dyslipidemia International Study II. Atherosclerosis. 2017;266:158-166. https://doi.org/10.1016/j.atherosclerosis.2017.08.013
7. Gitt AK, Lautsch D, Ferrieres J, Kastelein J, Drexel H, et al. Low-density lipoprotein cholesterol in a global cohort of 57,885 statin-treated patients. Atherosclerosis. 2016;255:200-209. https://doi.org/10.1016/j.atherosclerosis.2016.09.004
8. Ray KK, Molemans B, Schoonen WM, Giovas P, Bray S, et al. EU-Wide Cross-Sectional Observational Study of Lipid-Modifying Therapy Use in Secondary and Primary Care: the DA VINCI study. Eur J Prev Cardiol. 2021;28(11):1279-1289. https://doi.org/10.1093/eurjpc/zwaa047
9. Schuster H. The GALAXY Program: an update on studies investigating efficacy and tolerability of rosuvastatin for reducing cardiovascular risk. Expert Rev Cardiovasc Ther. 2007;5(2):177-193. https://doi.org/10.1586/14779072.5.2.177
10. Kotseva K, Wood D, De Bacquer D, De Backer G, Rydén L, et al. EUROASPIRE IV: A European Society of Cardiology survey on the lifestyle, risk factor and therapeutic management of coronary patients from 24 European countries. Eur J Prev Cardiol. 2016;23(6):636-48. https://doi.org/10.1177/2047487315569401
11. De Backer G, Jankowski P, Kotseva K, Mirrakhimov E, Reiner Ž, et al. Management of dyslipidaemia in patients with coronary heart disease: Results from the ESC-EORP EUROASPIRE V survey in 27 countries. Atherosclerosis. 2019;285:135-146. https://doi.org/10.1016/j.atherosclerosis.2019.03.014
12. Mach F, Baigent C, Catapano AL, Koskinas KC, Casula M, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020;41(1):111-188. Erratum in: Eur Heart J. 2020;41(44):4255. https://doi.org/10.1093/eurheartj/ehz455.
13. Catapano AL, Vrablik M, Karpov Y, Berthou B, Loy M, Baccara-Dinet M. A Phase 3 Randomized Controlled Trial to Evaluate Efficacy and Safety of New-Formulation Zenon (Rosuvastatin/Ezetimibe Fixed-Dose Combination) in Primary Hypercholesterolemia Inadequately Controlled by Statins. J Cardiovasc Pharmacol Ther. 2022;27:10742484221138284. https://doi.org/10.1177/10742484221138284
14. Кузнецов А.А., Маль Г.С. Вторичная профилактика ишемической болезни сердца и ингибиторы PCSK9. Терапия. 2021;2:105-111. https://doi.org/10.18565/therapy.2021.2.105-111
15. Thom S, Poulter N, Field J, Patel A, Prabhakaran D, et al. Effects of a fixed-dose combination strategy on adherence and risk factors in patients with or at high risk of CVD: the UMPIRE randomized clinical trial. JAMA. 2013;310(9):918-929. Erratum in: JAMA. 2013;310(14):1507. https://doi.org/10.1001/jama.2013.277064 .
16. Selak V, Elley CR, Bullen C, Crengle S, Wadham A, et al. Effect of fixed dose combination treatment on adherence and risk factor control among patients at high risk of cardiovascular disease: randomised controlled trial in primary care. BMJ. 2014;348:g3318. https://doi.org/10.1136/bmj.g3318
17. Castellano JM, Sanz G, Peñalvo JL, Bansilal S, Fernández-Ortiz A, et al. A polypill strategy to improve adherence: results from the FOCUS project. J Am Coll Cardiol. 2014;64(20):2071-2082. https://doi.org/10.1016/j.jacc.2014.08.021
18. Kim KJ, Kim SH, Yoon YW, Rha SW, Hong SJ, et al. Effect of fixed-dose combinations of ezetimibe plus rosuvastatin in patients with primary hypercholesterolemia: MRS-ROZE (Multicenter Randomized Study of ROsuvastatin and eZEtimibe). Cardiovasc Ther. 2016;34(5):371-382. https://doi.org/10.1111/1755-5922.12213
19. Маль Г.С., Кузнецов А.А. Ишемическая болезнь сердца и хроническая болезнь почек: возможности ингибиторов PCSK9 в достижении целевых значений атерогенных липопротеинов. Инновационная медицина Кубани. 2022;(2):14-21. https://doi.org/10.35401/2541-9897-2022-25-2-14-21
20. Кузнецов А. А., Маль Г. С. Динамика изменений липопротеинов и эстрогенов в процессе лекарственной коррекции дислипидемий ингибиторами PCSK9 с различной коморбидной патологией. Международный журнал сердца и сосудистых заболеваний. 2022;10(35):23-32. eLIBRARY ID: 49725100 EDN: BIAEWL
21. Кузнецов А.А., Маль Г.С. Возможности применения ингибиторов PCSK9 у больных ишемической болезнью сердца в сочетании с сахарным диабетом 2 типа. Регионарное кровообращение и микроциркуляция. 2022;21(2):16-25. https://doi.org/10.24884/1682-6655-2022-21-2-16-25
22. Sabatine MS, Giugliano RP, Keech AC, Honarpour N, Wiviott SD, et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med. 2017;376(18):1713-1722. https://doi.org/10.1056/NEJMoa1615664
23. Koren MJ, Sabatine MS, Giugliano RP, Langslet G, Wiviott SD, et al. Long-term Low-Density Lipoprotein Cholesterol-Lowering Efficacy, Persistence, and Safety of Evolocumab in Treatment of Hypercholesterolemia: Results Up to 4 Years From the Open-Label OSLER-1 Extension Study. JAMA Cardiol. 2017;2(6):598-607. https://doi.org/10.1001/jamacardio.2017.0747
24. Никитин А.Э., Аверин Е.Е., Рожков Д.Е., Созыкин А.В., Проценко Г.А. Опыт применения алирокумаба для достижения целевых уровней холестерина липопротеинов низкой плотности у пациентов, нуждающихся во вторичной профилактике сердечно-сосудистых заболеваний. Рациональная Фармакотерапия в Кардиологии. 2020;16(1):33-39. https://doi.org/10.20996/1819-6446-2020-02-06
Об авторах
А. А. КузнецовРоссия
Кузнецов Андрей Александрович - врач-кардиолог кардиологического отделения.
Московская область
Конфликт интересов:
Авторы заявляют, что данная работа, её тема, предмет и содержание не затрагивают конкурирующих интересов
Г. С. Маль
Россия
Маль Галина Сергеевна - д.м.н., профессор, зав. кафедрой фармакологии.
Курск
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
И. А. Сараев
Россия
Сараев Игорь Анатольевич - д.м.н., профессор кафедры внутренних болезней №2.
Курск
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов
Рецензия
Для цитирования:
Кузнецов А.А., Маль Г.С., Сараев И.А. Сравнительная эффективность различных способов назначения розувастатина и эзетимиба в комбинации с ингибиторами PCSK9. Медицинский вестник Юга России. 2024;15(2):81-89. https://doi.org/10.21886/2219-8075-2024-15-2-81-89
For citation:
Kuznetsov A.A., Mal G.S., Saraev I.A. Comparative effectiveness of different methods of prescribing rosuvastatin and ezetimibe in combination with PCSK9 inhibitors. Medical Herald of the South of Russia. 2024;15(2):81-89. (In Russ.) https://doi.org/10.21886/2219-8075-2024-15-2-81-89







































