Перейти к:
Таргетная терапия бронхиальной астмы у детей
https://doi.org/10.21886/2219-8075-2022-13-2-134-140
Аннотация
Цель: оценить клиническую эффективность таргетной терапии препаратом омализумаб у детей со среднетяжелой и тяжелой неконтролируемой бронхиальной астмой.
Материалы и методы: под наблюдением находились 7 детей, получающих терапию препаратом омализумаб в условиях стационара и поликлиники Городской детской клинической больницы №17 г. Уфа. В соответствии с инструкцией по применению, препарат моноклональных антител омализумаб вводился подкожно каждые 2–4 недели. Дозировка препарата определялась, исходя из массы тела ребенка и исходного уровня сывороточного IgE. У всех исследуемых детей изучались анамнез жизни и заболевания, результаты инструментальных и лабораторных методов исследования, результаты АСТ и с-АСТ тестов.
Результаты: на фоне терапии препаратом омализумаб у детей отмечалось значимое уменьшение частоты дневных симптомов (p=0,0179), уменьшение частоты ночных симптомов (p=0,0233), повышение физической активности (p=0,0179), уменьшение потребности в бронхолитиках (p=0,0179), увеличение ОФВ1 по данным спирографии (p=0,0431), уменьшение объема базисной противовоспалительной терапии со снижением дозы ИГКС у 71,43 % пациентов (p=0,0425), значимое повышение количества баллов АСТ и с-АСТ тестов: до лечения 12 [10; 13] баллов, на фоне лечения – 23 [20; 25] балла, (p=0,0277). За период наблюдения терапии препаратом омализумаб не было выявлено серьезных нежелательных реакций.
Заключение: таким образом, таргетная терапия с применением препарата омализумаб является клинически эффективной у детей со среднетяжелой и тяжелой неконтролируемой бронхиальной астмой.
Для цитирования:
Файзуллина Р.М., Санникова А.В., Шангареева З.А., Абсалямова Н.Т., Валеева Ж.А. Таргетная терапия бронхиальной астмы у детей. Медицинский вестник Юга России. 2022;13(2):134-140. https://doi.org/10.21886/2219-8075-2022-13-2-134-140
For citation:
Fayzullina R.M., Sannikova A.V., Shangareeva Z.A., Absalyamova N.T., Valeeva Zh.A. Targeted therapy of bronchial asthma in children. Medical Herald of the South of Russia. 2022;13(2):134-140. (In Russ.) https://doi.org/10.21886/2219-8075-2022-13-2-134-140
Введение
В настоящее время более 300 млн человек во всём мире страдает бронхиальной астмой (БА)1. Распространённость БА среди взрослого населения России составляет 6,9 %, среди детей достигает 10–12 % [1], при этом у 5–10 % больных отмечается тяжёлое течение заболевания [2]. Особую сложность представляют пациенты с тяжёлой и среднетяжёлой БА, которая не контролируется соответствующими ступенями лечения, требует высоких доз ингаляционных и системных глюкокортикостероидов, сопровождается развитием тяжёлых обострений [3]. Доказанная на сегодняшний день молекулярная и клиническая гетерогенность БА определяет персонифицированный подход к каждому конкретному пациенту. Одним из эффективных методов патогенетической терапии БА является применение препаратов моноклональных антител, предназначенных для больных с Т2-опосредованным типом воспаления.
Омализумаб — рекомбинантное гуманизированное моноклональное антитело, связывающее свободный иммуноглобулин E (IgE) и препятствующее его взаимодействию с рецепторами тучных клеток, базофилов и других участников Т2-воспаления. В настоящее время омализумаб одобрен на территории Российской Федерации (РФ) для терапии неконтролируемой среднетяжёлой и тяжёлой атопической БА у детей старше 6 лет, хронической спонтанной крапивницы, сезонного и круглогодичного аллергического ринита у пациентов старше 12 лет, полипозного риносинусита у пациентов старше 18 лет. Лечение омализумабом пациентов с БА приводит к ослаблению симптомов заболевания, увеличению показателей функции внешнего дыхания, снижению потребности в использовании бронхолитиков, повышению качества жизни, снижает риск развития обострений и госпитализаций [4][5].
На сегодняшний день исследования по применению генно-инженерного биологического омализумаба у детей в РФ немногочисленны, что представляет необходимость дальнейшего изучения данной темы.
В статье представлены результаты собственного наблюдения детей со среднетяжёлой и тяжёлой неконтролируемой БА, получающих терапию препаратом омализумаб.
Цель исследования — оценить клиническую эффективность таргетной терапии препаратом омализумабом у детей со среднетяжёлой и тяжёлой неконтролируемой бронхиальной астмой.
Материалы и методы
Проведено наблюдательное исследование без группы сравнения. Наблюдение проводили в период с марта 2019 г. по март 2022 г. Объектом исследования стали 7 детей со среднетяжёлой и тяжёлой неконтролируемой бронхиальной астмой, получающих базисную противовоспалительную терапию омализумабом в условиях стационара и поликлиники ГБУЗ РБ Городская детская клиническая больница №17 г. Уфы. Диагноз «Бронхиальная астма» был поставлен в соответствии с клиническими рекомендациями «Бронхиальная астма» (Москва, 2021) [6]. Определение степени тяжести и уровня контроля бронхиальной астмы проводилось в соответствии с общепринятыми классификациями [6][7].
Критериями включения в исследование стали следующие: 1) возраст детей от 6 до 18 лет; 2) масса тела более 20 кг; 3) среднетяжёлая и тяжёлая неконтролируемая БА; 4) доказанная атопическая этиология заболевания; 5) повышенный исходный уровень сывороточного IgE; 6) отсутствие противопоказаний к анти-IgE терапии. Критерии исключения из исследования следующие: 1) возраст младше 6 и старше 18 лет; 2) масса тела менее 20 кг; 3) лёгкая и среднетёжелая БА, хорошо контролируемая 1–4 ступенями терапии; 4) недоказанная атопическая этиология заболевания; 5) нормальный или очень высокий исходный уровень сывороточного IgE, более 1500 МЕ/мл; 6) наличие противопоказаний к анти-IgE терапии.
Все пациенты в настоящем исследовании получали генно-инженерный биологический препарат — омализумаб. В соответствии с инструкцией по применению доза и режим введения препарата определялись при первых обращении/госпитализации пациентов, доза препарата рассчитывалась исходя из массы тела ребенка и исходного уровня сывороточного IgE. Введение омализумаба осуществлялось подкожно 1 раз в 2 или 4 недели.
У всех исследуемых детей изучались анамнез жизни и анамнез заболевания (наследственная предрасположенность, длительность и степень тяжести БА, частота и тяжесть обострений, объём базисной противовоспалительной терапии, наличие сопутствующей аллергологической патологии), результаты инструментальных (спирография) и лабораторных методов исследования (уровень сывороточного IgE, клинический анализ крови с определением числа эозинофилов), специфической аллергологической диагностики (определение аллергенспецифических иммуноглобулинов E, кожные аллергологические пробы). Для оценки контроля БА исследуемым был предложен вопросник-тест по контролю над астмой (Asthma Control test, ACT), предназначенный для подростков старше 12 лет и взрослых, тест по контролю над астмой у детей (Children Asthma Control test, c-АСТ), предназначенный для детей в возрасте от 4 до 11 лет (до лечения и на фоне терапии омализумабом).
Статистическая обработка полученных результатов исследования проводилась с использованием пакета прикладных программ «Statistica 10.0». Для статистического анализа применялись методы для малых выборок (U-критерий Манна-Уитни, Фишера). Для сравнения двух независимых переменных применялся t-критерий Вилкоксона. Для определения взаимосвязи отдельных количественных признаков использовался критерий ранговой корреляции Спирмена. Непрерывные переменные были представлены в виде медианы и интерквартильного размаха (25 %-й и 75 5-й квартили): Me [Q1; Q3]. Результаты считались статистически значимыми при p <0,05.
Результаты
Среди исследуемых детей было 5 девочек (71,43 %), 2 мальчиков (28,57 %), средний возраст — 12,86 [ 9; 17] лет.
У 3 детей (42,86 %) была установлена среднетяжёлая, у четырех (57,14 %) — тяжёлая персистирующая бронхиальная астма. Отсутствие контроля над заболеванием наблюдалось у всех исследуемых пациентов, при этом для лечения использовались 3–4 ступени базисной противовоспалительной терапии (средние/высокие дозы ингаляционных глюкокортикостероидов (ИГКС) в комбинации с длительно действующими β2-агонистами (ДДБА) и/или антагонистами лейкотриеновых рецепторов (АЛР)). Оценка контроля БА осуществлялась при условии высокой приверженности терапии и правильной технике ингаляций.
Средняя длительность заболевания БА у исследуемых детей составила 10 [ 3; 14] лет. При этом лабораторно была доказана атопическая природа заболевания. Поливалентная сенсибилизация (по результатам определения аллергенспецифических IgE и кожных аллергологических проб) была выявлена у 100 % исследуемых: бытовая и пыльцевая — у 85,71 %, эпидермальная — у 71,43 %, пищевая — у 28,57 % детей. Наличие грибковой сенсибилизации установлено не было. Отягощённый аллергологический анамнез имел место у 6 исследуемых детей (85,71 %): со стороны матери — 42,86 %, отца — 28,57 %, родственников 2-й линии — 14,29 %. Неудовлетворительные условия проживания отмечены у 85,71 % детей, которые были обусловлены наличием мягкой мебели (85,71 %), книг на открытых полках (85,71 %), цветов (85,71 %), ковров и паласов (28,57 %), перьевых подушек (28,57 %), тараканов (28,57 %), домашних животных (27,14 %), сырости и плесени (14,29 %) в жилом помещении.
В качестве триггерных факторов обострения БА у детей были отмечены респираторные инфекции дыхательных путей (100 %), контакт с аллергеном (100 %), физическая нагрузка (85,71 %), изменение метеоусловий (85,71 %).
Анализ сопутствующей аллергологической патологии показал: аллергический ринит и атопический дерматит сопутствовали бронхиальной астме у 100 % детей, аллергическая крапивница составила 28,57 %, аллергический конъюнктивит — 14,29 %.
У всех исследуемых детей отмечалось повышение уровня общего IgE в сыворотке крови, что является условием, обязательным для проведения терапии препаратом рекомбинантных гуманизированных моноклональных антител против IgE — омализумабом. Средний уровень сывороточного IgE у детей составил 397,0 [ 225; 665,5] МЕ/мл. Средняя доза препарата Омализумаб у детей составила 300 [ 300; 450] мг, (табл. 1).
Таблица / Table 1
Доза омализумаба у исследуемых детей исходя из массы тела и исходного уровня сывороточного IgE, мг
The dose of omalizumab in the studied children, based on body weight and baseline serum IgE level, mg
|
Исходный уровень сывороточного IgE (МЕ/мл) Baseline serum IgE level (ME/ml) |
Масса тела (кг) Body weight (kg) |
||||||
|
23 |
28 |
34 |
46 |
46 |
56 |
57 |
|
|
475 |
300мг |
|
|
|
|
|
|
|
225 |
|
150мг |
|
|
|
|
|
|
847 |
|
|
600мг |
|
|
|
|
|
200 |
|
|
|
300мг |
|
|
|
|
397 |
|
|
|
|
450мг |
|
|
|
300 |
|
|
|
|
|
300мг |
|
|
655,5 |
|
|
|
|
|
|
300мг |
Длительность терапии омализумабом у детей с БА составила в среднем 13 [ 10; 35] месяцев.
Определение контроля бронхиальной астмы у исследуемых детей показало, что на фоне терапии омализумабом отмечалось значимое уменьшение частоты дневных симптомов (Z=2,3664; p=0,0179), уменьшение частоты ночных симптомов (Z=2,2678; p=0,0233), повышение физической активности (Z=2,3664; p=0,0179), уменьшение потребности в бронхолитиках (Z=2,3664; p=0,0179). Эффективность терапии омализумабом подтверждалась достоверным увеличением объёма форсированного выдоха (ОФВ1) у детей, по данным спирографии: до терапии ОФВ1 составил 86 [ 78; 92] %, на фоне терапии — 88 [ 86; 95] % (Z=2,0226; p=0,0431). Важно отметить, что на фоне лечения омализумабом удалось уменьшить объём базисной противовоспалительной терапии со снижением дозы ИГКС у 71,43 % пациентов (5 детей), Z=2,0284, p=0,0425.
Об улучшении контроля над заболеванием на фоне проводимой терапии омализумабом свидетельствовало значимое повышение количества баллов АСТ и с-АСТ тестов у всех обследованных детей: до начала лечения средние показатели тестов составили 12 [ 10; 13] баллов, на фоне лечения — 23 [ 20; 25] баллов (p=0,0277) (рис. 1).
По результату с-АСТ теста, предложенного детям в возрасте от 6 до 11 лет (n=3), на фоне терапии омализумабом сумма баллов у всех пациентов составила от 20 до 23 (наличие контроля). АСТ тест у детей старше 12 лет (n=4) показал, что на фоне терапии омализумабом у одного ребенка наблюдался полный контроль, у двоих — частичный контроль, у одного ребенка астму не удавалось достаточно контролировать.
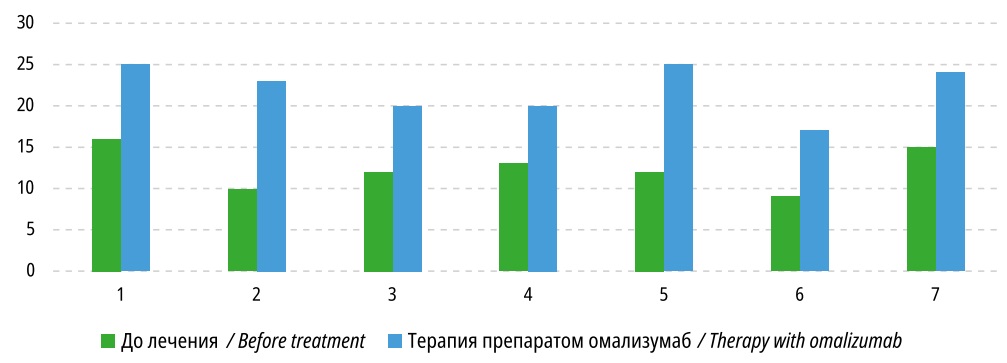
Рисунок 1. Результаты АСТ, с-АСТ теста у детей на фоне терапии омализумабом, баллы (p<0,05)
Figure 1. Results of AST, c-AST test in children with omalizumab therapy, scores (p<0.05)
На фоне терапии омализумабом также отмечалось улучшение клинического течения сопутствующей аллергологической патологии: полное отсутствие симптомов аллергического ринита (ремиссия) отмечалось у 85,71 % детей, атопического дерматита — у 42,86 %.
Важно отметить, что изучение зависимости длительности терапии омализумабом (мес.) не выявило статистически значимых взаимосвязей с результатом АСТ и с-АСТ тестов (m= -0,1272; p>0,05), частотой обострений (m= -0,1443; p>0,05), дневных симптомов (m= 0,1443; p>0,05), ночных симптомов (m= 0,4743; p>0,05), потребностью в бронхолитиках (m= 0,0398) на фоне лечения.
Анализ результатов клинических анализов крови и мочи, биохимического анализа крови во время лечения не выявил отклонений от возрастных норм. Исключение составило повышение уровня эозинофилов периферической крови у всех исследуемых пациентов, средний уровень эозинофилов крови составил 7 [ 6; 10] %.
За период наблюдения терапии препаратом омализумаб не было выявлено серьёзных нежелательных реакций. У одного ребенка (14,29 %) наблюдались местные реакции в виде гиперемии в области инъекции, которые не требовали отмены препарата.
Обсуждение
БА является одним из самых распространённых хронических гетерогенных заболеваний дыхательных путей. Основной целью терапии БА является достижение контроля заболевания. Большинство больных БА хорошо отвечают на традиционную противовоспалительную терапию, однако в общей структуре заболевания от 5 до 10% больных остаётся рефрактерными к стандартной базисной противовоспалительной терапии [8]. При современном ведении больных БА необходим глубокий анализ факторов риска с учётом клинических и биологических фенотипов и эндотипов болезни.
Более 80% всех случаев заболевания у детей приходится на аллергическую IgE-опосредованную БА [9]. Ключевыми медиаторами воспаления при атопической БА являются иммуноглобулины класса E, при этом наследственная предрасположенность к гиперпродукции IgE является важным условием формирования атопического заболевания [10]. Результаты проведённого нами исследования показали высокую частоту отягощённого семейного аллергологического анамнеза у детей с атопической БА (85,71%).
Как свидетельствуют многочисленные исследования, БА у детей сопровождается плохим контролем заболевания из-за ряда факторов. Так, например, результаты клинических исследований ENFUMOSA [4] и TENOR [5] показывают, что наличие сенсибилизации к аэроаллергенам у 50–90% пациентов препятствует достижению контроля БА. В нашем исследовании сенсибилизация к аэроаллергенам (бытовым и пыльцевым) была установлена у 85,71% детей, к эпидермальным — у 71,43 %. При этом неудовлетворительные условия проживания отмечены у 85,71% детей (наличие в жилом помещении мягкой мебели, ковров и паласов, книг на открытых полках, цветов и домашних животных). В ряде исследований также было показано, что причиной отсутствия контроля БА может быть наличие коморбидных атопических заболеваний [6][7]. Аналогичные данные были получены и в нашем наблюдении, где была установлена высокая частота коморбидной аллергической патологии (аллергический ринит, атопический дерматит, аллергическая крапивница, аллергический конъюнктивит) у всех исследуемых детей (100 %). Одним из самых распространённых факторов, способствующих развитию обострений БА у детей, являются вирусные инфекции дыхательных путей, которые в сочетании с атопией являются неблагоприятным фактором в достижении контроля [11]. По нашим данным, респираторные инфекции служили триггерным фактором обострения болезни у всех исследуемых детей с неконтролируемой БА (100%).
Таким образом, в нашем исследовании наличие наследственной предрасположенности к гиперпродукции IgE, доказанная сенсибилизация к аллергенам, повышенный уровень сывороточного IgE и неконтролируемое течение заболевания стали показанием для назначения препарата гуманизированных моноклональных антител против IgE-омализумаба у детей со среднетяжёлой и тяжёлой БА. В соответствии с повышенным исходным уровнем сывороточного IgE (397,0 [225; 665,5] МЕ/мл) доза омализумаба у детей составила 300 [ 300; 450] мг, длительность терапии — 13 [ 10; 35] месяцев.
Результаты проведённого нами исследования показали, что омализумаб является клинически эффективным при среднетяжёлой и тяжёлой неконтролируемой БА у детей и сопровождается значимым уменьшением частоты дневных и ночных симптомов, повышением физической активности, уменьшением потребности в бронхолитиках, то есть достижением контроля заболевания. Доказательства эффективности омализумаба в лечении больных с аллергической БА продемонстрированы в клинических исследованиях и систематических обзорах, результаты которых также показывают, что применение омализумаба у пациентов с тяжёлой БА сопровождается значимым снижением частоты обострений, увеличением числа пациентов с возможностью снижения или отмены ИГКС, уменьшением потребности в бронхолитиках и в целом улучшения контроля БА [12][13].
Результаты исследований российских авторов демонстрируют эффективность и безопасность длительной терапии омализумабом (более 4 лет) у 47 детей с тяжёлой персистирующей неконтролируемой БА [14], которые показывают, что на фоне терапии омализумабом снижается частота значимых тяжёлых обострений через 6 месяцев с начала лечения, уменьшается количество ежедневных симптомов и потребность в препаратах неотложной помощи (в 15,78 раз/мес.). В этом же исследовании показана положительная динамика показателей функции лёгких и сокращение базисной терапии ИГКС через четыре года терапии. В нашем исследовании эффективность терапии омализумабом подтверждалась достоверным увеличением ОФВ1 с 86 [ 78; 92] % до 88 [ 86; 95] % на фоне лечения. По результатам нашего наблюдения, на фоне лечения омализумабом объём базисной противовоспалительной терапии с применением ИГКС уменьшился у 71,43% детей.
Важным показателем в оценке уровня контроля БА является субъективная оценка пациентов. По нашим данным, до начала терапии омализумабом средний показатель АСТ и с-АСТ тестов был 12 баллов (14 [ 10; 13]), что соответствовало неконтролируемому течению бронхиальной астмы. По результату с-АСТ теста, на фоне терапии омализумабом сумма баллов составила от 20 до 23 (наличие контроля). АСТ тест показал, что на фоне терапии омализумабом у 25 % детей отмечался полный контроль, у 50 % — частичный контроль, у 25 % (1 пациент с тяжелой БА) астму не удавалось достаточно контролировать. По нашему мнению, с одной стороны, причиной отсутствия контроля БА у этого пациента являлось нерегулярное применение препаратов базисной противовоспалительной терапии. С другой стороны, при рефрактерной БА в дыхательных путях наряду с воспалительной реакцией развиваются структурные изменения (ремоделирование бронхов), которые сопровождаются необратимой обструкцией дыхательных путей [15]. Важное значение в этом случае имеет длительность заболевания, которая у детей в нашем исследовании составила в среднем 10 лет.
При этом в нашем исследовании не было выявлено значимых корреляционных взаимосвязей длительности БА с частотой обострений, потребностью в бронхолитиках и результатами АСТ и с-АСТ тестов, что свидетельствует об эффективности лечения омализумабом уже с первых месяцев терапии.
Таким образом, эффективность и безопасность омализумаба подтверждаются как в условиях реальной клинической практики в многоцентровых исследованиях [16], так и в рандомизированных клинических наблюдениях [17,18].
Заключение
Таргетная терапия с применением омализумаба является клинически эффективной у пациентов с резистентной к традиционной терапии бронхиальной астмой. Результаты собственного наблюдения показывают значимое уменьшение частоты дневных симптомов, ночных симптомов, уменьшение потребности в препаратах неотложной помощи, повышение физической активности, увеличение объема ОФВ1, по данным спирографии, уменьшение объёма базисной противовоспалительной терапии, достижение контроля бронхиальной астмы по результатам АСТ и с-АСТ тестов на фоне применения омализумаба в терапии среднетяжёлой и тяжёлой неконтролируемой БА у детей.
1. Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention. 2018. Global Initiative for Asthma (GINA). Available from: http://www.ginasthma.org
Список литературы
1. Национальная программа: Бронхиальная астма у детей. Стратегия лечения и профилактика. 5-е изд., перераб. и доп. М.: Оригинал-макет; 2017.
2. Колбин А. С., Намазова-Баранова Л. С., Вишнёва Е. А., Фролов М. Ю., Галанкин Т. Л. и др. Фармакоэкономический анализ применения омализумаба у детей, больных тяжелой неконтролируемой бронхиальной астмой: данные реальной клинической практики в России. Педиатрическая фармакология. 2016;13 (4): 345–353. DOI: 10.15690/pf.v13i4.1606.
3. Ненашева Н.М., Аверьянов А.В., Ильина Н.И., Авдеев С.Н., Осипова Г.Л. и др. Сравнительное изучение клинической эффективности биоаналогичного препарата Генолар® по результатам рандомизированного клинического исследования III фазы. Пульмонология. 2020;30(6): 782–796. DOI: 10.18093/0869-0189-2020-30-6-782-796.
4. Molimard M., Mala L., Bourdeix I., Le Gros V. Observational study in severe asthmatic patients after discontinuation of omalizumab for good asthma control. Respir Med. 2014;108(4):571–576. DOI: 10.1016/j. rmed.2014.02.003.
5. Козлов В.А., Савченко А.А. Кудрявцев И.В., Козлов И.Г., Кудлай Д.А., Продеус А.Р., Борисов А.Г. Клиническая иммунология. Красноярск. Поликор; 2020. 386 с. DOI: 10.17513/np.438
6. Клинические рекомендации. Бронхиальная астма. – Москва, 2021.
7. Клинические рекомендации. Бронхиальная астма у детей. – Москва, 2019.
8. Bousquet J., Mantzouranis E., Cruz A.A. et al. Uniform definition of asthma severity, control, and exacerbations: document presented for the World Health Organization Consultation on Severe Asthma. J. Allergy Clin. Immunol. 2010; 126 (5): 926–938. DOI: 10.1016/j.jaci.2010.07.019.
9. Wenzel S. Severe asthma: from characteristics to phenotypes to endotypes. Clin. Exp. Allergy. 2012; 42 (5): 650–658. DOI: 10.1111/j.1365-2222.2011.03929.x.
10. Княжеская Н.П., Анаев Э.Х., Белевский А.С., Камелева А.А., Сафошкина Е.В., Кириченко Н.Д. Омализумаб и модификация естественного течения бронхиальной астмы. Медицинский совет. 2021;(16):17–25. DOI: 10.21518/2079-701X-2021-16-17-25
11. Heymann P.W., Platts-Mills T.A.E., Woodfolk J.A., Borish L., Murphy D.D., Carper H.T. et al. Understanding the asthmatic response to an experimental rhinovirus infection: Exploring the effects of blocking IgE. J Allergy Clin Immunol. 2020;146(3):545–554. DOI: 10.1016/j.jaci.2020.01.035
12. Rodrigo G.J., Neffen H., Castro-Rodriguez J.A. Efficacy and safety of subcutaneous omalizumab vs placebo as addon therapy to corticosteroids for children and adults with asthma: a systematic review. Chest. 2011; 139 (1): 28–35. DOI: 10.1378/chest.10-1194.
13. Hanania N.A., Alpan O., Hamilos D.L. et al. Omalizumab in severe allergic asthma inadequately controlled with standard therapy: a randomized trial. Ann. Intern. Med. 2011; 154 (9): 573–582. DOI: 10.7326/0003-4819-154-9-20110 5030-00002.
14. Вишнёва Е.А., Намазова-Баранова Л.С., Добрынина Е.А., Алексеева А.А., Смирнов В.И., Левина Ю.Г и др. Длительный курс терапии омализумабом у детей с тяжелой персистирующей неконтролируемой бронхиальной астмой: оценка результатов по данным локального регистра. Педиатрическая фармакология. 2018; 15 (2): 149–158. DOI: 10.15690/pf.v15i2.1877
15. Авдеев С.Н., Ненашева Н.М., Жуденков К.В., Петраковская В.А., Изюмова Г.В. Распространенность, заболеваемость, фенотипы и другие характеристики тяжелой бронхиальной астмы в Российской Федерации. Пульмонология. 2018; 28 (3): 341–358. DOI: 10.18093/0869-0189-2018-28-3-341-358
16. Niven RM, Saralaya D, Chaudhuri R, et al. Impact of omalizumab on treatment of severe allergic asthma in UK clinical practice: a UK multicentre observational study (the APEX II study). BMJ Open. 2016;6(8):e011857. DOI: 10.1136/bmjopen-2016-011857.
17. Kupryś-Lipińska I, Majak P, Molinska J, Kuna P. Effectiveness of the Polish program for the treatment of severe allergic asthma with omalizumab: a single-center experience. BMC Pulm Med. 2016;16(1):61. DOI: 10.1186/s12890-016-0224-2.
18. Ledford D, Busse W, Trzaskoma B, et al. A randomized multicenter study evaluating Xolair persistence of response after longterm therapy. J Allergy Clin Immunol. 2017;140(1):162–169.e2. DOI: 10.1016/j.jaci.2016.08.054.
Об авторах
Р. М. ФайзуллинаРоссия
Файзуллина Резеда Мансафовна, д.м.н., профессор кафедры факультетской педиатрии с курсами педиатрии, неонатологии и симуляционным центром ИДПО
Уфа
А. В. Санникова
Россия
Санникова Анна Владимировна, к.м.н., доцент кафедры факультетской педиатрии с курсами педиатрии, неонатологии и симуляционным центром ИДПО
Уфа
З. А. Шангареева
Россия
Шангареева Зилия Асгатовна, к.м.н., доцент кафедры факультетской педиатрии с курсами педиатрии, неонатологии и симуляционным центром ИДПО
Уфа
Н. Т. Абсалямова
Россия
Абсалямова Нурсиля Талгатовна, главный врач
Уфа
Ж. А. Валеева
Россия
Валеева Жанна Александровна, к.м.н., заместитель главного врача по поликлинике
Уфа
Рецензия
Для цитирования:
Файзуллина Р.М., Санникова А.В., Шангареева З.А., Абсалямова Н.Т., Валеева Ж.А. Таргетная терапия бронхиальной астмы у детей. Медицинский вестник Юга России. 2022;13(2):134-140. https://doi.org/10.21886/2219-8075-2022-13-2-134-140
For citation:
Fayzullina R.M., Sannikova A.V., Shangareeva Z.A., Absalyamova N.T., Valeeva Zh.A. Targeted therapy of bronchial asthma in children. Medical Herald of the South of Russia. 2022;13(2):134-140. (In Russ.) https://doi.org/10.21886/2219-8075-2022-13-2-134-140







































