Перейти к:
Прогностическое значение вторичного гиперальдостеронизма у больных хронической сердечной недостаточностью с сохраненной фракцией выброса левого желудочка
https://doi.org/10.21886/2219-8075-2021-12-2-81-91
Аннотация
Цель: изучить прогностическое значение вторичного гиперальдостеронизма у больных хронической сердечной недостаточностью и сохранённой фракцией выброса. Материал и методы: проведено проспективное когортное исследование с участием 158 пациентов с хронической сердечной недостаточностью и сохранённой фракцией выброса. Исходно у всех больных определяли концентрацию альдостерона крови, гиперальдостеронемию диагностировали при уровне гормона > 160 пг/мл. Первичной конечной точкой исследования являлась смерть от любых причин. Результаты: гиперальдостеронемия была выявлена у 59 из 158 пациентов (37,3 %). Лица с гиперальдостеронемией были моложе, чаще страдали коморбидной патологией, имели более высокий функциональный класс хронической сердечной недостаточности и уровень NT-proBNP крови (все p < 0,05). В течение в среднем 32 месяцев (28 – 38 месяцев) наблюдения умерли 50 (37,6 %) пациентов. Сердечно-сосудистая смерть была зарегистрирована у 32 (20,3 %) больных, смерть по другим причинам наступила в 18 (11,4 %) случаев. В связи с ухудшением хронической сердечной недостаточности были госпитализированы 65 (41,1 %) пациентов. Наличие гиперальдостеронемии ассоциировалось с достоверным (р < 0,05) возрастанием риска госпитализации по поводу декомпенсации хронической сердечной недостаточности (скорректированное отношение шансов (ОШ) 2,14, 95% доверительный интервал (ДИ) 1,34 – 9,68), смерти от всех причин (ОШ 1,64; 95% ДИ 1,23 – 7,65, P = 0,033) и смерти от хронической сердечной недостаточности (ОШ 1,56; 95% ДИ 1,14 – 11,3, P = 0,021). Вывод: у больных хронической сердечной недостаточностью и сохранённой фракцией выброса наличие вторичного гиперальдостеронизма является независимым предиктором госпитализации по поводу хронической сердечной недостаточности, общей смерти и смерти от хронической сердечной недостаточности. Добавление альдостерона в существующие модели прогнозирования хронической сердечной недостаточности поможет улучшить их предсказательную ценность и оптимизировать медикаментозную терапию у пациентов высокого риска.
Ключевые слова
Для цитирования:
Шевелёк А.Н. Прогностическое значение вторичного гиперальдостеронизма у больных хронической сердечной недостаточностью с сохраненной фракцией выброса левого желудочка. Медицинский вестник Юга России. 2021;12(2):81-91. https://doi.org/10.21886/2219-8075-2021-12-2-81-91
For citation:
Shevelok A.N. Prognostic value of secondary hyperaldosteronism in patients with chronic heart failure with preserved ejection fraction. Medical Herald of the South of Russia. 2021;12(2):81-91. (In Russ.) https://doi.org/10.21886/2219-8075-2021-12-2-81-91
Введение
Хроническая сердечная недостаточность (ХСН) является одной из наиболее актуальных проблем современной кардиологии. По данным отечественных регистров, в Российской Федерации этой патологией страдают около 8 млн человек, и их количество продолжает неуклонно расти [1]. Экономические затраты на лечение пациентов с ХСН в развитых странах составляют 2 – 3% всего бюджета здравоохранения, а пятилетняя выживаемость больных не превышает 50%.
Долгое время ХСН отождествляли со снижением сократительной функции левого желудочка (ЛЖ), однако с годами стало очевидно, что значительное место в структуре заболевания занимают пациенты с сохранённой фракцией выброса (сФВ) ЛЖ. Данные исследований последних лет убедительно показывают, что тяжесть и прогноз ХСНсФВ на уровне популяции сопоставимы с ХСН с низкой ФВ (нФВ). Более того, согласно некоторым анализам, количество госпитализаций по поводу ХСНсФВ превышает таковое при ХСНнФВ [2][3]. Тревожность ситуации усугубляется неуклонно нарастающей заболеваемостью ХСНсФВ и отсутствием проверенных методов лечения в отношении снижения смертности. Всё это диктует необходимость поиска эффективных инструментов стратификации риска ХСНсФВ, которые будут способствовать оптимизации терапии и служить научным плацдармом для проведения дальнейших исследований лекарственных препаратов.
Известно, что существенный вклад в развитие и прогрессирование ХСН вносит активация ренинангиотензин-альдостероновой системы (РААС) и гиперпродукция её конечного эффектора альдостерона. Данные многочисленных исследований показывают, что увеличение плазменного уровня альдостерона приводит к значимому возрастанию риска развития инфаркта миокарда, фибрилляция предсердий, цереброваскулярных катастроф, хронической болезни почек, сердечнососудистой и общей смертности [4][5][6][7]. У пациентов с первичным альдостеронизмом кардиоваскулярная заболеваемость и смертность в несколько раз превышает таковую в общей популяции [5][8][9].
Среди больных ХСН наибольшая доказательная база прогностической значимости альдостерона и эффективности его блокаторов получена при ХСНнФВ. В то же время исследования, посвящённые роли гиперальдостеронемии у лиц с ХСНсФВ, крайне малочисленны, а применение антагонистов минералокортикоидных рецепторов с целью улучшения кардиоваскулярного прогноза этой когорты пациентов пока не увенчалось успехом. Ранее нами было доказано, что гиперальдостеронемия у пациентов с ХСНсФВ нередко возникает при длительном применении блокаторов РААС [10], будучи тесно ассоциированной с ухудшением углеводного обмена [11], развитием прогностически неблагоприятных желудочковых аритмий [12] и прогрессированием ремоделирования левого желудочка (ЛЖ) [13].
Цель исследования — оценка прогностического значения вторичного гиперальдостеронизма у больных ХСНсФВ.
Материалы и методы
Было проведено проспективное исследование с участием 158 пациентов с ХСНсФВ. Основными критериями исключения являлись первичный гиперальдостеронизм, вторичный гиперальдостеронизм почечного и печеночного генеза и приём антагонистов минералокортикоидных рецепторов в течение предшествующих 6 нед. Подробное описание критериев включения и исключения приведено в ранее опубликованной работе [11]. Все участники подписали информированное согласие. Протокол исследования и форма информированного согласия для пациентов были одобрены комиссией по вопросам биоэтики при Донецком национальном медицинском университете им. М. Горького (протокол заседания № 2 от 22.04.2016 г.).
На этапе включения у пациентов были собраны следующие данные: пол, возраст, курение (на момент исследования), функциональный класс (ФК) ХСН в соответствии с классификацией Нью-Йоркской ассоциации кардиологов (NYHA), сопутствующие заболевания, принимаемая лекарственная терапия, артериальное давление (АД), индекс массы тела, основные лабораторные и эхокардиографические показатели.
Лабораторные анализы включали оценку уровня альдостерона, гемоглобина, натрия, креатинина, NT-proBNP, холестерина липопротеинов низкой плотности (ХСЛПНП), глюкозы натощак, гликозилированного гемоглобина (HbA1c) и калия крови.
Концентрацию альдостерона измеряли иммуноферментным методом на фотометре «Multiskan» (Thermo Electron, Германия) с использованием тест-систем DRG (Германия), при этом забор крови выполняли после 30-минутного отдыха в положении лёжа натощак утром в течение 2 – 3 часов после пробуждения. Гиперальдостеронемия диагностировалась при плазменном уровне гормона, превышающем верхнюю границу референтного интервала (> 160 пг/мл). Уровень креатинина сыворотки крови определяли кинетическим методом Яффе. Скорость клубочковой фильтрации (СКФ) рассчитывали по формуле CKD-EPI (Chronic Kidney Desease Epidemiology Collaboration).
Уровень NT-proBNP определяли с помощью количественного иммунологического теста на аппарате Cardiac Reader («Roche», Германия) с использованием стандартных наборов (Roche Diagnostics). Пороговым значением NTproBNP для верификации диагноза ХСН считали 125 пг/ мл. Определение уровня глюкозы венозной крови проводили натощак колориметрическим глюкозоксидазным методом, HbA1c — турбидиметрическим методом, ХСЛПНП — с помощью прямого энзиматического метода на анализаторе Olympus 480 (Beckman Coulter, США). Уровень калия в сыворотке крови оценивали с помощью ион-селективных электродов на автоматическом биохимическом анализаторе «Cobas C 311» (Roche Diagnostics, Германия).
Трансторакальная эхокардиография выполнялась в М-модальном, двухмерном и допплеровском режимах на системе ультразвукового исследования сердца «Aplio MX SSA-780 A» (Toshiba Medical Systems Corporation, Япония) в положении больного на левом боку или спине. Исследования проводились в левой парастернальной позиции по длинной и короткой осям, а также в апикальной четырёх- и двухкамерной позициях. Определяли объём левого предсердия, индексированный к площади поверхности тела, конечно-диастолический и конечносистолический объемы, ФВ ЛЖ, толщину задней стенки ЛЖ в диастолу, толщину межжелудочковой перегородки, относительную толщину стенок ЛЖ и индекс массы миокарда ЛЖ. Гипертрофию ЛЖ диагностировали при индексе массы миокарда ЛЖ ≥ 115 г/м2 у мужчин и ≥ 95 г/м2 у женщин.
Состояние диастолической функции ЛЖ оценивалось с помощью импульсного допплеровского исследования трансмитрального кровотока и тканевого допплеровского исследования диастолического подъема основания ЛЖ. При этом определялись показатели максимальных скоростей раннего диастолического наполнения (Е) и наполнения в систолу предсердий (А), септальной и латеральной скорости движения кольца митрального клапана (e’), индексированного объёма левого предсердия и максимальной скорости трикуспидальной регургитации. Диастолическую дисфункцию ЛЖ диагностировали при наличии у пациента как минимум трёх из следующих признаков:
- скорости движения кольца митрального клапана e’ (септальная e’ <7 см/сек и латеральная e’ <10 см/ сек);
- отношения скорости E митрального потока к средней скорости движения митрального кольца E/e’ср (>14);
- индекса объёма левого предсердия (>34 мл/кв. м);
- максимальной скорости трикуспидальной регургитации (>2,8 м/сек).
После исходного обследования проводилось наблюдение за пациентами, при этом первичной конечной точкой исследования являлась смерть от любых причин. Больные наблюдались до истечения 36 мес. с момента включения или смерти в зависимости от того, что наступило раньше. Вторичными конечными точками исследования считали сердечно-сосудистую смерть, смерть, не связанную с сердечно-сосудистыми заболеваниями, госпитализацию в связи с декомпенсацией ХСН, изменение ФК ХСН и значимое снижение ФВ ЛЖ.
Определение факта госпитализации по поводу ХСН и классификация причин смерти проводилось двумя независимыми опытными клиницистами на основании медицинской документации и / или свидетельства о смерти. В случае разногласий окончательное решение принималось третьим клиницистом. Смертность от сердечно-сосудистых заболеваний была дополнительно классифицирована как смерть от фатального инфаркта миокарда, ХСН и других причин (внезапная сердечная смерть, смерть от инсульта, смерть после кардиохирургического вмешательства). Внезапная сердечная смерть была определена как внезапная неожиданная смерть либо смерть в течение 1 часа после появления симптомов. Не сердечно-сосудистая смертность была классифицирована как смерть от фатальной инфекции, злокачественных новобразований и других причин.
Оценку ФК ХСН и ФВ ЛЖ проводили у выживших пациентов спустя 36 мес. от начала исследования. Значимым снижением ФВ ЛЖ считали переход пациента их категории сФВ в категорию промежуточной ФВ (пФВ) либо нФВ. Статистический анализ результатов выполняли на персональном компьютере с помощью программного обеспечения «Jamovi 1.2.2». Категориальные данные выражали в процентах, непрерывные — как среднее значение и стандартное отклонение (М ± SD) либо как медиану и интерквартильные интервалы (Me (Q1 -Q3 ). Сравнения между группами проводились с использованием t-критерия Стьюдента при нормальном законе распределения данных и с помощью критерия Вилкоксона при отличном от нормального. Для сравнения категориальных величин применяли метод анализа таблиц сопряжённости с использованием критерия χ2 . Для выявления факторов, связанных с гиперальдостеронемией, использовался однофакторный и многофакторный пошаговые линейные регрессионные анализы. Взаимосвязь между признаками выражалась через отношение шансов (ОШ) с 95%-ным доверительным интервалом (ДИ) и V-критерий Крамера.
Статистически значимыми различия считались при уровне р < 0,05.
Результаты
При исходном лабораторном исследовании гиперальдостеронемия была выявлена у 59 из 158 пациентов (37,3 %, 95 % ДИ: 30,0 – 45,0 %). Между пациентами с повышенным и нормальным уровнем альдостерона были выявлены достоверные различия по возрасту, ФК ХСН, распространённости сопутствующих состояний, структурным параметрам миокарда и уровню лабораторных показателей (табл. 1).
Таблица / Таble 1
Клиническая характеристика пациентов
Clinical characteristic of patients
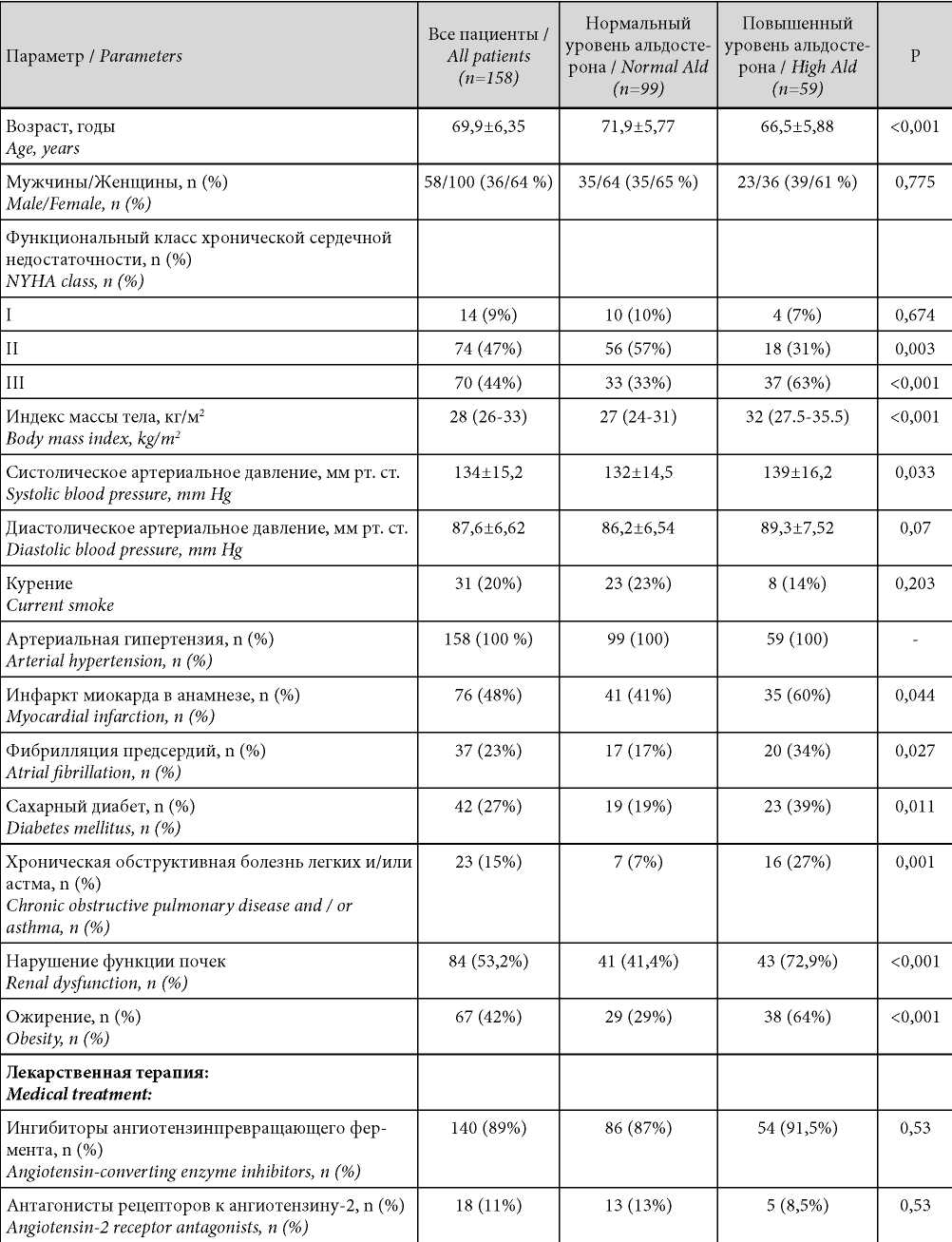
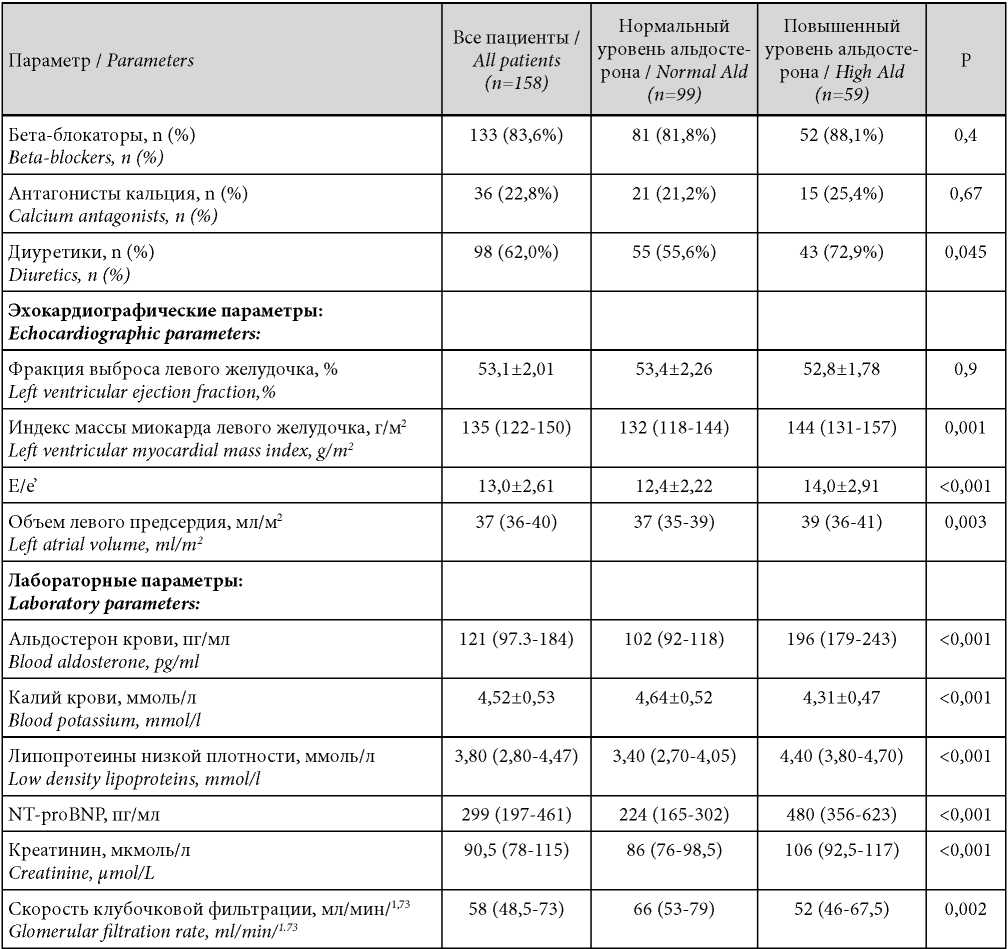
Примечание: непрерывные данные приводятся как среднее значение и стандартное отклонение (М ± SD) либо как медиана и интерквартильные интервалы (Me (Q1-Q3); р — различия между пациентами с нормальным и повышенным уровнем альдостерона.
Note: continuous data are given as the mean and standard deviation (M ± SD) or as median and interquartile intervals (Me (Q1-Q3); p — differences between patients with normal and high aldosterone levels.
Медиана периода наблюдения составила 32 месяца (28 – 38 месяцев), в течение которых умерли 50 (37,6 %) пациентов. Сердечно-сосудистая смерть была зарегистрирована у 32 (20,3 %) больных, смерть по другим причинам наступила в 18 (11,4 %) случаев. В связи с ухудшением ХСН были госпитализированы 65 (41,1%) пациентов. Детальная характеристика исходов представлена в табл. 2.
Таблица / Таble 2
Характеристика исходов в группах, n (%)
Outcomes in groups, n (%)
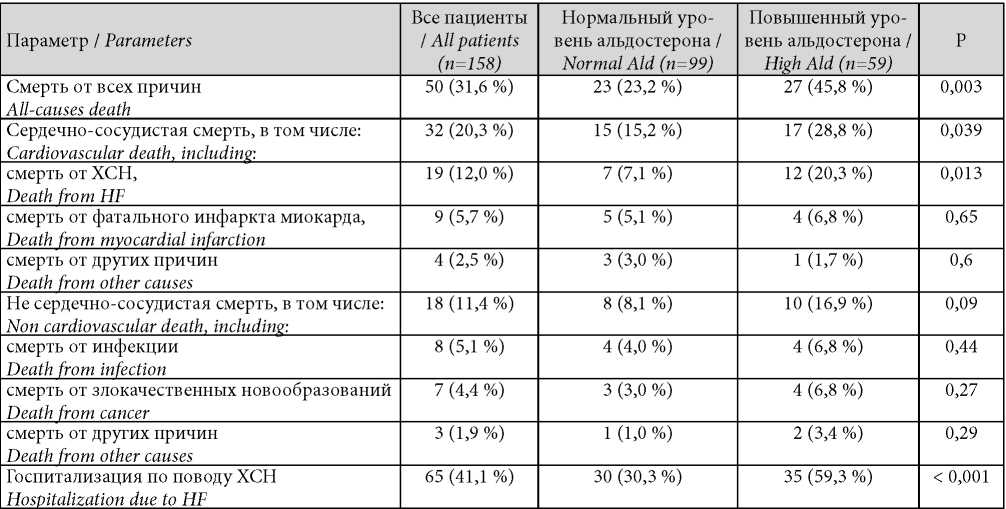
Сравнительный анализ показал, что лица с гиперальдостеронемией чаще госпитализировались по поводу декомпенсации ХСН и имели худшую выживаемость по сравнению с больными с исходно нормальным уровнем альдостерона. Детальный анализ причин летальных исходов определил, что различия в уровне общей смертности достигались только за счёт случаев сердечно-сосудистой смерти, в то время как смертность по другим причинам достоверно не различалась между группами. Наиболее частой причиной сердечно-сосудистой смерти была ХСН, в свою очередь различия в частоте фатального инфаркта миокарда и других фатальных кардиоваскулярных событий не достигли статистической достоверности (табл. 3). Анализ конкретных причин не сердечно-сосудистой смерти также показал отсутствие статистически значимых связей с уровнем альдостерона.
Таблица / Таble 3
Динамика функционального класса ХСН и фракции выброса левого желудочка к концу периода наблюдения
Changes in functional class of chronic heart failure and left ventricular ejection fraction at the end of follow-up
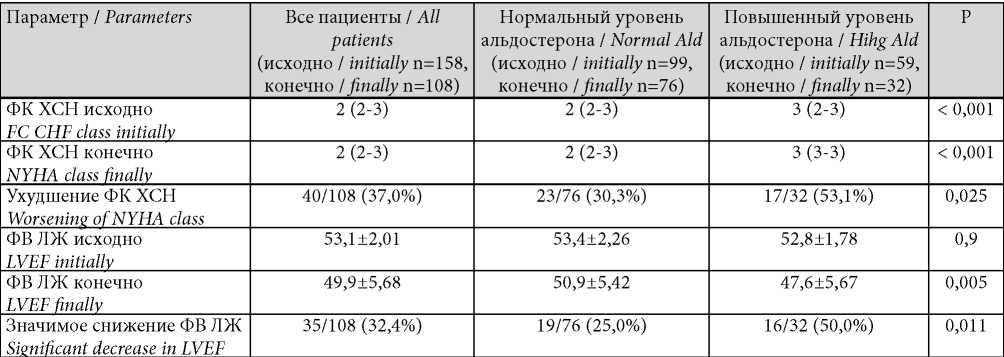
Примечание: ЛЖ — левый желудочек, ФВ — фракция выброса, ФК — функциональный класс, ХСН — хроническая сердечная недостаточность. ДЛЯ ПЕРЕВОДАНепрерывные данные приводятся как среднее значение и стандартное отклонение (М ± SD) либо как медиана и интерквартильные интервалы (Me (Q1-Q3); категориальные данные приводятся как абсолютное число пациентов с событием по отношению к общему числу пациентов в группе и их процентная доля; р — различия между пациентами с нормальным и повышенным уровнем альдостерона.
Note: LVEF — left ventricular ejection fraction; FC CHF — functional class of chronic heart failure. Continuous data are given as the mean and standard deviation (M ± SD) or as median and interquartile intervals (Me (Q1-Q3); categorical data are presented as the absolute number of patients with event in relation to the total number of patients in the group and their percentage; p — differences between patients with normal and high aldosterone levels.
Однофакторный регрессионный анализ показал, что наличие гиперальдостеронемии было достоверно связано с общей и сердечно-сосудистой смертностью, госпитализацией и смертью по причине ХСН, ухудшением ФК ХСН и снижением ФВ ЛЖ (табл. 4). Однако после поправки на возраст, коморбидные состояния, принимаемую терапию, эхокардиографические параметры и уровень биомаркеров взаимосвязь между высоким уровнем альдостерона крови и сердечно-сосудистой смертностью в целом была утрачена. По сравнению с лицами с нормальным уровнем альдостерона наличие гиперальдостеронемии ассоциировалось с достоверным возрастанием риска смерти от всех причин (скорректированное ОШ 1,64; 95% ДИ 1,23 – 7,65, P = 0,033), сердечно-сосудистой смерти (ОШ 1,86; 95% ДИ 1,02 – 6,97, P = 0,046) и смерти от ХСН (ОШ 1,56; 95% ДИ 1,14 – 11,3, P = 0,021). В многофакторной модели сохранялось значимое влияние гиперальдостеронемии и на течение ХСН, в частности на госпитализации по поводу декомпенсации заболевания, прогрессирование ФК и снижение ФВ.
Таблица / Таble 4
Взаимосвязь гиперальдостеронемии с исходами и течением ХСН
Association of hyperaldosteronemia with outcomes and severity of HF

Примечание: ЛЖ — левый желудочек, ФВ — фракция выброса, ФК — функциональный класс, ХСН — хроническая сердечная недостаточность; * — приведены скорректированные отношения шансов с учетом возраста, сопутствующей патологии, принимаемой терапии, эхокардиографических показателей и уровня биомаркеров.
Note: LVEF — left ventricular ejection fraction, HF — heart failure; * — adjusted odds ratios for age, comorbidity, therapy, echocardiographic parameters, and biomarker levels are given.
Обсуждение
В настоящее время высокая прогностическая значимость плазменного уровня альдостерона убедительно продемонстрирована у пациентов с различными формами ишемической болезни сердца (ИБС) [14][15][16][17]. В исследовании OPERA [18] более высокие уровни альдостерона крови у лиц с инфарктом миокарда, даже находящиеся в пределах физиологических значений, были связаны с повышенным риском желудочковых и наджелудочковых нарушений ритма, повторного инфаркта, инсульта, ХСН и смерти. В крупном исследовании LURIC с участием более 3000 пациентов с ИБС плазменная концентрация альдостерона являлась независимым предиктором сердечно-сосудистых катастроф и смерти от всех причин даже при уровне ниже верхнего порогового значения. Анализ конкретных причин смерти показал, что альдостерон был связан с более высоким риском внезапной сердечной смерти и фатального инсульта, причем эта связь была обнаружена как у пациентов с хронической ИБС, так и у лиц с острым коронарным синдромом. У последних взаимосвязь между уровнем альдостерона и сердечно-сосудистой смертностью сохранялась даже при нормальной или минимально сниженной систолической функции ЛЖ, что подтверждает сообщения о положительном эффекте антагонистов минералокортикоидных рецепторов при инфаркте миокарда независимо от наличия систолической дисфункции [19][20]. Подробный анализ показал, что концентрации альдостерона выше 48 пг/мл, нижнего предела нормы, уже может приводить к повреждениям органов-мишеней.
В пользу важнейшей прогностической роли гиперальдостеронемии свидетельтвуют и результаты досрочно прекращенного в 2005 г. исследования ILLUMINATE [21] по оценке эффективности применения ингибитора белкапереносчика эфиров холестерина (БПЭХ) торцетрапиба. Это первый препарат данной группы, механизм действия которого направлен на повышение уровня холестерина липопротеинов высокой плотности (ХС-ЛПВП). Применение торцетрапиба у больных с сердечно-сосудистыми заболеваниями действительно приводило к увеличению уровня ХС-ЛПВП на 70%, а также к снижению концентрации ХС-ЛПНП на 25%, но сопровождалось увеличением частоты кардиоваскулярных осложнений и смертности, обусловленной повышением концентрации альдостерона крови и АД. В 2012 г. были опубликованы результаты III фазы исследования dal-OUTCOMES [22], в ходе которого оценивалась эффективность второго экспериментального препарата, относящегося к классу ингибиторов БПЭХ, далцетрапиба. Исследование также было прекращено досрочно после получения результатов промежуточного анализа, которые свидетельствовали об отсутствии снижения риска сердечно-сосудистых осложнений при приёме далцетрапиба по сравнению с плацебо, несмотря на увеличение концентрации ХС-ЛПВП почти на 30%. По мнению некоторых экспертов, одной из причин отрицательных результатов исследования могло стать небольшое, но клинически значимое повышение уровня систолического АД, возможно, вызванное гиперальдостеронемией. Влияние ингибиторов БПЭХ на уровень альдостерона не подтвердилось в исследовании ACCELERATE [23], посвящённом оценке эффективности эвацетрапиба у пациентов высокого кардиоваскулярного риска. Препарат способствовал повышению ХС-ЛПВП и снижению ХС-ЛПНП, не изменяя при этом плазменной концентрации альдостерона. Тем не менее улучшение липидного профиля не сопровождалось снижением кардиоваскулярных событий и смертности.
Доказательства неблагоприятного влияния гиперальдостеронемии на прогноз были получены и среди пациентов с ХСН. Еще в 1990 г. небольшое исследование CONSENSUS показало, что уровень альдостерона является независимым предиктором смерти у пациентов с тяжёлой декомпенсированной ХСН [24]. Дальнейшие клинические исследования подтвердили, что более высокие концентрации гормона связаны с повышенной смертностью при ХСН при длительном наблюдения, при этом риск возрастает в большей степени при сочетанном повышении уровня альдостерона и кортизола [25].
Однако проведённые на сегодняшний день исследования, посвящённые оценке влияния альдостерона на прогноз ХСН, включали либо пациентов с нФВ, либо больных с различной систолической функцией ЛЖ. Мы впервые продемонстрировали влияние альдостерона на прогноз в популяции больных ХСНсФВ. Результаты нашего исследования показали, что повышение плазменного уровня альдостерона широко распространено среди пациентов с ХСНсФВ даже вне фазы декомпенсации и регистрируется в 37% случаев. По всей видимости, оно представляет собой явление вторичного альдостеронизма, обусловленного наличием АГ, различных внекардиальных состояний (ожирение, хроническое обструктивное заболевание лёгких, почечная дисфункция, сахарный диабет), а также феноменом ускользания альдостерона из-под лекарственного контроля ингибиторами РААС. Возможные механизмы взаимосвязи между гиперальдостеронемией и сопутствующими состояниями подробно описаны нами в предыдущих публикациях [26].
Примечательно, что влияние гиперальдостеронемии на течение и исход ХСН сохранялось и после учёта таких общепринятых предикторов кардиоваскулярного прогноза, как возраст, структурные параметры миокарда и уровень некоторых биомаркеров. Это даёт основание полагать, что добавление альдостерона в существующие модели прогнозирования ХСН поможет улучшить их предсказательную ценность и оптимизировать медикаментозную терапию у пациентов высокого риска.
На сегодняшний день серьезная доказательная база для лечения пациентов с ХСНсФВ, к сожалению, отсутствует. Результаты исследования TOPCAT и данные крупных мета-анализов показывают, что антагонисты минералокортикоидных рецепторов снижают смертность и частоту госпитализаций по сердечно-сосудистым причинам только при нФВ, но не при сФВ [27][28]. В то же время известно, что ХСНсФВ представляет собой довольно разнородное по своим причинам и механизмам развития состояние. Возможно, антагонисты альдостерона действительно не докажут эффективности в улучшении прогноза в широкой популяции больных ХСНсФВ, но смогут способствовать снижению риска смерти у определённых категорий больных. Наша работа позволяет предполагать, что назначение препаратов, блокирующих минералокортикоидные рецепторы, может быть оправдано у лиц с гиперальдостеронемией, однако для проверки данной гипотезы необходимы дальнейшие исследования.
Помимо главной цели — определения прогностической значимости гиперальдостеронемии у больных ХСНсФВ — выполнение данной работы позволило решить ряд дополнительных задач. Так, нами было установлено, что трёхлетняя выживаемость больных ХСНсФВ даже при оптимальной медикаментозной терапии заболеваний, лежащих в основе, составляет 68,4%. Также было выявлено, что на протяжении 3 лет наблюдения каждый третий пациент с ХСНсФВ переходит в категорию пФВ или нФВ, а гиперальдостеронемия является независимым предиктором ухудшения систолической функции ЛЖ.
Определённым лимитирующим фактором работы стала относительно небольшая выборка пациентов, что ограничило возможность изучения взаимосвязи уровня альдостерона с рядом конкретных причин сердечнососудистой смертности, такими как внезапная сердечная смерть, инсульт, кардиохирургические вмешательства. Дальнейшие более крупные исследования позволят ответить на поставленные вопросы.
Выводы
У пациентов с ХСНсФВ повышенный уровень альдостерона крови ассоциируется с достоверным возрастанием риска госпитализаций по поводу декомпенсации заболевания, прогрессирования ХСН и нарушения систолической функции ЛЖ. Наличие гиперальдостеронемии у данной когорты больных является независимым предиктором общей, сердечно-сосудистой смерти и смерти от ХСН.
Список литературы
1. Фомин И.В. Хроническая сердечная недостаточность в Российской Федерации: что сегодня мы знаем и что должны делать. // Российский кардиологический журнал. – 2016. - №8. – С.7-13. DOI: 10.15829/1560-4071-2016-8-7-13
2. Steinberg B.A., Zhao X., Heidenreich P.A., Peterson E.D., Bhatt D.L., et al. Trends in patients hospitalized with heart failure and preserved left ventricular ejection fraction: prevalence, therapies, and outcomes. // Circulation. – 2012. – V.126(1). – P. 65-75. DOI: 10.1161/CIRCULATIONAHA.111.080770
3. Oktay A.A., Rich J.D., Shah S.J. The emerging epidemic of heart failure with preserved ejection fraction. // Curr Heart Fail Rep. – 2013. – V. 10(4). DOI: 10.1007/s11897-013-0155-7
4. Mentz R.J., Bakris G.L., Waeber B., McMurray J.J., Gheorghiade M., et al. The past, present and future of renin-angiotensin aldosterone system inhibition. // Int J Cardiol. – 2013. – V. 167(5). – P. 1677-1687. doi:10.1016/j.ijcard.2012.10.007
5. Milliez P., Girerd X., Plouin P.-F., Blacher J., Safar M.E., Mourad J.J. Evidence for an increased rate of cardiovascular events in patients with primary aldosteronism. // J Am Coll Cardiol. – 2005. – V. 45(8). – P. 1243-1248. DOI: 10.1016/j.jacc.2005.01.015
6. Murin J. Cardiovascular effects of aldosterone. // Bratisl Lek Listy. – 2005. – V. 106(1). – P. 3-19.
7. Sata M., Fukuda D. Crucial role of renin-angiotensin system in the pathogenesis of atherosclerosis. // J Med Invest. – 2010. – V. 57(1-2). – P. 12-25. DOI: 10.2152/jmi.57.12
8. Catena C., Colussi G., Nadalini E., Chiuch A., Baroselli S., et al. Cardiovascular outcomes in patients with primary aldosteronism after treatment. // Arch Intern Med. – 2008. – V. 168(1). – P. 80-85. DOI: 10.1001/archinternmed.2007.33
9. Young W.F. Primary aldosteronism: renaissance of a syndrome. // Clin Endocrinol (Oxf). – 2007. – V. 66(5). – P. 607-618. DOI: 10.1111/j.1365-2265.2007.02775.x
10. Шевелёк А.Н. Влияние терапии блокаторами ренин-ангиотензиновой системы на уровень альдостерона крови у больных хронической сердечной недостаточностью с сохраненной фракцией выброса левого желудочка. // Медицинский вестник Юга России. – 2020. – Т.11, №4. – С. 67-73. DOI: 10.21886/2219-8075-2020-11-4-67-73
11. Шевелёк А.Н. Взаимосвязь плазменных уровней альдостерона и показателей углеводного обмена при хронической сердечной недостаточности с сохраненной фракцией выброса. // Российский кардиологический журнал. – 2021. – Т.26(1). – С. 3991. DOI: 10.15829/1560-4071-2021-3991
12. Шевелёк А.Н. Взаимосвязь гиперальдостеронемии с электрофизиологической активностью миокарда у больных хронической сердечной недостаточностью с сохраненной фракцией выброса. // Архивъ внутренней медицины. – 2020. – Т.10(5). – С. 382-389. DOI: 10.20514/2226-6704-2020-10-5-382-389
13. Шевелёк А.Н. Взаимосвязь уровня альдостерона крови со структурно-функциональным состоянием левого желудочка у пациентов с хронической сердечной недостаточностью с сохраненной фракцией выброса. // Кардиоваскулярная терапия и профилактика. – 2021. – Т. 20(2). – С. 2640. DOI: 10.15829/1728-8800-2021-2640
14. Resic N., Durak-Nalbantic A., Dzubur A., Begic A., Begic E. Serum aldosterone as predictor of progression of coronary heart disease in patients without signs of heart failure after acute myocardial infarction. // Med Arch. – 2018. – V. 72(6). – P. 406-409. doi: 10.5455/medarh.2018.72.406-409
15. Mignano A., Pitruzzella V., Arnone G., Arnone M.T., Rotolo A. et al. Prognostic role of aldosterone in patients with acute coronary syndrome: short and medium term follow-up. // J Cardiovasc Med (Hagerstown). - 2014. – V. ;15(1). – P. 27-32. DOI: 10.2459/JCM.0b013e328364129c
16. Hillaert M.A., Lentjes E.G., Kemperman H., van der Graaf Y., Nathoe H.M., et al. Aldosterone, atherosclerosis and vascular events in patients with stable coronary artery disease. // Int J Cardiol. – 2013. – V. 167(5). – P. 1929-1935. DOI:10.1016/j.ijcard.2012.05.034
17. Ivanes F., Susen S., Mouquet F., Pigny P., Cuilleret F., et al. Aldosterone, mortality, and acute ischaemic events in coronary artery disease patients outside the setting of acute myocardial infarction or heart failure. // Eur Heart J. – 2012. – V. 33(2). – P. 191-202. DOI: 10.1093/eurheartj/ehr176
18. Beygui F., Montalescot G., Vicaut E., Rouanet S., Van Belle E., et al. Aldosterone and long-term outcome after myocardial infarction: A substudy of the french nationwide Observatoire sur la Prise en charge hospitalière, l’Evolution à un an et les caRactéristiques de patients présentant un infArctus du myocarde avec ou sans onde Q (OPERA) study. // Am Heart J. – 2009. – V. 157(4). – P. 680-687. DOI: 10.1016/j.ahj.2008.12.013
19. Tomaschitz A., Pilz S., Ritz E., Meinitzer A., Boehm B.O., März W. Plasma aldosterone levels are associated with increased cardiovascular mortality: the Ludwigshafen Risk and Cardiovascular Health (LURIC) study. // Eur Heart J. 2010. – V. 31(10). – P. 1237-1247. DOI: 10.1093/eurheartj/ehq019
20. Hayashi M., Tsutamoto T., Wada A., Tsutsui T., Ishii C., et al. Immediate administration of mineralocorticoid receptor antagonist spironolactone prevents post-infarct left ventricular remodeling associated with suppression of a marker of myocardial collagen synthesis in patients with first anterior acute myocardial infarction. // Circulation. – 2003. – V. 107(20). – P. 2559-2565. DOI: 10.1161/01.CIR.0000068340.96506.0F
21. Barter P.J., Caulfield M., Eriksson M., Grundy S.M., Kastelein J.J., et al. Effects of torcetrapib in patients at high risk for coronary events. // N Engl J Med. – 2007. – V. 357(21). – P. 2109-2122. DOI: 10.1056/NEJMoa0706628
22. Schwartz G.G., Olsson A.G., Abt M., Ballantyne C.M., Barter P.J., et al. Effects of dalcetrapib in patients with a recent acute coronary syndrome. // N Engl J Med. – 2012. – V. 367(22). – P. 2089-2099. DOI: 10.1056/NEJMoa1206797
23. Lincoff A.M., Nicholls S.J., Riesmeyer J.S., Barter P.J., Brewer H.B., et al. Evacetrapib and cardiovascular outcomes in high-risk vascular disease. // N Engl J Med. – 2017. – V.376(20). – P. 1933-1942. DOI: 10.1056/NEJMoa1609581
24. Swedberg K., Eneroth P., Kjekshus J., Wilhelmsen L. Hormones regulating cardiovascular function in patients with severe congestive heart failure and their relation to mortality. CONSENSUS Trial Study Group. // Circulation. – 1990. – V. 82(5). – P. 1730-1736. DOI: 10.1161/01.cir.82.5.1730
25. Güder G., Bauersachs J., Frantz S., Weismann D., Allolio B., et al. Complementary and incremental mortality risk prediction by cortisol and aldosterone in chronic heart failure. // Circulation. – 2007. – V. 115(13). – P. 1754-1761. DOI: 10.1161/CIRCULATIONAHA.106.653964
26. Ватутин Н.Т., Шевелёк А.Н. Влияние коморбидных состояний на уровень альдостерона крови у больных с хронической сердечной недостаточностью с сохраненной систолической функцией левого желудочка. // Кардиоваскулярная терапия и профилактика. – 2017. – Т.16(6). – С. 92-98. DOI: 10.15829/1728-8800-2017-6-92-98
27. Ezekowitz J.A., McAlister F.A. Aldosterone blockade and left ventricular dysfunction: a systematic review of randomized clinical trials. // Eur Heart J. – 2009. – V. 30(4). – P. 469-77. DOI: 10.1093/eurheartj/ehn543
28. Xu Y., Qiu Z., Yang R., Wu Y., Cheng X. Efficacy of mineralocorticoid receptor antagonists in postmyocardial infarction patients with or without left ventricular dysfunction: A meta-analysis of randomized controlled trials. // Medicine (Baltimore). – 2018. – V. 97(51). – P. e13690. DOI: 10.1097/MD.0000000000013690
Об авторе
А. Н. ШевелёкУкраина
Анна Николаевна Шевелёк, к.м.н., доцент, доцент кафедры госпитальной терапии, Донецкий национальный медицинский университет им. М. Горького, старший научный сотрудник отдела кардиологии и кардиохирургии Института неотложной и восстановительной хирургии им. В.К. Гусака. SPIN-код РИНЦ 8049-8539
Донецк, ДНР
Рецензия
Для цитирования:
Шевелёк А.Н. Прогностическое значение вторичного гиперальдостеронизма у больных хронической сердечной недостаточностью с сохраненной фракцией выброса левого желудочка. Медицинский вестник Юга России. 2021;12(2):81-91. https://doi.org/10.21886/2219-8075-2021-12-2-81-91
For citation:
Shevelok A.N. Prognostic value of secondary hyperaldosteronism in patients with chronic heart failure with preserved ejection fraction. Medical Herald of the South of Russia. 2021;12(2):81-91. (In Russ.) https://doi.org/10.21886/2219-8075-2021-12-2-81-91







































