Перейти к:
Коронавирусы человека, способные вызывать чрезвычайные ситуации
https://doi.org/10.21886/2219-8075-2021-12-1-14-23
Аннотация
Первый коронавирус HCoV-B814, выделенный от человека, был изолирован в 1965 г. и не сохранился до наших дней. Долгое время считалось, что коронавирусы не способны вызывать опасные для жизни заболевания. Они не входили в список особо опасных инфекций, а серьёзную проблему представляли исключительно в ветеринарии. Но с 2002 г., после вспышки тяжёлого острого респираторного синдрома, мнение ученых изменилось. Новый подтип коронавируса проник в популяцию людей и получил название SARS-CoV. В 2012 г. удалось открыть природные очаги Ближневосточного респираторного синдрома. Возникшая в конце 2019 г. эпидемия новой коронавирусной инфекции привлекла к себе внимание исследователей всего мира. Первоочередной задачей стало подробное и пристальное изучение всех разновидностей данного вируса. В данном обзоре описаны семь видов коронавирусов, способных вызывать чрезвычайные ситуации среди населения всего мира.
Ключевые слова
Для цитирования:
Кононенко А.А., Носков А.К., Водяницкая С.Ю., Подойницина О.А. Коронавирусы человека, способные вызывать чрезвычайные ситуации. Медицинский вестник Юга России. 2021;12(1):14-23. https://doi.org/10.21886/2219-8075-2021-12-1-14-23
For citation:
Kononenko A.A., Noskov A.K., Vodyanitskaya S.Yu., Podoynitsyna O.A. Human coronaviruses that can cause emergencies. Medical Herald of the South of Russia. 2021;12(1):14-23. https://doi.org/10.21886/2219-8075-2021-12-1-14-23
В 30-х гг. ХХ в. после многочисленных исследований коронавирусы были официально признаны патогенными для животных, а тридцать лет спустя были идентифицированы штаммы, способные вызывать респираторные заболевания у человека [1].
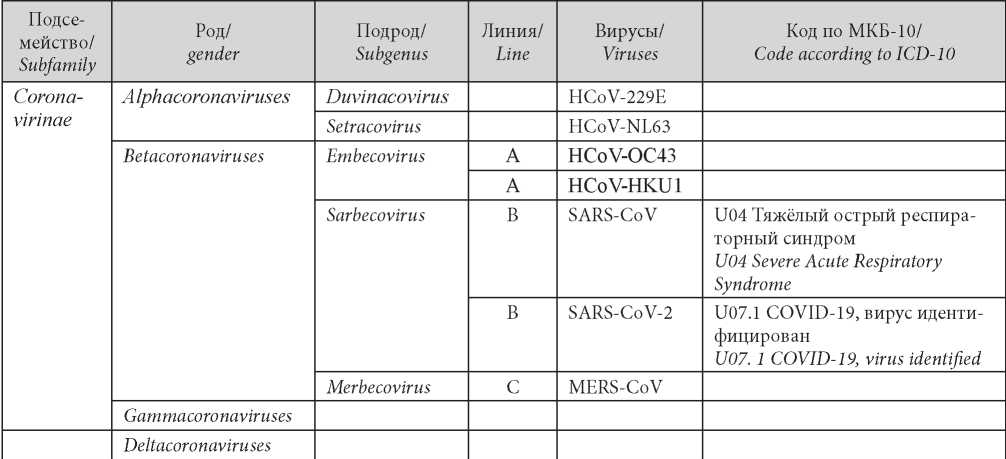
В настоящее время коронавирусы образуют самую большую группу порядка Nidovirales, включающую семейства Coronaviridae, Arteriviridae, Roniviridae и Mesoviridae. Семейство Coronaviridae состоит из двух подсемейств — Coronavirinae и Torovirinae. Коронавирусы подразделяются на четыре рода: Alphacoronaviruses, Betacoronaviruses, Gammacoronaviruses, Deltacoronaviruses. Первоначально внутри рода Betacoronavirus вирусы подразделялись на линии А, В, С и D, которые в дальнейшем были переименованы в Эмбековирус (предыдущая линия A), Сарбековирус (предыдущая линия B), Мербековирус (предыдущая линия С) и Нобековирус (предыдущая линия D) [2]. Эти четыре линии классифицируются в подроды Betacoronaviruses
Среди многочисленных представителей семейства известны семь коронавирусов, способных вызывать заболевания человека (табл. 1). Четыре вируса (HCoV229E, HCoV-NL63, HCoV-OC43 и HCoV-KHU1) являются этиологическими агентами респираторных вирусных инфекции (ОРВИ) лёгкой или среднетяжелой степени тяжести. Два вируса способны вызывать заболевания, приводящие к летальному исходу, — тяжёлый острый респираторный синдром коронавируса (SARS-CoV) и Ближневосточный респираторный синдром коронавируса (MERS-CoV). Седьмой вирус (SARS-CoV-2) — это новый коронавирус, первый случай заболевания которого диагностирован в Китае в конце 2019 г. В начале 2020 г. SARS-CoV-2 принял повсеместное распространение [3, 4].
Таблица / Table 1
Классификация вирусов Coronavirinae
Classification of Coronavirinae viruses
Коронавирусы человека HCoV-229E и HCoV-OC43
В 1965 г. учёные Д. Тирелл и М. Бино смогли впервые культивировать вирус, который был получен из дыхательных путей мальчика с обычной простудой путём пассажа в эмбриональных культурах органов трахеи человека [5][6]. А первая официальная научная публикация, посвящённая коронавирусам, датируется 16.11.1968 г., когда был представлен очередной выпуск журнала «Nature». В статье было предложено объединить эти вирусы в группу «coronaviruses» вследствие характерной морфологии вирионов 229E, OC43 с четко выраженным зубчатым (коронообразным) обрамлением (порядка 20 нм) округлых плейоморфных частиц (120–160 нм) [7].
По степени патогенности Coronaviridae были отнесены
- к IV группе патогенности, в которую вошли HCoV229E, а также многочисленные вирусы животных;
- к III группе патогенности, объединившей вирусы HCoV-OC43 и близкородственные вирусы животных [6].
По официальным данным, полученным в результате многочисленных опытов на добровольцах, которые входили в «здоровую группу», было установлено, что вирусы HCoV-229E и HCoV-OC43 приводят к обычной простуде [8][9], и с тех пор HCoVs считались условно патогенными респираторными вирусами.
Экспериментально было показано, что для HCoV229E и HCoV-OC43 характерен воздушно-капельный путь передачи. Инфицированные вирусом добровольцы выделяли его в течение 5 дней, начиная с 48 часов после заражения, что соответствовало времени появления первых симптомов заболевания [10].
Исследования показали, что заражение HCoV-229E происходило путем инокуляции слизистых оболочек дыхательных путей. Экссудация плазмы слизистой оболочки носа и повышенный уровень интерферона γ (IFNy) в образцах назофарингеального смыва напрямую зависел от тяжести симптомов [11].
Вирусная нагрузка дыхательных путей достигала максимума в течение первых трёх дней после инфицирования и резко снижалась через одну неделю, это связано с появлением приобретенного активного иммунитета у человека [12].
Начиная с 2000 гг., были обнаружены представители семейства Coronaviridae, способные вызвать тяжелые респираторные заболевания, в ряде случаев приводящие к смертельному исходу.
Коронавирус человека SARS-CoV
Первый случай заболевания, вызванного SARS-CoV, произошел в населенном пункте Шанлане, провинции Гуандун на Юге Китая в ноябре 2002 г. Передача инфекции происходила в основном в госпитальных условиях. Один больной в среднем заражал трёх-четырёх контактных лиц. Итальянский врач Карло Урбани, входивший в состав организации «Врачи без границ», первым идентифицировал наблюдаемое им заболевание как новое, не встречавшееся ранее. Карло Урбани заразился при лечении пациента с ТОРС и погиб. Штамм выделенного вируса получил название в его честь — вирус SARSrelated human coronavirus Urbani (SARS). Благодаря усилиям Карло Урбани и его коллег масштабного распространения тяжелого острого респираторного синдрома (ТОРС) удалось предотвратить [4].
В 2003 г. было показано, что возбудителем болезни является неизвестный ранее вариант коронавируса. Он был маркирован как SARS–CoV. Его геномная организация схожа с ранее изученными видами коронавирусов. Однако филогенетический анализ и сравнение последовательностей позволяют утверждать, что SARS–CoV не имеет сродства ни с одним из коронавирусов, охарактеризованным до него. Вирионы содержат плюс-цепь полиаденилированной РНК длиной 16–30 kb (коронавирусы обладают самым большим геномом, превосходящим геном других вирусов в три раза) [13]. SARS-CoV был отнесен ко III группе патогенности по классификации, принятой в РФ.
На основании проведённых исследований была выдвинута гипотеза о первичном проникновении вируса в популяции людей при употреблении в пищу мяса циветт, поскольку выделенный от этих животных коронавирус инактивировался сыворотками крови от больных SARS-CoV. [14][15].
В дальнейшем было установлено, что природные очаги вируса SARS-CoV, связаны с местами проживания отряда рукокрылых (Chiroptera), в первую очередь с летучими мышами. Также SARS-CoV-подобные вирусы были изолированы от подковоносов Rhinolophus, а также от видов, принадлежащих к другим родам в Азии (прежде всего в Китае), Африке, Австралии, Европе, Америке. Нельзя полностью исключить и прямую передачу инфекции людям через продукты жизнедеятельности летучих мышей, днёвки которых могут проходить на чердаках жилых домов [3][16].
Тяжесть болезни варьировалась от лёгкой формы до тяжёлой с летальным исходом. У большинства людей болезнь протекала в лёгкой или среднетяжёлой форме с признаками обычного ОРВИ, быстрым восстановлением организма и развитием специфического иммунитета. Однако у некоторых больных развивалась тяжёлая форма пневмонии, сопровождавшаяся острым респираторным синдромом [17][18].
Распространение заболевания было остановлено в 2003 г. высокоэффективными глобальными ответными мерами в области общественного здравоохранения, и в настоящее время SARS не циркулирует среди людей [19][20].
Но, как было отмечено ранее, коронавирусы способны эволюционировать и приспосабливаться к новым хозяевам. Вспышка атипичной пневмонии вернула коронавирусы в центр внимания, и благодаря возобновившемуся интересу к Coronaviridae были обнаружены ещё два представителя семейства, способные вызывать заболевания человека.
Коронавирусы человека HCoV-NL63 и HCoV-HKU1
В 2004 г. голландские исследователи в Нидерландах впервые выделили у семимесячного ребенка с бронхиолитом новый вирус HCoV-NL63 (Human coronavirus NL63), который был отнесён к IV группе патогенности [21][22][23].
В январе 2005 г. сотрудники Гонконгского университета выделили у 71-летнего пациента с острым респираторным заболеванием, осложнённым двусторонней пневмонией, новый коронавирус человека HKU1 (HCoV-HKU1 — Human coronavirus HKU1) [24]. Именно гонконгский университет (англ. Hong Kong University), положил начало использованию префикса HKU в классификации коронавирусов, с порядковым номером штамма, который встречается в названиях многих вирусов. Вирус HCoV-HKU1 был отнесён ко III группе патогенности.
HCoV-NL63 и HCoV-HKU1 представляли собой одноцепочечные положительные РНК-вирусы. У большинства заболевших вирусами наблюдались такие основные симптомы, как ринорея, лихорадка, кашель и свистящее дыхание, а проявления заболевания включали бронхиолит и пневмонию [25][26].
Первые случаи инфицирования здоровых людей вирусом HCoV-NL63 были зарегистрированы среди детей раннего возраста с тяжёлыми инфекциями нижних дыхательных путей в условиях стационара, в то время как
первые случаи заболевания вирусом HCoV-HKU1 были зафиксированы среди пожилых пациентов с основными сопутствующими заболеваниями в основном со стороны дыхательной и сердечно-сосудистой систем. В настоящее время вирус HCoV-HKU1 также регистрируется и у детей с острыми респираторными заболевания и с инфекциями верхних или нижних дыхательных путей [21][26].
Заболевания, вызванные вирусами HCoV-HKU1 и HCoV-NL63, как правило, не представляют угрозы для жизни, особенно у здоровых людей. Это позволило предположить, что HCoV-NL63 и HCoV-HKU1, как и HCoV-229E и HCoV-OC43 способны провоцировать заболевания с ярко выраженными клиническими симптомами лишь у детей, пожилых людей и тех, кто имели нарушения иммунной системы [27].
С 2006 по 2012 гг. продолжалось всестороннее изучение представителей семейства коронавирусов, и в июне 2012 г. мир узнал о новом, не менее опасном его представителе, который получил название MERS-CoV.
Коронавирус человека MERS-CoV
В июне 2012 г. в городе Джидда (Саудовская Аравия) врач-вирусолог Али Мохамед Заки впервые выделил новый коронавирус из мокроты пациента, погибшего от тяжелой вирусной пневмонии, осложненной острой почечной недостаточностью. По многим признакам выявленный возбудитель был сходен с SARS-CoV. Соответственно, новая инфекция получила название «Ближневосточный респираторный синдром».
Первоначально вирус MERS-CoV планировали назвать «вирус острого респираторного синдрома с почечной недостаточностью», однако быстро выяснилось, что почечная недостаточность не являлась ведущей патологией, и некоторое время использовалось не вполне удачное обозначение «новый коронавирус» (HCoVEMC/2012). В мае 2013 г. на заседании группы изучения коронавирусов при Международном комитете по таксономии вирусов было решено ввести современное номенклатурное название — MERS-CoV [28].
Несмотря на то, что передача вируса между людьми считалась не столь интенсивной, MERS-CoV вызвал две крупные вспышки — в Саудовской Аравии (в 2012 г.) и Южной Корее (в 2015 г.), где общее количество подтвержденных случаев превысило две тысячи при уровне летальности 35% [29]. У пожилых людей, особенно с сопутствующими патологиями, инфекция, вызванная MERS-CoV, имела более тяжёлое течение и нередко приводила к летальному исходу [28].
Вирус MERS-CoV представлял собой линейную несегментированную однонитевую положительную РHK. По степени патогенности вирус был отнесен ко ІI группе патогенности по классификации, принятой в Российской Федерации.
Была выдвинута гипотеза о том, что летучие мыши, возможно, являлись не единственным резервуаром MERS-CoV. Появились данные, подтверждающие возможность носительства вируса у Европейского ежа (Erinaceus europaeus). Также представляется вероятным, что резервуаром MERS-CoV могут являться верблюды [30].
Было установлено, что изолированные от верблюдов штаммы MERS-CoV были полностью идентичны таковым, выделенным от людей. Более того, специфические для MERS-CoV антитела очень часто обнаруживались у верблюдов в странах Ближнего Востока, Африки и Азии. Анти-MERS-CoV антитела были обнаружены в образцах сыворотки верблюдов, собранных еще в 1983 г., поэтому предполагается, что вирусы циркулируют у верблюдов более 30 лет.
Многие исследование официально подтвердили, что природным резервуаром MERS-CoV являлись летучие мыши (Chiroptera). Вирус, выделенный от одного из больных, оказался идентичным в молекулярно-генетическом отношении вирусу, полученному от могильного мешкокрыла (Taphozous perforatus) из семейства футлярохвостых (Emballonuridae) [31]. Летучие мыши выделяли вирус со слюной, мочой, фекалиями, которые могут стать источником заражения людей и других животных. Могильный мешкокрыл встречался не только на юге Аравийского полуострова, но также в Африке и в западной части полуострова Индостан, поэтому не исключено, что ареал природной очаговости MERS-CoV гораздо обширнее, чем принято считать. Было показано, что MERS-CoV способен репродуцироваться в первичных клеточных культурах, полученных от летучих мышей различных таксономических групп: короткохвостых листоносов (Phyllostomidae, Carollia), ночных крыланов (Pteropodidae, Rousettus) [32].
Исследователями из Саудовской Аравии была проведена серологическая разведка на территории Омана с целью обнаружения MERS-CoV в популяциях сельскохозяйственных животных, которая показала, что 100% одногорбых верблюдов (Camelus dromedarius) имеют антитела против субъединицы S1 спайкового белка MERSCoV. Затем были получены прямые доказательства циркуляции в организме верблюдов вариантов MERS-CoV, идентичных эпидемическим, и возможности заражения человека от этих животных [33]. Рукокрылые заражали верблюдов во время своих днёвок в загонах для сельскохозяйственных животных. Оказалось, что иммунная прослойка у MERS-CoV среди одногорбых верблюдов имеется в Африке, включая Канарские острова [32]. Вместе с тем специфические антитела к MERS-CoV отсутствовали у одногорбых верблюдов в Австралии [34], что свидетельствует о том, что эти животные не могут быть основным хозяином MERS-CoV. Специфические антитела-MERS были обнаружены у содержащихся в Катаре альпака (Vicugna pacos) [35]. Не исключено, что все мозоленогие (Artiodactyla: Tylopoda) имеют чувствительность к вирусу MERS-CoV и могут являться промежуточным хозяином и удобным индикатором для этого вируса при наличии природного резервуара — рукокрылых, содержащих вирус. Это предположение согласуется с отсутствием иммунной прослойки у двугорбых верблюдов (Camelus bactrianus) на неэндемичных для MERS-CoV территориях — в Казахстане [36], Монголии [37] и Cеверном Китае [38].
Несмотря на то, что поиск хозяев MERS-CoV среди других домашних животных (крупного рогатого скота, лошадей, коз, овец) не увенчался успехом в настоящее время, эти исследования существенно стимулировали изучение коронавирусов в популяциях млекопитающих помимо рукокрылых.
Имеются также свидетельства передачи MERS-CoV от человека к человеку, причём единственным известным источником инфекции является уже инфицированный человек. Однако передача MERS-CoV от человека к человеку, как правило, происходит только при тесном контакте с инфицированным, например, в медицинских учреждениях или при присоединении вторичной инфекции.
В настоящее время на территории Саудовской Аравии вирус MERS-CoV считается серьёзной угрозой здоровью населения, потому что миллионы верующих людей из 184 стран ежегодно совершают паломничество в данную территорию на Хадж или Умру, что может спровоцировать возникновение новой вспышки с более широким ареалом распространения данной инфекции. Последняя публикация о заболевании Ближневосточным респираторным синдромом была зарегистрирована в Катаре, Саудовская Аравия в феврале 2020 г. у пожилого мужчины с несколькими хроническими заболеваниями.
Коронавирусная инфекция SARS-CoV-2
В конце 2019 г. мир узнал о новом смертельном вирусе на территории КНР. Был обнаружен новый коронавирус, который стал причиной серии пневмонии в городе Ухань, провинции Хубэй, Китай. Быстрое распространение вируса положило начало эпидемии в Китае, за которой последовала всемирная пандемия. В феврале 2020 г. Всемирная организация здравоохранения (ВОЗ) присвоила инфекции название «COVID-19» (англ. COronaVIrus Disease 2019)1.
Международным комитетом по таксономии вирусов 11 февраля 2020 г. новому коронавирусу присвоено название SARS-CoV-2. Генетическая последовательность SARS-CoV-2 сходна с последовательностью SARS-CoV, по меньшей мере, на 79 %.
Анализ генетической основы S-белка Spike, проведённый специалистами из ведущих научных центров США, Австралии и Великобритании, показал, что благодаря произошедшим в нём мутациям рецептор-связывающего домена (RBD) шиповидных белков SARS-CoV-2 в отличие от других коронавирусов появилась способность эффективно «цепляться» за специфический рецептор АСЕ2. Было высказано следующее предположение: для осуществления такого захвата рецептор ACE2 тоже должен был претерпеть определенные генетические изменения. Это свидетельствует о том, что появление у SARS-CoV-2 способности заражать человека — результат естественного отбора [39][40][41].
Первые случаи заболевания, предположительно, были связаны с посещением рынка морепродуктов в Ухане, на котором продавали мясо домашней птицы, а также экзотических животных (летучих мышей, змей, панголинов). Однако специалисты тропического ботанического сада при Китайской академии наук пришли к выводу о том, что рынок в Ухане, который изначально считали первичным очагом распространения заболевания, не являлся таковым, так как первые заболевания новым коронавирусом были зарегистрированные еще в ноябре 2019 г. и не были взаимосвязаны [42]. Также установлена эпидемиологическая связь больных с поездками в КНР из сопредельных стран. Наибольшее количество заболевших выявлено в юго-восточной части Китая — 84% общего числа случаев в КНР [43].
SARS-CoV-2 представляет одноцепочечный РНКсодержащий вирус. По классификации патогенности он относится ко II группе. SARS-CoV-2 включён в перечень заболеваний, представляющих опасность для окружающих.
Генетический анализ вируса, вызвавшего заболевания выявил схожесть с коронавирусами, распространёнными среди подковоносых летучих мышей, однако пока достоверно неизвестно, являются ли они изначальным источником инфекции. Сейчас же основным способом распространения вируса является передача от человека к человеку.
Учёным быстро удалось установить, что вирус SARS-CoV-2 высоко контагиозен и что он может оставаться жизнеспособным в окружающей среде до 2 часов, а на поверхностях — от нескольких часов до 2 суток [44]. Инкубационный период после заражения — до 14 дней. Все возрастные группы восприимчивы к вирусу, при этом пожилые пациенты с сопутствующими заболеваниями подвержены более тяжелому течению болезни. Основным источником инфекции являются больные люди, бессимптомные носители и больные, находящиеся в инкубационном периоде. До сих пор основными путями передачи инфекции считаются воздушнокапельный и контактный. Вертикальный путь передачи между матерью и младенцем заподозрен после того, как заражение новым коронавирусом подтверждено у новорожденного спустя 30 часов после появления на свет в детской больнице Уханя. Также предполагается, что инфекция попадает в организм через конъюнктиву глаза, поскольку конъюнктивальный эпителий может быть инфицирован аэрозолем или другими биологическими жидкостями, содержащими вирус [45].
В начале эпидемического распространения свойства вируса имели стабильный характер с клональной идентичностью вируса SARS-CoV-2. Массовое проведение скрининг-исследований позволило выявить начальное эволюционное изменения вируса в разных частях света. Все вирусы естественным образом мутируют с течением времени, и SARS-CoV-2 не является исключением.
Данные секвенирования показали, что коронавирусы изменяются медленнее, чем большинство других РНК-вирусов, вероятно, это происходит благодаря ферменту, который исправляет потенциально фатальные ошибки копирования. Типичный вирус SARS-CoV-2 накапливает в своем геноме только две однобуквенные мутации в месяц-скорость изменения примерно вдвое меньше, чем у гриппа, и на четверть меньше, чем у ВИЧ. Данное исследование проходило в Базельском университете, Швейцария2.
Исследования Университетского колледжа Лондона показали, что два вируса SARS-CoV-2, собранные из разных точек мира, отличаются в среднем всего на 10 букв РНК из 29 903, это позволяет отслеживать эволюционные преобразования вируса. Многие выявленные мутации не имеют никакого значения для способности вируса распространяться или вызывать заболевание среди людей, однако некоторые генетические изменения способны давать штамму эволюционное преимущество и способствовать его распространению. Так, например, линия B.1.1.7 («Британский штамм») представляет собой филогенетический кластер, который быстро распространяется на юго-востоке Англии. До его обнаружения в начале сентября 2020 г. эта линия накопила 17 специфических мутаций, что свидетельствует о значительной предшествующей эволюции, возможно, в хронически инфицированном хозяине. По состоянию на 28 декабря 2020 г. на этот вариант приходилось примерно 28% случаев заражения SARS-CoV-2 в Англии, и популяционно-генетические модели позволяют предположить, что данная линия распространяется на 56% быстрее других. Линия B.1.1.7 распространилась, когда SARS-CoV-2 выявлялся уже повсеместно и, по-видимому, достигла доминирующего положения, превзойдя существующую популяцию циркулирующих вариантов. Это убедительно говорит о естественном отборе вируса с большей трансмиссивностью на популяционном уровне. В то время как меры общественного здравоохранения, такие как маски, соблюдение дистанции и ограничение больших скоплений людей, должны оставаться эффективными, но борьба с более трансмиссивным («более заразным») вариантом, вероятно, потребует более строгого применения и повсеместного принятия этих мер. Восемь мутаций линии B.1.1.7 затрагивают гликопротеин шиповидных отростков (S-белок). Предполагается, что эти мутации могут влиять на связывание АПФ2 и репликацию вируса. Другой штамм коронавируса, также с мутацией в рецептор-связывающем домене, быстро распространяется в Южной Африке. Влияние этих мутаций на антигенность в настоящее время неясно3.
В связи с тем, что SAR-CoV-2 уже распространился по всем континентам и количество заболевших людей продолжает расти, первоочередной задачей для здравоохранения всего мира является специфическая профилактика. По состоянию на декабрь 2020 г. различными медицинскими учреждениями и фармацевтическими компаниями велись разработки более 200 потенциальных вакцин.
В 2020 г. 11 августа в России была зарегистрирована вакцина «Гам-Ковид-Вак (Спутник V)», разработанная НИЦЭМ им. Н.Ф. Гамалеи.
Позднее, 13 октября 2020 г. Россия заявляет о регистрации еще одной вакцины — «ЭпиВакКорона», — разработанной Государственным научным центром вирусологии и биотехнологии «Вектор» Роспотребнадзора.
Ещё один перспективный вариант вакцины зарегистрирован 20 февраля 2021 г., разработанный Научным центром исследований и разработки иммунобиологических препаратов им. М.П. Чумакова (Москва).
По данным ВОЗ, в 2021 г. ведутся клинические исследования 63 вакцин-кандидатов во всем мире. Доказано, что для людей характерна высокая восприимчивость к коронавирусу: данному заболеванию подвержены все возрастные группы. Антигенная разнородность вирусов обусловливает высокую частоту повторного инфицирования.
Таким образом, появление новых представителей семейства коронавирусов подчеркивает актуальность дальнейшего всестороннего их изучения с целью выбора перспективных профилактических (противоэпидемических) мероприятий, совершенствования специфической профилактики и дальнейших разработок вакцин.
Современное поколение жителей планеты стало свидетелем беспрецедентной для нашего времени пандемии. Сегодня вся планета пытается выработать эффективные меры борьбы с COVID-19, вводит карантинные мероприятия и санкции за их нарушение. Всему человечеству ещё предстоит оценить и осмыслить масштабы нанесенного социально-экономического ущерба и последствия людских потерь. Каким будет наше общество после эпидемии COVID-19 — покажет время.
1. Kenneth McIntosh Coronavirus disease 2019 (COVID-19): Epidemiology, virology, and prevention
https://www.uptodate.com/contents/coronavirusdisease-2019-covid-19-epidemiology-virology-and-prevention
2. Электронный ресурс https://www.nature.com/articles/d41586-020-02544-6
3. Электронный ресурс https://jamanetwork.com/journals/jama/fullarticle/2775006
Список литературы
1. Щелканов М.Ю., Попова А.Ю. Дедков В.Г., Акимкин В.Г., Малеев В.В. История изучения и современная классификация Коронавирусов (Nidovirales: Coronaviridae) // Инфекция и иммунитет. - 2020. - Т.10, №2. - С. 221-246. DOI: 10.15789/2220-7619-HOI-1412
2. Li X., Luk H.K.H., Lau S.K.P., Woo P.C.Y. Human Coronaviruses: General Features. // Reference Module in Biomedical Sciences. – 2019. - B978-0-12-801238-3.95704-0. DOI: 10.1016/B978-0-12-801238-3.95704-0.
3. Львов Д.К., Колобухина Л.В., Дерябин П.Г. Коронавирусная инфекция. Тяжелый острый респираторный синдром // Инфекционные болезни: Новости. Мнения. Обучение. - 2015. - №4 (13). – С. 35-42. eLIBRARY ID: 25197472
4. Львов Д. К., Альховский С.В., Колобухина Л.В., Бурцева Е.И. Этиология эпидемической вспышки COVID-19 в г. Ухань (провинция Хубэй, Китайская Народная Республика), ассоциированной с вирусом 2019-ncov (Nidovirales, Coronaviridae, Coronavirinae, Betacoronavirus, Подрод Sarbecovirus): уроки эпидемии SARS-COV // Вопросы вирусологии. - 2020.- №1. – С. 6-15. DOI: 10.36233/0507-4088-2020-65-1-6-15
5. Шамшева О.В. Новый коронавирус COVID-19 (SARSCOV-2) // Детские инфекции. - 2020. – Т.19, №1. - С. 5-6. eLIBRARY ID: 42706398
6. Tyrrell D.A., Bynoe M.L. Cultivation of a novel type of common-cold virus in organ cultures. // Br Med J. – 1965. – V.1. – P.1467-1470. DOI: 10.1136/bmj.1.5448.1467
7. Almeida J.D., Berry D.M., Cunningham C.H., Hamre D., Hofstad M.S., et al. Virology: Coronaviruses. // Nature. – 1968. – V.220. – P. 650. DOI: 10.1038/220650b0
8. Bradburne AF, Somerset BA. Coronative antibody tires in sera of healthy adults and experimentally infected volunteers. // J Hyg (Lond). – 1972. – V.70(2). – P.235-44. DOI: 10.1017/s0022172400022294
9. Hamre D, Procknow JJ. A new virus isolated from the human respiratory tract. // Proc Soc Exp Biol Med. – 1966. –V.121(1). – P. 190-3. DOI: 10.3181/00379727-121-30734.
10. Akerlund A, Greiff L, Andersson M, Bende M, Alkner U, Persson CG. Mucosal exudation of fibrinogen in coronavirus-induced common colds. // Acta Otolaryngol. – 1993. – V.113(5). – P. 642-8. DOI: 10.3109/00016489309135878
11. Linden M, Greiff L, Andersson M, Svensson C, Akerlund A, et al. Nasal cytokines in common cold and allergic rhinitis. // Clin Exp Allergy. – 1995. – V.25(2). – P.166-72. DOI: 10.1111/j.1365-2222.1995.tb01022.x
12. Щелканов М.Ю., Колобухина Л.В., Львов Д.К. Коронавирусы человека (Nidovirales, Coronaviridae): возросший уровень эпидемической опасности // Лечащий врач. - 2013. - № 10. - С.49-54. eLIBRARY ID: 22592720
13. Чучалин А.Г. Тяжелый острый респираторный синдром (ТОРС) // Русский медицинский журнал. - 2003. - Т.11. 22(194). - С. 1197-1204.
14. Медицинская вирусология: учебное пособие. Под ред. И.И. Генералова. - Витебск, ВГМУ, 2017.
15. Woo P.C., Lau S.K., Lam C.S., Lau C.C., Tsang A.K., et al. Discovery of seven novel Mammalian and avian coronaviruses in the genus deltacoronavirus supports bat coronaviruses as the gene source of alphacoronavirus and betacoronavirus and avian coronaviruses as the gene source of gammacoronavirus and deltacoronavirus. // J Virol. – 2012. – V.86(7). – P.3995-4008. DOI: 10.1128/JVI.06540-11
16. Balboni A., Battilani M., Prosperi S. The SARS-like coronaviruses: the role of bats and evolutionary relationships with SARS coronavirus. // New Microbiol. – 2012. – V.35(1). – P. 1-16. PMID: 22378548.
17. Андрейчик М.А., Копча В.С., Нычик Н.А. Тяжелый острый респираторный синдром // Международный медицинский журнал. - 2003. - №3, - С. 98-102.
18. Fouchier R.A., Hartwig N.G., Bestebroer T.M., Niemeyer B., de Jong J.C., et al. A previously undescribed coronavirus associated with respiratory disease in humans. Proc Natl Acad Sci U S A. 2004;101(16):6212-6. DOI: 10.1073/pnas.0400762101.
19. Lednicky J.A., Waltzek T.B., McGeehan E., Loeb J.C., Hamilton S.B., Luetke M.C. Isolation and genetic characterization of human coronavirus NL63 in primary human renal proximaltubular epithelial cells obtained from a commercial supplier, and confirmation of its replication in two different types of human primary kidney cells. // Virol J. – 2013. – V. 10. – P.213. DOI: 10.1186/1743-422X-10-213
20. Van der Hoek L., Pyrc K., Jebbink M.F., Vermeulen-Oost W., Berkhout R.J., et al. Identification of a new human coronavirus. // Nat Med. – 2004. – V. 10(4). – P. 368-73. DOI: 10.1038/nm1024
21. Woo P.C., Lau S.K., Chu C.M., Chan K.H., Tsoi H.W., et al. Characterization and complete genome sequence of a novel coronavirus, coronavirus HKU1, from patients with pneumonia. // J Virol. – 2005. – V. 79(2). – P. 884-95. DOI: 10.1128/JVI.79.2.884-895.2005
22. Lau S.K., Woo P.C., Yip C.C., Tse H., Tsoi H.W., et al. Coronavirus HKU1 and other coronavirus infections in Hong Kong. // J Clin Microbiol. – 2006. – V.44(6). – P.2063-71. DOI: 10.1128/JCM.02614-05
23. Sloots T.P., McErlean P., Speicher D.J., Arden K.E., Nissen M.D., Mackay I.M. Evidence of human coronavirus HKU1 and human bocavirus in Australian children. // J Clin Virol. – 2006. – V.35(1). – P.99-102. DOI: 10.1016/j.jcv.2005.09.008
24. Arden K.E., Nissen M.D., Sloots T.P., Mackay I.M. New human coronavirus, HCoV-NL63, associated with severe lower respiratory tract disease in Australia. // J Med Virol. – 2005. – V.75(3). – P.455-62. DOI: 10.1002/jmv.20288
25. Chiu S.S., Chan K.H., Chu K.W., Kwan S.W., Guan Y., et al. Human coronavirus NL63 infection and other coronavirus infections in children hospitalized with acute respiratory disease in Hong Kong, China. // Clin Infect Dis. – 2005. – V.40(12). – P.1721-9. DOI: 10.1086/430301
26. Vabret A., Dina J., Gouarin S., Petitjean J., Corbet S., Freymuth F. Detection of the new human coronavirus HKU1: a report of 6 cases. // Clin Infect Dis. – 2006. – V. 42(5). – P.634-9. DOI: 10.1086/500136
27. Bastien N., Anderson K., Hart L., Van Caeseele P., Brandt K., et al. Human coronavirus NL63 infection in Canada. // J Infect Dis. – 2005. – V.191(4). – P.503-6. DOI: 10.1086/426869
28. Щелканов М.Ю., Ананьев В.Ю., Кузнецов В.В., Шуматов В.Б. Ближневосточный респираторный синдром: когда вспыхнет тлеющий очаг? // Тихоокеанский медицинский журнал. - 2015. - № 2. -С. 94–98. eLIBRARY ID: 24275106
29. Müller M.A., Raj V.S., Muth D., Meyer B., Kallies S., et al. Human coronavirus EMC does not require the SARS-coronavirus receptor and maintains broad replicative capability in mammalian cell lines. // mBio. – 2012. – V.3(6). – P. e00515-12. DOI: 10.1128/mBio.00515-12
30. De Benedictis P., Marciano S., Scaravelli D., Priori P., Zecchin B., et al. Alpha and lineage C betaCoV infections in Italian bats. // Virus Genes. – 2014. – V.48(2). – P.366-71. DOI: 10.1007/s11262-013-1008-x
31. Gortazar C., Segalés J. Middle East respiratory syndrome (MERS) coronavirus: a new challenge for veterinarians? // Vet Pathol. – 2013. – V.50(6). – P.954-5. DOI: 10.1177/0300985813506391
32. Azhar E.I., El-Kafrawy S.A., Farraj S.A., Hassan A.M., AlSaeed M.S., et al. Evidence for camel-to-human transmission of MERS coronavirus. // N Engl J Med. – 2014. – V.370(26). – P.2499-505. DOI: 10.1056/NEJMoa1401505
33. Corman V.M., Jores J., Meyer B., Younan M., Liljander A., et al. Antibodies against MERS coronavirus in dromedary camels, Kenya, 1992-2013. // Emerg Infect Dis. – 2014. – V.20(8). – P.1319-22. DOI: 10.3201/eid2008.140596
34. Crameri G., Durr P.A., Barr J., Yu M., Graham K., et al. Absence of MERS-CoV antibodies in feral camels in Australia: Implications for the pathogen’s origin and spread. // One Health. – 2015. – V.1. – P. 76-82. DOI: 10.1016/j.onehlt.2015.10.003
35. Reusken C.B., Schilp C., Raj V.S., De Bruin E., Kohl R.H., et al. MERS-CoV Infection of Alpaca in a Region Where MERSCoV is Endemic. // Emerg Infect Dis. – 2016. – V.22(6). – P. 1129-31. DOI: 10.3201/eid2206.152113
36. Miguel E., Perera R.A., Baubekova A., Chevalier V., Faye B., et al. Absence of Middle East Respiratory Syndrome Coronavirus in Camelids, Kazakhstan, 2015. // Emerg Infect Dis. – 2016. – V.22(3). – P.555-7. DOI: 10.3201/eid2203.151284
37. Chan S.M., Damdinjav B., Perera R.A., Chu D.K., Khishgee B., et al. Absence of MERS-Coronavirus in Bactrian Camels, Southern Mongolia, November 2014. // Emerg Infect Dis. – 2015. – V. 21(7). – P.1269-71. DOI: 10.3201/eid2107.150178
38. Liu R., Wen Z., Wang J., Ge J., Chen H., Bu Z. Absence of Middle East respiratory syndrome coronavirus in Bactrian camels in the West Inner Mongolia Autonomous Region of China: surveillance study results from July 2015. // Emerg Microbes Infect. – 2015. – V.4(12). – P.e73. DOI: 10.1038/emi.2015.73
39. Белоцерковская Ю.Г., Романовских А.Г., Смирнов И.П. COVID-19: респираторная инфекция, вызванная новым коронавирусом: новые данные об эпидемиологии, клиническом течении, ведении пациентов. // Consilium Medicum. – 2020. – Т. 22, №3. – С. 12–20. DOI: 10.26442/20751753.2020.3.200092
40. Xu X., Chen P., Wang J., Feng J., Zhou H., et al. Evolution of the novel coronavirus from the ongoing Wuhan outbreak and modeling of its spike protein for risk of human transmission. // Sci China Life Sci. – 2020. – V.63(3). – P.457-460. DOI: 10.1007/s11427-020-1637-5
41. Jaimes J.A., Millet J.K., Stout A.E., André N.M., Whittaker G.R. A Tale of Two Viruses: The Distinct Spike Glycoproteins of Feline Coronaviruses. // Viruses. – 2020. – V.12(1). – P. 83. DOI: 10.3390/v12010083
42. Wang W., Tang J., Wei F. Updated understanding of the outbreak of 2019 novel coronavirus (2019-nCoV) in Wuhan, China. // J Med Virol. – 2020. – V.92(4). – P.441-447. DOI: 10.1002/jmv.25689
43. Малинникова Е.Ю. Новая коронавирусная инфекция. Сегодняшний взгляд на пандемию XXI века // Инфекционные болезни: Новости. Мнения. Обучение. - 2020. -№2 (33). – С. 18-32. DOI: 10.33029/2305-3496-2020-9-2-18-32
44. van Doremalen N., Bushmaker T., Morris D.H., Holbrook M.G., Gamble A., et al. Aerosol and Surface Stability of SARS-CoV-2 as Compared with SARS-CoV-1. // N Engl J Med. – 2020. – V.382(16). – P.1564-1567. DOI: 10.1056/NEJMc2004973
45. Lu C.W., Liu X.F., Jia Z.F. 2019-nCoV transmission through the ocular surface must not be ignored. // Lancet. – 2020. – V.395(10224). – P. e39. DOI: 10.1016/S0140-6736(20)30313-5
Об авторах
А. А. КононенкоРоссия
Кононенко Анна Александровна, младший научный сотрудник лаборатории санитарной охраны территории
Ростов-на-Дону
А. К. Носков
Россия
Носков Алексей Кимович, к.м.н. директор
Ростов-на-Дону
С. Ю. Водяницкая
Россия
Водяницкая Светлана Юрьевна, к.м.н., главный специалист (инфекционист) отдела лечебной помощи взрослому населению управления лечебно-профилактической помощи Минздрава РО
Ростов-на-Дону
О. А. Подойницина
Россия
Подойницына Оксана Андреевна, к.б.н., научный сотрудник лаборатории микробиологии холеры
Ростов-на-Дону
Рецензия
Для цитирования:
Кононенко А.А., Носков А.К., Водяницкая С.Ю., Подойницина О.А. Коронавирусы человека, способные вызывать чрезвычайные ситуации. Медицинский вестник Юга России. 2021;12(1):14-23. https://doi.org/10.21886/2219-8075-2021-12-1-14-23
For citation:
Kononenko A.A., Noskov A.K., Vodyanitskaya S.Yu., Podoynitsyna O.A. Human coronaviruses that can cause emergencies. Medical Herald of the South of Russia. 2021;12(1):14-23. https://doi.org/10.21886/2219-8075-2021-12-1-14-23







































