Перейти к:
Хирургические аспекты лечения грыж пищеводного отверстия диафрагмы
https://doi.org/10.21886/2219-8075-2024-15-4-104-112
Аннотация
Цель: улучшение результатов лечения пациентов с осложнёнными грыжами пищеводного отверстия диафрагмы (ГПОД) на основе разработанного индивидуального комплексного подхода.
Материалы и методы: проведён анализ 204 наблюдений больных с осложнёнными формами ГПОД в возрасте от 17 до 77 лет (44% мужчин, 56,4%женщин). Все 204 пациента страдали гастроэзофагеальной рефлюксной болезнью (ГЭРБ). У 53 (26%) пациентов с осложнёнными формами ГПОД при хирургическом лечении использованы синтетические имплантаты. У 38 пациентов (18,6%) с ГПОД и метаплазией слизистой оболочки пищевода (СОП), лечебная тактика включала в себя антирефлюксную операцию и проведение аргон-плазменной коагуляции (АПК).
Результаты: ранние послеоперационные осложнения чаще встречались в группе пациентов, у которых были использованы сетчатые имплантаты. Поздние специфические послеоперационные осложнения в группе пациентов, которым по показаниям были применены синтетические имплантаты, встречались достоверно реже. При оценке качества жизни по данным опросников GERD-HRqL, GSRS субъективные симптомы ГЭРБ резко уменьшаются после операции (через 3 месяца), продолжают снижаться и до 12 месяцев, после чего приобретают постоянный характер. При ГПОД, осложнённых метаплазией СОП, после окончания курсов АПК во всех случаях отмечена полная регрессия измененного эпителия.
Выводы: хирургическое лечение осложнённых форм грыж пищеводного отверстия диафрагмы с использованием видеоэндоскопических технологий на основе разработанного алгоритма является высокоэффективным, что подтверждается низким числом послеоперационных осложнений и значительным улучшением качества жизни пациентов.
Ключевые слова
Для цитирования:
Черкасов Д.М., Черкасов М.Ф., Татьянченко В.К., Старцев Ю.М., Меликова С.Г., Галашокян К.М., Скуратов А.В., Ендоренко К.В. Хирургические аспекты лечения грыж пищеводного отверстия диафрагмы. Медицинский вестник Юга России. 2024;15(4):104-112. https://doi.org/10.21886/2219-8075-2024-15-4-104-112
For citation:
Cherkasov D.M., Cherkasov M.F., Tat’yanchenko V.K., Starcev Y.M., Melikova S.G., Galashokyan K.M., Skuratov A.V., Endorenko K.V. Surgical aspects of treatment of hiatal hernia. Medical Herald of the South of Russia. 2024;15(4):104-112. (In Russ.) https://doi.org/10.21886/2219-8075-2024-15-4-104-112
Введение
Грыжа пищеводного отверстия диафрагмы (ГПОД) — одно из самых часто встречающихся в мире заболеваний, почти всегда осложняющееся гастроэзофагеальным рефлюксом [1]. К менее частым, но более серьёзным осложнениям относятся метаплазия пищевода, эрозии, язвы, стенозы, ущемления, кровотечения. По данным многих исследований, метапластические изменения слизистой оболочки пищевода (СОП) увеличивают риск развития злокачественных опухолей [2].
Хирургическое вмешательство уже давно интегрировано в комплексное лечение пациентов с осложнёнными ГПОД, но большинству хирургов всё ещеё необходимо улучшить понимание механизмов развития грыжи и анатомических особенностей организма [1][3].
До сих пор нет однозначного ответа на вопрос о том, как следует выполнять пластику дефекта диафрагмы при грыже пищеводного отверстия. Также не существует общего мнения о том, следует или нет использовать синтетические имплантаты, и если да, то какие и в каких случаях [3–5].
При диагностировании у пациентов такого осложнения ГПОД, как метаплазия слизистой пищевода, используется комплексный подход, который включает в себя не только антирефлюксную операцию, но и пред- и послеоперационную консервативную терапию, а также эндоскопическое воздействие разными способами на патологически изменённую слизистую оболочку пищевода [6].
Цель исследования — улучшение результатов лечения пациентов с осложнёнными грыжами пищеводного отверстия диафрагмы на основе разработанного индивидуального комплексного подхода и анатомических исследований.
Материалы и методы
Анатомическое исследование. Возрастные и конституциональные особенности биомеханических свойств фасциальных структур, а также кровоснабжение диафрагмы изучены на 40 препаратах от трупов людей в возрасте от 19 до 75 лет, умерших от причин, не связанных с заболеваниями органов пищеварения и сердечно-сосудистой системы.
Нами было выявлено, что, начиная со II зрелого возрастного периода, эластичная ткань фасциальных структур диафрагмальной ножки дегенерирует, что сопровождается рубцовыми изменениями коллагеновых пучков в этих анатомических образованиях. В пожилом возрасте фасциальные структуры диафрагмальных ножек теряют свою прочность и эластичность.
Начиная со II зрелого возраста, особенно у брахиморфных людей, количество жировых волокон, окружающих ПОД, значительно уменьшается. Это один из предрасполагающих факторов для развития диафрагмальной грыжи. В процессе анатомических исследований со II зрелого возрастного периода также было отмечено выраженное снижение кровообращения мышечных тканей в области ПОД. Анализ диаметра сосудов, кровоснабжающих данные мышечные ткани, показал значительное уменьшение диаметра основных сосудов и их ветвей, кроме того, уменьшается численность ветвей III–IV порядков, у них появляется извитость, что приводит к снижению васкуляризации в тканях диафрагмы. Исследование ёмкости артериального русла показало его снижение в 1,5–2 раза в пожилом возрастном периоде.
Клиническое исследование. В клинике РостГМУ был проведён анализ комплексной терапии 204 пациентов с различными формами осложнений грыжи пищеводного отверстия диафрагмы. Стоит отметить, что большинство пациентов (52,4%) состояло в средней возрастной группе, общий возраст колебался от 17 до 77 лет. На основании наших анатомических исследований все 204 пациента были разделены по типу телосложения.
Согласно классификации Б.В. Петровского и Н.Н. Каншина (1962), грыжи пищеводного отверстия делятся на аксиальные и параэзофагеальные. В нашем исследовании мы чаще сталкивались с пациентами с аксиальными грыжами (156 пациентов (76,5%)). С целью оценки дефекта пищеводного отверстия диафрагмы (ПОД) при лечении данной категории больных мы использовали формулу Granderath, которая позволяет вычислить площадь дефекта ПОД, что являлось одним из важнейших данных, позволяющих в дооперационном периоде определиться с выбором пластики диафрагмальных ножек.
100% пациентов в нашем исследовании страдало гастроэзофагеальной рефлюксной болезнью, кроме того, в процессе обследования нам удалось выявить и другие осложнения, связанные с наличием у больных грыжи пищеводного отверстия диафрагмы.
Распределение пациентов по типу телосложения и площади ПОД, а также перечень осложнений ГПОД представлены в таблице 1.
Таблица / Table 1
Основные характеристики пациентов
Basic patient characteristics
|
Характеристики пациентов Patient characteristics |
Количество пациентов (абс, %) Number of patients (abs., %) |
|
I. По типу телосложения / By body type: |
|
|
Брахиморфный тип / Brachymorphic type |
62 (30,4) |
|
Мезоморфный тип / Mesomorphic type |
108 (52,9) |
|
Долихоморфный тип / Dolichomorphic type |
34 (16,7) |
|
II. По площади дефекта пищеводного отверстия диафрагмы / By the area of the defect of the esophageal opening of the diaphragm: |
|
|
1. Аксиальные грыжи / Axial hernias |
|
|
Малая / Small |
54 (26,5) |
|
Большая / Large |
88 (43,1) |
|
Гигантская / Giant |
14 (6,9) |
|
2. Параэзофагеальные грыжи / Paraesophageal hernias |
|
|
Большая / Large |
32 (15,7) |
|
Гигантская / Giant |
16 (7,8) |
|
III. По осложнениям ГПОД / By complications of hiatal hernias: |
|
|
ГЭРБ / GERD |
204 (100) |
|
Эрозивно-язвенные изменения СОП / Erosive and ulcerative changes in the mucous membrane of the esophagus |
29 (14,2) |
|
Метаплазия желудочного типа / Gastric type metaplasia |
11 (5,4) |
|
Метаплазия кишечного типа / Intestinal type metaplasia |
27 (13,2) |
|
Пептическая стриктура пищевода / Peptic stricture of the esophagus |
7 (3,4) |
|
Ущемленная параэзофагеальная грыжа / Strangulated paraesophageal hernia |
1 (0,5) |
Все пациенты с осложнёнными формами ГПОД получили комплексное лечение, включающее в себя хирургическое вмешательство, выполняемое строго по показаниям и включающее в себя пластику дефекта пищеводного отверстия диафрагмы и наложение антирефлюксной манжеты. Распределение пациентов, согласно показаниям к выполнению оперативного вмешательства, выглядит следующеим образом:
- неэффективные курсы медикаментозной терапии (84 человека);
- метаплазия СОП (38 человек, среди них кишечного типа — 27, желудочного типа — 11);
- параэзофагеальная грыжа (45 человек);
- эрозивно-язвенные изменения СОП (29 человек);
- пептическая стриктура пищевода (7 человек);
- ущемлённая параэзофагеальная грыжа (1 человек).
Сопутствующая хирургическая патология была выявлена у 31 пациента, данной категории больных были выполнены симультанные оперативные вмешательства. В нашей хирургической практике, как и в проведённом нами исследовании, мы используем сетчатые имплантаты достаточно избирательно, согласно разработанному нами алгоритму, учитывая не только размер дефекта пищеводного отверстия диафрагмы, но и возраст пациента и тип телосложения. В связи с этим из 204 пациентов 53 пациентам сетчатые имплантаты были установлены нами на этапе пластики пищеводного отверстия диафрагмы, что составило 26% от общего количества больных, подвергшихся комплексному лечению. Так, у 29 пациентов причиной установки сетчатого имплантата явились гигантские параэзофагеальные (13 пациентов) и аксиальные (16 пациентов) грыжи пищеводного отверстия диафрагмы. Согласно разработанному алгоритму пластики ПОД, нами были установлены сетчатые имплантаты 24 пациентам с большими грыжами (согласно формуле Granderath) II и пожилого возрастных периодов, имеющих брахиморфный тип телосложения.
При выполнении пластики ножек диафрагмы путём крурорафии мы используем разработанный нами алгоритм, в котором оцениваем размеры грыжевого дефекта, типы телосложения и возраст пациентов. На этом основании при малых размерах дефекта ПОД вне зависимости от телосложения пластика дефекта диафрагмы выполняется исключительно местными тканями. При гигантских размерах грыжевого дефекта крурорафию мы укрепляем имплантатом, у больных с большими грыжами ПОД пластика диафрагмальных ножек выполняется в зависимости от типа телосложения. Так, при долихоморфном типе телосложения диафрагмокрурорафия выполняется нитью «V-loc», а с целью укрепления накладываются одиночные швы, для этого мы используем нить «VICRYL». У пациентов с брахиморфным телосложением диафрагмокрурорафию укрепляем сетчатым имплантатом, расположенным в заднем средостении. Что касается пациентов с мезоморфным типом телосложения, то в данной группе больных в зависимости от морфофункционального состояния диафрагмальных ножек применимы обе вышеописанные методики.
Способ аллопластики заключается в следующем: под визуальным контролем прямоугольный сетчатый имплантат устанавливался в заднее средостение над диафрагмой таким образом, чтобы длинная сторона имплантата находилась на расстоянии не менее 2 см от задней стенки пищевода, а поверхность имплантата перекрывала пищеводное отверстие диафрагмы и диафрагмальные ножки. Эндопротез по углам фиксировали к диафрагме, после чего следовало полное укрытие имплантата путём ушивания ножек диафрагмы так, чтобы крайний шов на ножках накладывался выше имплантата (Патент на изобретение РФ №2611912/01.03.2017 «Способ хирургического лечения грыж пищеводного отверстия диафрагмы»).
Во время обследования у 38 пациентов с грыжами пищеводного отверстия диафрагмы было выявлено такое осложнение основного заболевания, как метаплазия СОП, вызванная выраженным гастроэзофагеальным рефлюксом. У этой группы пациентов помимо метаплазии, также были выявлены тяжёлые формы эзофагита, согласно Лос-Анджелесской классификации, что потребовало проведения медикаментозной терапии на до- и послеоперационных этапах комплексного лечения. При обследовании на дооперационном этапе в данной группе пациентов обязательным исследованием являлась биопсия слизистой оболочки пищевода, с последующим морфологическим исследованием. Так была выявлена дисплазия низкой степени у 9 пациентов в группе больных с метаплазией слизистой оболочки пищевода, что составило 23,7%. У всех 38 пациентов после проведения морфологического исследования биоптата СОП дисплазии высокой степени отмечено не было. Всем пациентам с метаплазией слизистой оболочки пищевода, кроме консервативной терапии в послеоперационном периоде, через 30–45 дней проводились сеансы аргон-плазменной коагуляции.
Разработанный способ аргон-плазменной коагуляции (Патент на изобретение РФ № 2625592/17.07.2017 «Способ эндохирургического лечения пищевода Барретта») основывается на выявлении и измерении максимальной длины циркулярного сегмента метаплазии (МДЦСМ), что позволяет применять данный метод, не опасаясь возникновения характерных для данной манипуляции осложнений.
Схема выполнения аргон-плазменной коагуляции:
- при МДЦСМ ≤ 1,5 см сначала выполняли АПК двух соседних стенок пищевода, через 30 дней — двух оставшихся стенок;
- при выполнении условия 1,5 см < МДЦСМ ≤ 3,0 см сначала выполняли АПК двух стенок пищевода расположенных через одну, через 30 дней — двух оставшихся стенок;
- при МДЦСМ ˃ 3 см сначала выполняли АПК одной стенки пищевода, через 30 дней выполняли АПК противоположной стенки пищевода, еще через 30 дней — третьей стенки пищевода, ещё через 30 дней — АПК оставшейся стенки пищевода.
Количество сеансов АПК напрямую зависит от размеров площади поражения метаплазией СОП. Для того, чтобы снизить риски возможного формирования стриктуры пищевода, нужно, чтобы площадь поверхности, подвергающейся АПК была не более 4 см².
Сбор данных проводили при помощи электронных таблиц Microsoft Excel 2013 (Microsoft, США). Обработку и анализ данных проводили при помощи программ SPSS Statistic (IBM Statistics, США) и Stattech v. 3.1.8 (разработчик — ООО «Статтех», Россия).
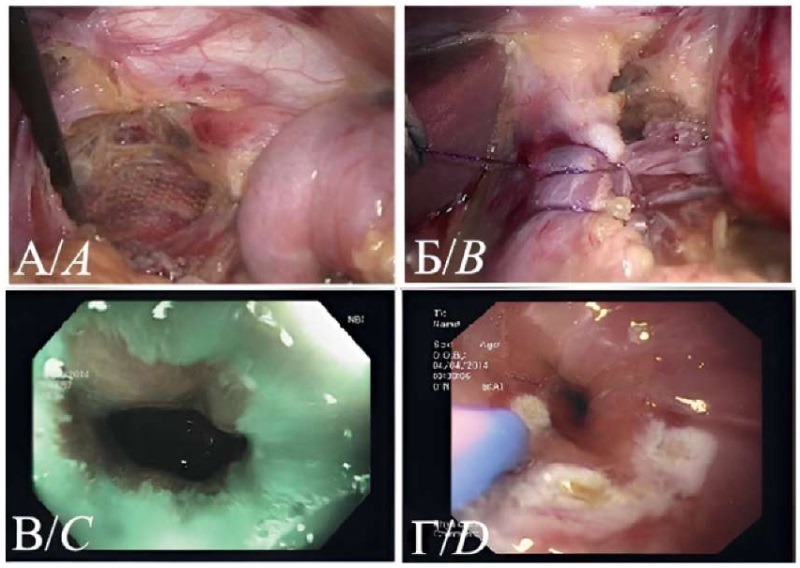
Рисунок 1. Этапы комплексного лечения пациента с грыжей пищеводного отверстия диафрагмы осложненной метаплазией кишечного типа. А — интраоперационное фото, установка синтетического имплантата в заднее средостение. Б — интраоперационное фото, ушивание диафрагмальных ножек. В — эндоскопическое исследование в режиме NBI. Участки измененной слизистой оболочки пищевода. Г — эндоскопическое исследование. Выполнение аргон-плазменной коагуляции.
Figure 1. Stages of complex treatment of a patient with a hiatal hernia complicated by Barrett's esophagus. A — intraoperative photo, installation of a mesh implant in the posterior mediastinum. B — intraoperative photo, suturing of the diaphragmatic crura. C — endoscopic examination in NBI mode. Areas of metaplasia of the esophageal mucosa. D — endoscopic examination. Performing argon plasma coagulation.
Результаты
В клинике РостГМУ проведён тщательный анализ осуществлённого комплексного лечения пациентов с осложнениями ГПОД. В нашем исследовании у 53 пациентов от общего числа больных была выполнена пластика ПОД с использованием синтетического имплантата, установленного в заднем средостении и укрытого диафрагмальными ножками во избежание механического контакта имплантата с полыми органами брюшной полости.
После изучения данных результатов лечения больных, которым пластика пищеводного отверстия выполнялась местными тканями, у 32 пациентов (21,2%) были выявлены послеоперационные осложнения, у части которых были диагностированы более одного осложнения, что подробно представлено в таблице 2.
Таблица / Table 2
Ранние послеоперационные осложнения у пациентов при пластике ПОД местными тканями
Early postoperative complications after plastic using local tissues
|
Осложнения / Complications |
Мужчин / Males (n = 68) |
Женщин / Females (n = 83) |
Всего / Total (n = 151) |
|
Синдром gas-bloat / Gas-bloat syndrome |
8 |
11 |
19 |
|
Дисфагия / Dysphagia |
4 |
4 |
8 |
|
Икота / Hiccups |
1 |
1 |
2 |
|
Диспептические расстройства / Dyspeptic disorders |
5 |
9 |
14 |
|
Всего / Total |
18 |
25 |
43 |
Нам удалось проследить почти за всеми больными данной группы (147 пациентов из 151). При анализе послеоперационных осложнений установлено, что большинство осложнений купировалось уже через месяц после оперативного лечения. Всего лишь у трёх пациентов оставались диспепсические расстройства, у одного — явления дисфагии.
Что касается пациентов, которым выполнялась пластика ПОД с использованием сетчатого имплантата, то в данной категории проанализированы все 53 пациента. Выявлены 17 пациентов, у которых отмечены ранние послеоперационные осложнения. Характер данных осложнений представлен в таблице 3.
Таблица / Table 3
Ранние послеоперационные осложнения у пациентов при пластике ПОД с сетчатым имплантатом
Early postoperative complications after plastic using a mesh implant
|
Осложнения / Complications |
Мужчин / Males (n = 22) |
Женщин / Females (n = 31) |
Всего / Total (n = 53) |
|
Синдром gas-bloat / Gas-bloat syndrome |
3 |
5 |
8 |
|
Дисфагия / Dysphagia |
1 |
2 |
3 |
|
Икота / Hiccups |
– |
1 |
1 |
|
Диспептические расстройства / Dyspeptic disorders |
2 |
3 |
5 |
|
Всего / Total |
6 |
11 |
17 |
Через месяц после выполненного оперативного вмешательства было зафиксировано незначительное количество жалоб: двое жаловались на диспептические расстройства, двое — на отрыжку, один больной — на проявления дисфагии.
Согласно классификации Clavien-Dindo, все выявленные ранние послеоперационные осложнения соответствовали I степени. Необходимо указать, что данные осложнения чаще отмечались у пациентов, у которых интраоперационно применялись синтетические имплантаты, однако все эти осложнения носили временный эффект, и их удалось купировать медикаментозными средствами, не прибегая к выполнению повторных хирургических вмешательств.
В сроке до 5 лет нам удалось провести анализ результатов у 142 пациентов из 151, у которых не использовались сетчатые имплантаты, что составило 94%, и у всех 53 пациентов с установленным сетчатым имплантатом.
У пациентов с пластикой ножек диафрагмы местными тканями выявлены следующие поздние осложнения: миграция фундопликационной манжетки (n-3), феномен телескопа (n-2), гиперфункция манжетки (n-2) и гастроэзофагеальный рефлюкс (n-8).
Диагностируемые нами миграция и соскальзование желудочной манжеты не проявлялись какими-либо клиническими симптомами либо жалобами пациентов, в связи с чем в дополнительном лечении не было необходимости. Другие выявленные осложнения не потребовали проведения повторных хирургических манипуляций и были купированы с помощью применения медикаментозной терапии.
Среди 53 отслеженных нами в течение 5 лет пациентов, у которых использовался сетчатый имплантат в качестве укрепляющего материала, такое осложнение как гастроэзофагеальный рефлюкс был диагностирован только у 2 (3,8%) пациентов. Этим больным была назначена консервативная терапия, которая дала положительный эффект. Проведённые исследования и их анализ наглядно продемонстрировали, что осложнения в позднем послеоперационном периоде у пациентов, которым при выполнении пластики пищеводного отверстия диафрагмы использовался сетчатый материал, выявлялись значительно реже, нежели у группы больных с пластикой местными тканями.
Качество жизни пациентов оценивалось с использованием общепринятых опросников (рис. 2).
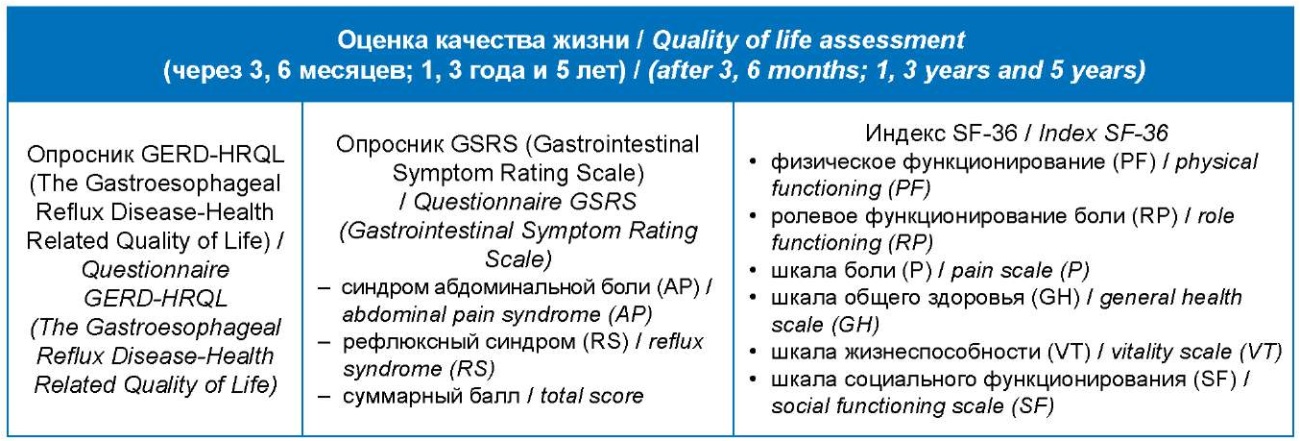
Рисунок 2. Применяемые для оценки качества жизни опросники
Figure 2. Questionnaires used to assess quality of life
Благодаря опросникам нам удалось установить, что по истечении 3-х месяцев после проведённого хирургического лечения проявления рефлюкса снижаются достаточно явно, тенденция к снижению данных проявлений продолжается до года и затем приобретает непрерывный характер.
Проведённый анализ данных опросника GERD-HRQL у больных с укреплением крурорафии синтетическим материалом выявил высокие показатели у этой группы пациентов до оперативного вмешательства и через 3 месяца после его выполнения по сравнению с группой пациентов, пластика которым выполнялась без использования сетчатого материала (рис. 3). Более выраженные жалобы связаны с тем, что изначально пациенты, которым пластика пищеводного отверстия диафрагмы дополнялась укреплением синтетическим имплантатом, имели большие размеры грыжевых ворот и отмечали более выраженные клинические проявления своего заболевания.
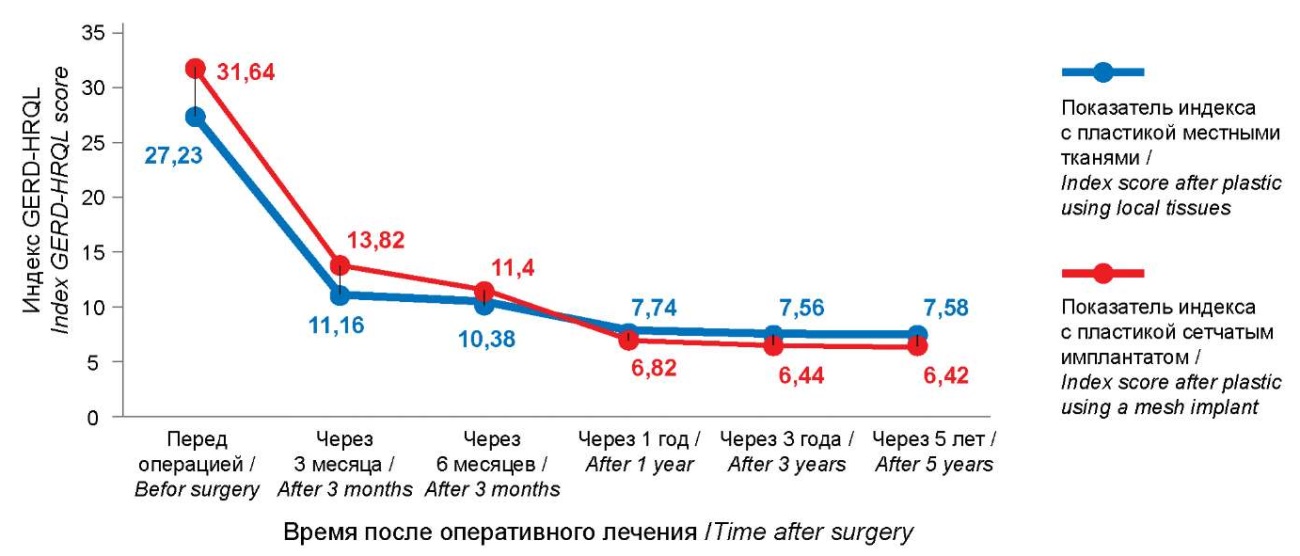
Рисунок 3. Показатели индекса GERD-HRQL
Figure 3. GERD-HRQL index scores
Во время анализа данных опросника GSRS в обеих группах наблюдения показатель таких шкал, как «абдоминальная боль», «рефлюксный синдром» и шкала суммарного измерения, имеют значительную тенденцию к снижению к 3-му месяцу после оперативного вмешательства. К 6-му месяцу мы также наблюдали снижение данных показателей, а с 12-го месяца значения могут быть сравнимы с соответствующими данными здоровых людей. При анализе шкалы «Рефлюксный синдром» было выявлено наибольшее снижение показателей уже к третьему месяцу. Стоит отметить, что у больных, которым пластика грыжевых ворот дополнялась сетчатым имплантатом, было отмечено более медленное снижения показателей. При изучении шкалы «Диспептический синдром» была отмечена нормализация данных показателей уже к 3-му месяцу, у пациентов с пластикой только местными тканями изученные нами данные не отличались от предоперационных. Показатели данной шкалы несколько повышены у пациентов, которым применяли пластику с использованием синтетических материалов, это связано с диспептическими расстройствами в раннем периоде после оперативного вмешательства, однако было отмечено, что уже к 6-му месяцу послеоперационного периода данные показатели снижаются, а к 12-му месяцу после операции приходят в норму, характерную для здорового человека.
Уровень выраженности болевого синдрома индекса SF-36 значительно снижается к 3-му месяцу, а к 6-му месяцу уже не отличается от нормальных величин. Выраженность боли в послеоперационном периоде у пациентов, пластика которым выполнялась с использованием синтетического имплантата, достоверно выше, чем у больных с пластикой местными тканями. Остальные используемые шкалы индекса SF-36 у больных обеих групп постепенно повышаются к 3-му и 6-му месяцам послеоперационного периода, а к 12-му месяцу становятся такими же, как и у здоровых людей.
За всё продолжительное время наблюдения нами не было отмечено ни одного рецидива заболевания в обеих группах.
У пациентов с ГПОД, у которых в ходе обследования была выявлена метаплазия СОП, выполнение антирефлюксного оперативного вмешательства приводит к выраженному снижению воспалительных проявлений на слизистой оболочке пищевода, что в свою очередь делает возможным проведение коагуляции в благоприятных условиях.
Осложнений во время аргон-плазменной коагуляции отмечено не было.
Пациентам с диагностированной метаплазией СОП было выполнено от 2 до 5 сеансов АПК.
Морфологически подтверждена полная регрессия метаплазии слизистой оболочки пищевода путём замещения его многослойным плоским эпителием при контрольном исследовании биопсийного материала после окончания всех курса лечения. В нашем исследовании мы не отметили рецидива метаплазии слизистой оболочки пищевода в течение пяти лет после проведённого комплексного лечения.
Обсуждение
За последние десятилетия лапароскопическое устранение ГПОД постепенно заменило «открытую» операцию, став стандартным подходом к лечению данной патологии [7]. Что касается вопроса эффективности применения сетчатых имплантатов для пластики пищеводного отверстия диафрагмы, то он до сих пор остается спорным. По данным Guan L. и соавт., одним из важных элементов для предотвращения анатомического рецидива грыжи является надлежащее закрытие пищеводного отверстия диафрагмы и укрепление его сеткой [7]. В другом исследовании авторы хоть и отмечают преимущества аллопластики с точки зрения улучшения качества жизни и снижения риска рецидива грыжи, но в то же время описывают необходимость дальнейших исследований, чтобы определить чёткие показания к использованию сетчатых имплантатов [8].
Проведённый обзор литературы показал, что практически отсутствуют работы, посвящённые анатомическим исследованиям в области пищеводного отверстия диафрагмы для обоснования применения синтетических материалов. По результатам наших анатомических исследований установлено, что у пациентов со II зрелого периода с учётом уменьшения кровоснабжения фасциальных и мышечных тканей, в результате чего возникает ишемия зоны пищеводного отверстия диафрагмы (особенно у пациентов брахиморфного телосложения), применение исключительно собственных тканей с целью закрытия дефекта ПОД недостаточно и анатомически и физиологически слабо обосновано.
Как известно, использование синтетических материалов в брюшной полости может сопровождаться травматизацией органов и риском развития специфических осложнений, таких как аррозия и пролежни пищевода и желудка имплантом (вплоть до перфорации), поэтому установка сетчатого имплантата в заднее средостение над диафрагмальными ножками, последующее их ушивание предотвращают контактирование имплантата с полыми органами брюшной полости и позволяют надежно укрепить крурорафию [1].
В нашем исследовании осложнения в позднем послеоперационном периоде у пациентов после выполнения пластики пищеводного отверстия диафрагмы с использованием сетчатого имплантата отмечались реже, чем у группы больных с пластикой местными тканями, что, на наш взгляд, может быть связано с особенностями отбора пациентов в группы и выбранными топографо-анатомическими предпосылками для установки сетчатых имплантатов, основывающихся на данных анатомических исследований.
Данные о качестве жизни пациентов в послеоперационном периоде, полученные в ходе использования опросников, указывают на улучшение качества жизни пациентов в обеих группах. Сравнительный анализ этих данных с данными, полученными другими авторами, демонстрирует схожие результаты [9].
Восстановление нормальных морфофункциональных взаимоотношений тканей пищеводно-желудочного перехода в ходе антирефлюксной операции приводит к снижению частоты рефлюксов, что в свою очередь приводит к стиханию воспалительных изменений на слизистой пищевода. Эндоскопическая эрадикация очагов метаплазии после оперативного вмешательства по устранению ГПОД проводится в более благоприятных условиях, что позволяет улучшить отдаленные результаты лечения, что подтверждается и в практике других клиницистов [10].
Заключение
Разработанный алгоритм оперативного лечения даёт возможность подобрать метод пластики ПОД дифференцированно, основываясь на данных о размерах дефекта ПОД, типах телосложения, состоянии и характеристиках фасциальных и мышечных структур зоны ПОД, а также о возрасте пациента.
Новый хирургический метод укрепления крурорафии с использованием сетчатого имплантата, который был разработан нами, позволяет избежать возможного контакта сетки с полыми органами брюшной полости, что в свою очередь значительно снижает характерные для данной категории больных риски послеоперационных осложнений.
Разработанный дифференцированный способ АПК метапластических участков слизистой пищевода, зависящий от величины МДЦСМ, предоставляет возможность значительно уменьшить количество осложнений, как интра-, так и послеоперационных. Данный способ хорошо переносится больными, и его можно выполнять в амбулаторных условиях.
Выполнение малоинвазивных видеоэндоскопических оперативных вмешательств с опорой на разработанный нами алгоритм дифференцированного подхода к пластике ПОД различными вариантами доказало свою высокую эффективность и позволило значительно улучшить качество жизни и снизить число осложнений в послеоперационном периоде у пациентов, страдавших осложнёнными формами грыж пищеводного отверстия диафрагмы.
Список литературы
1. Sovpel I, Ishchenko R, Sedakov I, Sovpel O, Mykhaylichenko V, Parshin D. Modern aspects of diagnosis and surgical treatment of hiatal hernias: literature review. Archiv Euro-Medica. 2022;12(1):55-60. https://orcid.org/10.35630/2199-885x/2022/12/1.13
2. Михалева Л.М., Войтковская К.С., Федоров Е.Д., Бирюков А.Е., Грачева Н.А., и др. Клинико-морфологический анализ дисплазии при пищеводе Барретта и цилиндроклеточной метаплазии. Альманах клинической медицины. 2020;48(2):94-101. https://orcid.org/10.18786/2072-0505-2020-48-011
3. Petric j, Bright T, Liu DS, wee Yun M, watson DI. Sutured Versus Mesh-augmented Hiatus Hernia Repair: A Systematic Review and Meta-analysis of Randomized Controlled Trials. Ann Surg. 2022;275(1):e45-e51. https://orcid.org/10.1097/SLA.0000000000004902
4. Campos V, Palacio DS, Glina F, Tustumi F, Bernardo wM, Sousa AV. Laparoscopic treatment of giant hiatal hernia with or without mesh reinforcement: A systematic review and meta-analysis. Int J Surg. 2020;77:97-104. https://orcid.org/10.1016/j.ijsu.2020.02.036
5. Rausa E, Manfredi R, Kelly ME, Bianco F, Aiolfi A, et al. Prosthetic Reinforcement in Hiatal Hernia Repair, Does Mesh Material Matter? A Systematic Review and Network Meta-Analysis. J Laparoendosc Adv Surg Tech A. 2021;31(10):1118-1123. https://orcid.org/10.1089/lap.2020.0752
6. Stawinski PM, Dziadkowiec KN, Kuo LA, Echavarria j, Saligram S. Barrett's Esophagus: An Updated Review. Diagnostics (Basel). 2023;13(2):321. https://orcid.org/10.3390/diagnostics13020321
7. Guan L, Nie Y, Yuan x, Chen j, Yang H. Laparoscopic repair of giant hiatal hernia for elderly patients. Ann Transl Med. 2021;9(8):704. https://orcid.org/10.21037/atm-21-1495
8. Laxague F, Sadava EE, Herbella F, Schlottmann F. when should we use mesh in laparoscopic hiatal hernia repair? A systematic review. Dis Esophagus. 2021;34(6):doaa125. https://orcid.org/10.1093/dote/doaa125
9. Chan DL, Tran S, Kanakaratne S, Bruce HM, Thilakanathan C, et al. Long-term outcomes and satisfaction of laparoscopic non-absorbable mesh-reinforced hiatal hernia repair. Surgery Open Digestive Advance. 2022;6:100042. https://orcid.org/10.1016/j.soda.2022.100042
10. Mittal SK, Baboli KM, Bremner RM. Reflux Control Aſter Barrett’s Esophagus Ablation. Foregut. 2021;1(1):78-85. https://orcid.org/10.1177/2634516121997233
Об авторах
Д. М. ЧеркасовРоссия
Черкасов Денис Михайлович, д.м.н., профессор кафедры хирургических болезней № 2
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
М. Ф. Черкасов
Россия
Черкасов Михаил Федорович, д.м.н., профессор, заведующий кафедрой хирургии № 4
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
В. К. Татьянченко
Россия
Татьянченко Владимир Константинович, д.м.н., профессор, заведующий кафедрой оперативной хирургии, клинической анатомии и патологической анатомии ФПК и ППС
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Ю. М. Старцев
Россия
Старцев Юрий Михайлович, к.м.н., доцент кафедры хирургии № 4
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
С. Г. Меликова
Россия
Меликова Сабина Гаджиевна, врач-хирург
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
К. М. Галашокян
Россия
Галашокян Карапет Мелконович, к.м.н., ассистент кафедры хирургии № 4
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
А. В. Скуратов
Россия
Скуратов Андрей Владимирович, к.м.н., ассистент кафедры гастроэнтерологии и эндоскопии
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
К. В. Ендоренко
Россия
Ендоренко Константин Вячеславович, ассистент кафедры нормальной анатомии
Ростов-на-Дону
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Рецензия
Для цитирования:
Черкасов Д.М., Черкасов М.Ф., Татьянченко В.К., Старцев Ю.М., Меликова С.Г., Галашокян К.М., Скуратов А.В., Ендоренко К.В. Хирургические аспекты лечения грыж пищеводного отверстия диафрагмы. Медицинский вестник Юга России. 2024;15(4):104-112. https://doi.org/10.21886/2219-8075-2024-15-4-104-112
For citation:
Cherkasov D.M., Cherkasov M.F., Tat’yanchenko V.K., Starcev Y.M., Melikova S.G., Galashokyan K.M., Skuratov A.V., Endorenko K.V. Surgical aspects of treatment of hiatal hernia. Medical Herald of the South of Russia. 2024;15(4):104-112. (In Russ.) https://doi.org/10.21886/2219-8075-2024-15-4-104-112
JATS XML







































